第五章测试1.
第二类导体又称离子导体,下面对它的特点描述不确的是( )
A:导电总量分别由正、负离子分担 B:温度升高,电阻升高 C:正、负离子作反向移动而导电 D:导电过程中有化学反应发生
答案:B
2.
在一定温度和浓度的水溶液中,一般情况是带相同电荷的Li+, Na+, K+, Rb+,它们的离子半径依次增大,但其离子摩尔电导率恰也依次增大,这是由于( )
A:电场强度的作用依次减弱 B:离子的水化作用依次减弱 C:离子的迁移数依次减小 D:离子的电迁移率依次减小 3.
Al2(SO4)3的化学势 m 与 Al3+, SO42- 的化学势 m+ , m_之间的关系为( )
A:m = m+ + m_ B:m =3m+ + 2m_ C:m =2m+ + 3m_ D:m = m+ · m_ 4.
298K时,H2SO4当溶液的质量摩尔浓度从0.01 mol·kg-1增加到0.1 mol·kg-1时,其电导率 k 和摩尔电导率 Lm 将( )
A:k 增加, Lm 增加 B:k 减小, Lm 增加 C:k 增加, Lm 减小 D:k 减小, Lm 减小 5.
下列电池中,哪个电池的电动势与Cl-的活度无关?( )
A:
Zn(s)︱ ZnCl2(aq) ︱Cl2 (g) ︱ Pt(s)
B:Ag(s) ︱AgCl(s) ︱ KCl(aq) ︱Cl2 (g) ︱ Pt(s)
C:Hg(l)︱Hg2Cl2 (s) ︱ KCl(aq) ‖ AgNO3(aq) ︱Ag(s)
D:Zn(s)︱ ZnCl2(aq) ‖ KCl(aq) ︱ AgCl(s) ︱ Ag(s)
6.如果规定标准氢电极的电极电势为1V,则可逆电极的标准还原电极电势j$和电池的标准电动势 E$ 将如何变化( )
A:
j$和 E$ 各增加1V
B:j$减少1V, E$ 不变
C:j$增加1V,E$ 不变
D:j$和 E$各减少1V
7.质量摩尔浓度为1.0mol·kg-1的 K4[Fe(CN)6] 溶液的离子强度为( )
A:
15 mol·kg-1
B:4 mol·kg-1
C:7 mol·kg-1
D:10 mol·kg-1
8.使2000A的电流通过一个铜电解器,在1h内,能得到铜的质量( )
A:
10 g
B:2369 g
C:500 g
D:1285 g
9.已知电极Tl 3+, Tl +︱Pt的电极电势 , 电极Tl+︱Tl (s) 的电极电势
, 电极Tl+︱Tl (s) 的电极电势 ,
,
则电极Tl3+︱Tl (s) 的电极电势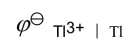 为( )
为( )
A:
0.914 V
B:1.586 V
C:2.164 V
D:0.721 V
10.下列描述正确的是( )
A:原电池的正极是阳极 B:电解池的正极是阳极 C:电解池的负极是阳极 D:原电池的负极是阳极







