- 溶液的化学势等于溶液中各组分的化学势之和。( )

- 二组分的理想液态混合物的蒸气总压力介于二纯组分的蒸气压力之间。( )
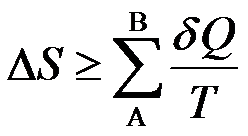
- 若A分子和B分子之间的相互作用力与A、B各自处于纯态时分子之间的相互作用力相同,混合后,则有ΔmixH = 0。 ( )
- 依据相律,恒沸点混合物的沸点不随外压的改变而改变。( )

- 在大气压力下,I2(s)在H2O(l)和CCl4(l)两个完全不互溶的液相中达分配平衡。设平衡时I2(s)已不存在,则该系统的组分数和自由度数分别为( )
- 实际气体进行绝热自由膨胀,ΔU和ΔS的变化为 ( )
- 对于与本身的蒸气处于平衡状态的液体,通过下列哪种作图法可获得一直线( )
- 一种实际气体,状态方程为pVm=RT+αp(α<0),该气体经节流膨胀后 ( )
- 在下列有关化学势的表达式中,正确的是 ( )


- 1 mol理想气体在简单的状态变化中从T1、p1、V1变到T2、p2、V2,在计算该过程的熵变时,错误关系式是( )
- 在绝热的刚性容器中,发生了不做非膨胀功的某化学反应,实验测得容器的温度升高500 K,压力增大了2026 kPa,则此反应过程的ΔrU、ΔrH、ΔrS、ΔrA变化为( )。
- 在50 g CCl4中溶入0.05g C10H8,测得溶液沸点升高了0.04 K,若在同量CCl4中溶入0.05 g未知物,沸点升高了0.06 K。此未知物的分子量为( )
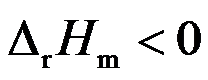

- 理想气体从同一始态(p1, V1, T1)出发,分别经恒温可逆压缩和绝热可逆压缩,环境所做的功分别为WT和WA。若压缩至同一终态体积V2,下述表述中正确的是( )
- 溶剂中溶入挥发性溶质,肯定会引起溶液的蒸气压升高。
- 根据热力学第一定律,因为能量不能无中生有,所以一个系统若要对外做功,必须从外界吸收能量。 ( )
- 一个已达平衡的化学反应,只有当标准平衡常数改变时,平衡才会移动。( )
- 功可以全部转化为热,但热不能全部转化为功。( )

- 系统达平衡时熵值最大,Gibbs自由能最小。( )
- 根据C(石墨)=C(金刚石)的化学平衡原理。金刚石只有在高温高压下才能合成。( )

- 在抽空密闭容器中加热NH4Cl(s),有一部分分解成NH3 (g)和HCl(g),当体系建立平衡时,其独立组分数和自由度是C=1、f=1。( )
- 定温定压下,A与B组成的均相系统,若A的偏摩尔体积随浓度的改变而增加,则B的偏摩尔体积随浓度将 ( )
- 非电解质A和B组成非理相溶液,若以UA-B、UA-A和UB-B分别表示分子A与B、A与A及B与B之间的作用能,当UB-B>UA-B、UB-B>UA-A时,则体系相对于拉乌尔定律产生负偏差。( )
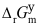
- 下列哪个关系式不是化学势( )
- 在温度为T,压力为p时,反应3O2 (g) = 2O3 (g)的Kp与Kx的比值为( )
- 各种运动形式的配分函数中与压力有关的是( )
- 在298 K,101.3 kPa下,2 mol甲苯与50 mol的苯组成混合物,其中甲苯的化学势为μ1;又4 mol 甲苯加100 mol 苯组成的混合物,其甲苯的化学势为μ2,则两者的关系为 ( )
- 410 K时,纯氯苯的蒸汽压为115.71 kPa,纯溴苯为60.79 kPa,在此温度下,与含氯苯的物质的量分数为0.35的蒸汽成平衡的氯苯与溴苯溶液中氯苯的物质的量分数为( )
- 某一水溶液共有S种溶质,相互之间无化学反应。若该水溶液与纯水达到渗透平衡时,则该系统的自由度数为( )
- 298K时,将11.2dm3 O2与11.2dm3 N2混合成11.2dm3的混合气体,该过程 ( )
- 对热力学能的意义,下列说法中正确的是 ( )
- H2O、K+、Na+、Cl–、I– 体系的独立组分数是 ( )
- 下列过程中体系的熵减小的是( )

- 一定量理想气体从同一始态出发,分别经两个过程达到相同压力的终态,①等温压缩,焓变∆H1,②绝热压缩,焓变为∆H2,两者之间的关系为 ( )
- 两种理想气体在等温下混合( )
- CO2分子转动时,它对热力学能U r的贡献为( )
- 一定量理想气体经等温恒外压压缩至终态,这时系统和环境的熵变应为 ( )
- 体系经历一个不可逆循环后( )
- 硫存在着单斜、斜方、液态和蒸气四种不同的物态,故在硫的相图中三相点的数目可高达( )
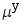
- 1 mol A与n mol B组成的溶液,体积为0.65 dm3,当xB = 0.8时,A的偏摩尔体积VA,m = 0.090 dm3·mol-1,那么B的偏摩尔VB,m 为( )
- 在一绝热的气缸(活塞也绝热)中有1mol理想气体,其始态为p1、V1、T1,经可逆膨胀到p2、V2、T2,再恒外压将气体压缩至V3=V1的终态,则整个过程的W、ΔH、ΔS分别为( )
- 对双原子分子理想气体,发生一个物理变化,欲求其热力学性质,需要知道( )
- 二组分体系最多可平衡共存的相数为( )
- A、B两液体混合物在T - x图中出现最低点,则该混合物对Raoult定律产生( )
- 1 mol、373 K、100 kPa下的水经下列两个过程变为373 K、100 kPa下的水汽:①等温等压可逆蒸发;②向真空蒸发。则两个过程中功和热的关系为 ( )
- 在等容条件下,将100 dm3单原子理想气体从273 K,101.3 kPa加压到202.6 kPa,则其ΔU和ΔH分别为( )
- 液态苯在一绝热钢性的氧弹中燃烧,其化学反应为C6H6(l)+7.5O2(g) = 6CO2(g)+3H2O(g) ,则下面表示正确的是 ( )
- 某一固体在298 K和101.3 kPa下升华,这意味着( )

- 270 K、100 kPa时,1 mol水凝结为同温同压下的冰,则系统和环境的熵变分别为( )
- 统计热力学是系统宏观状态函数与微观性质的联系桥梁,大量微观粒子性质的集合统计平均体现在配分函数上,系统的宏观性质可直接用配分函数计算。( )
- 对双原子分子理想气体的一般物理过程,下面关于系统熵函数和各运动形式对熵的贡献,描述错误的是( )
- 选择不同的能量零点对配分函数和热力学函数没有影响。( )
- 下面关于Maxwell-Boltzmann统计、Bose-Einstein统计和Fermi-Dirac统计的描述中,正确的是 ( )
- 体积为1cm3,质量为m克的单原子分子理想气体,在温度为T时,对一般的物理过程,分子的平动配分函数为 ( )
- 假定某种分子的许可能级是0,ε,2ε和3ε,简并度分别为1,1,2,3。四个这样的分子构成的定位系统,其总能量为3ε时,系统的微观状态数为 ( )
- 下面关于等概率假设的描述正确的是( )
- Boltzmann分布定律适用于粒子数N很大的独立子系统在各分子态中的分布;由Boltzmann分布定律可知,系统平衡时ni/N的值是一定的(ni是能量为εi的分子态中分布的粒子数)。( )


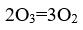







- 对于只有一对液体部分互溶的三液系统,下列说法中不正确的是( )。
- 已知A和B可构成固溶体,在组分A中若加入组分B可使固溶体的熔点提高,则组分B在此固溶体中的含量与组分B在液相中的含量相比( )。
- 关于相的下列说法,不正确的是( )。
- 关于能形成完全互溶固溶体的二组分系统,下列说法不正确的是( )。

- 对于恒沸点混合物,下列说法中错误的是( )。
- 压力升高时,单组分系统的熔点将( )。

- 下列系统不适用分配定律的是( )。
- 下列叙述中错误的是( )。
- 若用四维空间的相图来描述三组分体系的相平衡状态,则相数最多的区域是( )。
- 吐鲁番盆地的海拨高度为-154米。在此盆地,水的沸点是( )。


- 对于纯物质的任意两相平衡体系,在下列平衡压力与温度的关系式中不正确的是( )。
- 有下列四种关于物质的聚集状态与相之间的关系的叙述: (1)同一态中的 物质必为同一相 (2)同一相中的物质必为同一态(3)同一态中的物质不一定是同一相 (4)同一相中的物质不一定是同一态其中正确的是( )。
- 在电化学测量中,常会用到镉标准电池,若要求液相中Cd的浓度不因Cd的量发生微小变化而变化,则在293 K时,镉汞齐电极中Cd的浓度处于( )。

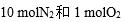
- 在100 kPa下,往纯水中加入少量KCl,与纯水相比,此稀溶液的沸点升高。
- 混合体系的某组分的广度性质,其偏摩尔量与其物质的量的乘积具有加和性。
- 在相同温度和压力下,纯溶剂的化学势大于其在稀溶液中的化学势。
- 标准态是人为规定的某些特定状态。
- 在相同温度和压力下,纯溶剂的蒸气压大于其混合溶液的蒸气压。
- 混合体系中,某组分B用Gibbs自由能表示的化学势也是其偏摩尔量。
- 偏摩尔体积是强度性质,因此由A和B组成的混合系统,不论系统的组成如何变化,A和B的偏摩尔体积不变
- 自发进行的相转移过程,组分B总是由化学势较大的一相流向化学势较小的一相。
- 混合体系中,某组分B的化学势可以用U、H、A、G对组分B的物质的量的偏微分表示,因限定条件不同,所以,四种热力学函数表示的化学势数值也不同。
- 只有在等温、等压、除B以外的其他组分的量保持不变时,某广度性质对组分B的物质的量的偏微分才称为偏摩尔量。
- 下列哪个不是稀溶液的依数性( )。
- 定温定压条件下,混合体系中,组分B的偏摩尔量也是其化学势。
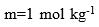
- 在等温、等压条件下,溶剂A和溶质B形成一定浓度的稀溶液,采用不同浓度表示的话,则( )。
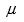
- 下列表达式与拉乌尔定律无关的是( )。
- A和B的摩尔体积没有相关性,二者形成的混合液中,二者的偏摩尔体积之间也没有相关性。
- 理想液态混合物的混合性质是( )。
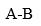
- 下列关于化学势的关系式,不正确的是( )。
- 在相同温度和压力下,相同质量摩尔浓度的食盐水和葡萄糖水的渗透压是一样的。
- 定温、定压下,A和B组成的均相系统,若A的偏摩尔体积随系统的组成的变化而增大,那么B的偏摩尔体积随系统组成的变化将( )。
- 关于化学势的表达式,正确的是( )。
- 关于拉乌尔定律,下列描述哪个是正确的( )。
- 由A和B两种液体组成的混合物溶液的体积与下面哪些因素无关?
- 稀溶液的凝固点降低、沸点升高等依数性均是因为稀溶液导致溶剂的蒸气压降低。
- 关于气体化学势的描述,不正确的是( )。
- 关于偏摩尔量的表达式,正确的是( )。
- 对理想溶液的形成过程,下列表达式不正确的是( )。
- (a) H2和O2在绝热钢瓶中发生反应生成水;(b) 液态水在373 K和101.3 kPa下蒸发成水蒸汽。(a)和(b)两个过程的热力学函数ΔA的变化均大于零。( )
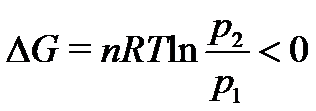
- 有两个可逆Carnot热机,在高温热源温度为500 K,低温热源分别为300 K和250 K之间工作,若两者分别经一个循环后所作的功相等,则两个热机的效率相等,但两个热机自低温热源吸收的热量和向高温热源放出的热量不等。( )
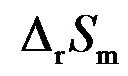
- 下列过程中可直接用dH = TdS + Vdp公式进行计算的过程是 ( )。
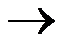
- 1 mol理想气体从p1、V1、T1分别经:(a) 绝热可逆膨胀到p2、V2、T2;(b) 绝热恒外压膨胀到p3、V3、T3,若p2 = p3,则 ( )。
- nmol某气体的恒容下由T1加热到T2,其熵变为ΔS1,相同量的气体在恒压下由T1加热到T2,其熵变为ΔS2,则ΔS1与ΔS2的关系为 ( )。
- 下面关系式中不正确的是 ( )。
- 下列各过程中U、H、S、G及A均为零的是 ( )。
- 101.3 kPa下的水经下列两个不同过程变为373.2 K、101.3 kPa 下的水汽:(1)等温等压可逆蒸发;(2)向真空蒸发。则(1)、(2)两个过程中,下列关系正确的是 ( )。
- 一理想气体在500 K时作等温膨胀,已求得系统的熵变ΔS=10 J∙K−1。若此过程中系统做功仅是最大功的1/10,则系统从热源中吸热( )。
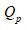
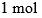
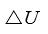
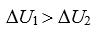
- 绝热圆筒上有一理想的 (无摩擦无重量的) 绝热活塞内放入理想气体,内壁绕有电阻丝,当通电时气体慢慢膨胀,以气体和电阻丝为体系,则 ( )
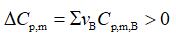
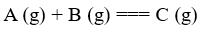
- 下列公式不受理想气体条件限制的是 ( )。
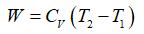
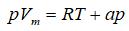
- 物理化学的发展意义是什么( )?。
答案:错
答案:错
答案:对
答案:错
答案:对
答案:错
答案:0.64
答案:C=3,f *=2
答案:ΔU=0,ΔS>0
答案:

答案:温度下降
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!



