第四章测试1.反应 N2(g)+3H2(g)
 2NH3(g)
2NH3(g) 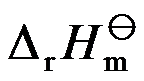 = -92kJ·mol-1,从热力学观点看要使H2达到最大转化率,反应的条件应该是( )
= -92kJ·mol-1,从热力学观点看要使H2达到最大转化率,反应的条件应该是( )A:低温低压 B:高温高压 C:低温高压 D:高温低压
答案:C
2.下列叙述中正确的是( )。
A:平衡常数不随温度变化 B:平衡常数随起始浓度不同而变化 C:一种反应物的转化率随另一种反应物的起始浓度不同而异 D:反应物的转化率不随起始浓度而变 3.增加反应物浓度,反应速率加快的主要原因是( )。
A:反应的活化分子数比例增加 B:反应物的活化能下降 C:反应的活化分子数增加 D:单位时间内分子间碰撞数增加 4.反应A + B
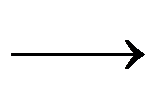 3C正逆反应的活化能分别为m kJ·mol-1和n kJ·mol-1,则反应的ΔrHm / kJ·mol-1为( )。
3C正逆反应的活化能分别为m kJ·mol-1和n kJ·mol-1,则反应的ΔrHm / kJ·mol-1为( )。 A:m - 3n B:m - n C:n - m D:3n – m 5.关于催化剂的作用,下述中不正确的是( )。
A:能改变某一反应的正逆向速率的比值 B:能缩短到达平衡的时间,但不能改变某一反应物的转化率 C:在几个反应中,能选择性地加快其中一、二个反应 D:能够加快反应的进行
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!







