中国石油大学(华东)
- 某绝热的房间内放一冰箱,通电后若打开冰箱门,则房间内的温度将逐渐下降。( )
- Virial方程中B12反映了异分子间的相互作用力,因此B12=0的气体必定是理想气体混合物。( )
- 孤立体系的熵一定恒定。( )
对于给定温度和压力下的二元系统,如果知道活度系数的信息,就能够计算其相互溶解度,如果相α组分1富集,而相β组分2富集,则
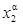 、
、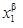 为两个相互溶解度。相互溶解度受温度的影响很大。( )
为两个相互溶解度。相互溶解度受温度的影响很大。( ) - 普遍化第二virial系数法只适合于低压非极性气体,适用范围较窄。( )
- 偏心因子可用于正常流体,也可用于H2、He等量子流体或强极性流体和氢键流体。( )
- 理想气体的定压热容和定容热容之间的关系:Cp−Cv=R。( )
- 热力学效率表示能量利用真实过程与可逆过程的差距,因此,热力学效率必然小于1。( )
- 理想功就等于可逆功。( )
- 正规溶液的混合焓变为0,混合体积变化为0。( )
- SRK方程和PR方程能同时适用于汽、液两相,在工业中得到广泛应用。( )
- 经典热力学只从宏观角度研究大量分子组成的体系,达到平衡时所表现出的宏观性质。只能以实验数据作为基础,利用热力学函数和物质状态之间的关系进行宏观性质的关联,从某些宏观性质推算另一些宏观性质。( )
- SRK方程可以较好地预测石油馏分汽液平衡。( )
- virial(维里)方程的理论意义大于实际应用价值。( )
- virial方程是无穷级数的形式,实际中常采用截项的virial方程。( )
- 纯物质的平衡汽化过程,摩尔体积、焓、热力学能、Gibbs自由能的变化值均大于零。( )
- 在常温、常压下,将10cm3的液体水与20cm3的液体甲醇混合后,其总体积为30cm3,混合前后体积相等。( )
- 节流膨胀与等熵膨胀均是获取低温流体(即制冷)的方法,工程上常将两种膨胀结合并用。( )
- 物质的偏心因子是由蒸汽压定义的,它具有压力的单位。( )
- 偏心因子ω表示分子的偏心度或非球性,对简单球形流体(氩、氪、氙)的ω=0。( )
- 可逆过程不会产生㶲损失。( )
- 对于理想溶液,i组分在溶液中的逸度系数和i纯组分的逸度系数相等。( )
- 汽液两相平衡的条件是汽、液两相的逸度相等。( )
- 能量E由㶲(有效能)和火无(无效能)两部分组成。( )
- 对于状态函数来说,广度性质具有偏摩尔性质,而偏摩尔性质本身是强度性质。( )
- 不可逆过程中孤立体系的( )。
- 计算剩余焓和剩余熵的图解方法需要知道的已知条件是( )。
- 下列哪个设备是不属于消耗轴功的设备( )。
- 湿蒸汽的干度(或品质)是指( )。
- 某流体在稳流装置内经历一个不可逆绝热过程,所产生的功为25kJ,则流体的熵变为( )。
- 对于最高压力共沸体系,其特点不包括( )。
- 对戊醇和水形成的二元三相汽液液平衡体系,其自由度为( )。
- 下列关于超额Gibbs自由能GE关系式正确的是( )。
- 指定温度下的纯物质,当压力低于该温度下的饱和蒸气压时,则物质的状态为( )。
- 吸收式制冷循环中发生器、节流阀、吸收器和溶液泵这一溶液回路(又称“化学泵”)的作用相当于蒸汽制冷循环的( )。
- 关于用能过程热力学第二定律的描述,不正确的是( )。
- 混合物中组分i的逸度的完整定义式是( ) 。
- 工作于温度为600K和300K热源间的热机,工质从高温热源吸收100kJ的热量,则最多可做的功为( )kJ。
- 下列哪一项不属于偏摩尔性质计算过程中的常用工具( )。
- 合理地评价化工过程能量综合利用所采用的方法是( )。
- 相同的压力下,对外做功的绝热膨胀比节流膨胀温度降低的程度( )。
- 500℃恒温热源下100kJ的热量所具有的㶲为( ),设T0=298K。
- 某流体在稳流装置内经历一不可逆过程。加给装置的功为25kJ,从此装置散出的热量是10kJ。试问流体的熵变为( )。
- 热泵的工作原理与制冷机的原理( )。
- 对学过的状态方程的精度差异,下列那个是不正确的( )。
- 在工程上广泛采用的计算蒸气压的方程是( )。
- 在某一过程中,气体吸收了50 kJ的热量,同时热力学能增加了84 kJ,此过程中( )。
用
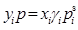 进行汽液平衡计算时,除了可以直接测定的T、p、yi和xi之外,只需要对饱和蒸气压和活度系数进行计算,其中计算活度系数可以选用相应的活度系数模型,下列哪个模型不在选用范围( )。
进行汽液平衡计算时,除了可以直接测定的T、p、yi和xi之外,只需要对饱和蒸气压和活度系数进行计算,其中计算活度系数可以选用相应的活度系数模型,下列哪个模型不在选用范围( )。- 有关物理㶲的描述,下列叙述不正确的是( )。
- 在流体流动和换热过程中,下列哪一项的大小影响过程的经济性( )。
A:错 B:对
答案:错
A:对 B:错
答案:B
A:对 B:错
答案:错
A:对 B:错
答案:对
A:对 B:错
答案:A:对
A:错 B:对
答案:A:错
A:对 B:错
答案:A: 对
A:对 B:错
答案:对
A:错 B:对
答案:B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
A:总熵是增加的,但㶲是减少的 B:总熵总是增加的,㶲也是增加的 C:总熵总是减少的,㶲也是减少的 D:总熵是减少的, 但㶲是增加的
A:
普遍化关联式
B:合适的状态方程
C:p-V-T实验数据
A:压缩机 B:水轮机 C:泵 D:鼓风机
A:饱和蒸汽的质量 B:湿蒸汽中所含饱和蒸汽的质量分数 C:湿蒸汽中所含饱和液体的质量分数 D:湿蒸汽的质量
A:不能确定 B:负 C:零 D:正
A:
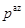 <
<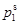 ,
, 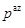 <
<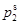
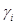 >1
>1
 >
>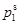 ,
, 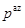 >
>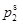
A:2 B:3 C:1 D:0
A:
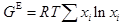
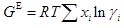
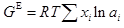
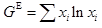
A:饱和蒸汽 B:过热蒸汽 C:液体 D:超临界流体
A:膨胀机 B:压缩机 C:冷凝器 D:节流阀
A:由火无转化为㶲是不可能的 B:实际过程中,有火无转化为㶲 C:只有可逆过程,㶲才守恒 D:在一切不可逆过程中,㶲转化为火无
A:
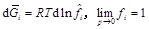

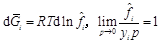
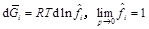
A:50 B:75 C:25 D:60
A:Gibbs-Duhem方程 B:集合公式 C:道尔顿分压定律 D:截距公式
A:
热力学第一和第二定律
B:热力学第二定律
C:热力学第一定律
A:大 B:小 C:相同
A:100kJ B:约40kJ C:约20kJ D:约60kJ
A:可正可负 B:负 C:正
A:相同 B:不同
A:vdW方程>RK方程 B:SRK方程>RK方程 C:PR方程>SRK方程 D:立方型EOS>两项截断virial方程
A:Antoine方程 B:克-克方程 C:状态方程 D:Clapeyron(克拉佩龙)方程
A:气体对环境做功134 kJ B:环境对气体做功34 kJ C:环境对气体做功134 kJ D:气体对环境做功34 kJ
A:SRK方程 B:van Laar方程 C:NRTL方程 D:Wilson方程
A:物系由所处的状态到达与环境成约束性平衡状态所提供的最大有用功 B:物理基态只需要确定环境状态的温度和压力 C:由于组成与环境模型不同时所具有的㶲 D:
物系仅由于温度、压力与环境模型的温度T0 、压力p0不同所具有的㶲
A:
过程的理想功
B:过程的损失功
C:流体流速
D:冷热流体温差
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!





