第五章测试1.对于多组份的封闭系统,反应向
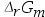 减小的方向进行。( )
减小的方向进行。( )A:错 B:对
答案:A
2.反应平衡常数值改变了,平衡一定会移动。( )
A:错 B:对 3.
在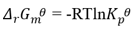 的等式中,
的等式中,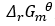 表示平衡状态时Gibbs自由能的变化值。( )
表示平衡状态时Gibbs自由能的变化值。( )
A:对 B:错 4.反应达到平衡后,增大压强,若
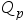 增加,则反应向逆向进行。( )
增加,则反应向逆向进行。( )A:对 B:错 5.600 K时,反应CO(g)+H2O(g)=CO2(g)+H2(g)的Kc、Kx、Kp关系为( )。
A:Kp<Kx<Kc B:Kp=Kx=Kc C:无法判断 D:Kp>Kx>Kc 6.已知某温度下CO(g)+H2O(g)=CO2(g)+H2(g)的
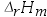 = -42 kJ·mol-1,
= -42 kJ·mol-1,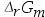 = -29 kJ·mol-1。下列关于该反应方向判断错误的是( )。
= -29 kJ·mol-1。下列关于该反应方向判断错误的是( )。A:升高温度,该反应逆向进行 B:增加压强,该反应一定不会移动 C:该条件下,该反应正向进行 D:该条件下,向反应体系中加入惰性气体,该反应一定不会移动 7.
对于以下两个反应:
(1)3H2(g)+N2(g)=2NH3(g) 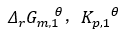
(2)3/2H2(g)+N2(g)= NH3(g) 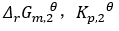
表达正确的是( )
A:
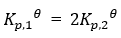
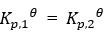
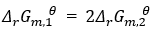
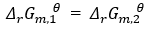
A:通入氮气,保持压力不变,体积增加一倍 B:气体总压减小到原来的一半 C:通入氯气, 保持体积不变,压力增加一倍 D:通入氮气,保持体积不变,压力增加一倍 9.已知某反应在610 K时的平衡常数为2.8,在620 K时的平衡常数为6.69,则该反应的
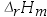 为( )。
为( )。A:274 J·mol-1 B:274 kJ·mol-1 C:-274 kJ·mol-1 D:无法确定 10.
在T=1000 K时,理想气体反应2SO3(g)=2SO2(g)+O2(g)的平衡常数Kp=29 kPa,则该反应的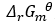 为( )。
为( )。
A:10.3 kJ·mol-1 B:28 kJ·mol-1 C:-28 kJ·mol-1 D:-10.3 kJ·mol-1
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!

