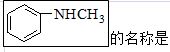
- 所有含有苯环的有机物都属于芳香烃。
- 配体数等于中心原子的配位数。
- 临床上的两种等渗溶液只有以相同的体积混合时,才能得到等渗溶液。
- 将浓度为c的醋酸稀释一倍,溶液中的[H+]为原来的1/2
- 具有未成对电子的两个原子相互接近时可以形成稳定的共价键
- 二甲胺的碱性比甲胺的强
- 对任何原子核外某一电子来说,只有四个量子数完全确定后,其能量才有一定值。
- 元素的电负性是指原子在分子中吸引成键电子的相对能力。某元素的电负性越大,表明其原子在分子中吸引成键电子的能力越强。
- 含有3个手性碳原子的化合物有8个光学异构体。
- 浓度相等的两种溶液之间一定不会发生渗透现象。
- 下列两两分子间,三种范德华力和氢键都存在的是
- 欲使相同温度的两种稀溶液间不发生渗透,应使两溶液(A,B中的基本单元均以溶质的分子式表示)
- 描述原子轨道的量子数组合是
- 人体必需脂肪酸不包括
- 多电子原子中,在主量子数为n,角量子数为l的亚层上,原子轨道数为
- 欲配制pH=10.0的缓冲溶液,下列四组缓冲体系中,应选择
- 能与甘油反应生成深蓝色溶液的是
- 某氨基酸的pI=6.4,它在pH=4.8的缓冲溶液中往哪个电极移动
- 可以鉴别葡萄糖和果糖的是
- 甲胺的结构式
- 存在顺反异构的是
- 常温下,相同浓度的HAc 与NaOH 溶液等体积混合,所得溶液的pH
- 中含有几个伯碳原子
- 不能与饱和亚硫酸氢钠溶液亲核加成的是
- 与碱性硫酸铜反应生成蓝色溶液的是
- 能与FeCl3发生显色反应的是
- 能与苯酚显色的是
- 一分子醛与两分子醇在干燥HCl的条件下,生成的化合物是
- H2CO3的Ka1、Ka2与Kw三个表达式中,[H+]数值关系是
- 当AgCl固体在水中的质量不发生变化时,此时溶液中的IP与Ksp的关系是
- 属于伯醇类的是
- 与卢卡斯试剂反应速率最快的是
- 酸性最强的是
- ① 甲酸、② 乙二酸、③ 苯甲酸、④ 丙酸的酸性由强到弱的顺序是:
- 不正确的说法是
- 下列化合物属于伯醇的是
- 298.15K时AgCl的溶解度S=1.33×10-5 mol·L-1 ,其Ksp (AgCl)为
- 氨基酸根据氨基和羧基的数目可分为
- 氨基酸在水溶液中发生电离后,三种离子同时存在
- pH>pI,氨基酸带负电
- 氨基酸从营养学角度可以分为
- 氨基酸处于等电状态时溶液的pH值,称为氨基酸的等电点
- 氨基酸自身不能发生酸碱反应
- 一般来说氨基酸的酸式电离强于碱式电离
- 氨基酸分子具有酸碱两性
- 某氨基酸的pI=10.74,在pH=7.35的缓冲溶液中做电泳实验,它往哪个极移动
- 某氨基酸的pI=4.50,它在pH=7.40的缓冲溶液中带何种电荷
- 各种氨基酸的等电点不同,在等电点时氨基酸的溶解度最小,可以利用调节溶液pH的方法分离、提纯不同的氨基酸。
- 缩二脲反应可以鉴别多肽或蛋白质。
- 氨基酸具有酸碱两性。
- 酸性氨基酸分子中含有一个氨基和两个羧基
- 中性氨基酸pH值等于7。
- 某氨基酸的pI=9.42,在pH=5.4的缓冲溶液中,该氨基酸在电泳中移向哪极
- 氨基酸命名时通常使用俗称
- 关于葡萄糖的描述正确的是
- 葡萄糖具有变旋光现象
- 葡萄糖变旋光现象产生的原因是环状结构和开链式结构相互转化,最终达到动态平衡导致的
- 葡萄糖分子中5号碳上的羟基在费歇尔投影式右侧,为D-葡萄糖
- 水溶液中,开链式葡萄糖分子占64%
- 在水溶液中,葡萄糖环状结构和开链式结构不能相互转化
- 从吡啶中结晶得到的葡萄糖晶体比旋光度为右旋,112度
- 在费歇尔投影式和哈沃斯式不能相互转化
- 葡萄糖分子不含有手性碳
- 葡萄糖在水溶液中不具有变旋光现象。
- 能鉴别葡萄糖和果糖的试剂是
- 果糖不能与Tollens试剂反应。
- 属于多糖的是
- 果糖能发生银镜反应。
- 下列糖在碱性条件下具有还原性的是
- 葡萄糖是还原性糖。
- 下列属于还原性糖的是
- 下列何者不是还原糖
- 关于皂化值的描述正确的是
- 下列物质不属于油脂的是
- 油脂酸败时会产生难闻的气味
- 油脂硬化后更容易被空气氧化、变质
- 皂化值可用来检验油脂的质量
- 简单甘油酯在命名时不需要标明高级脂肪酸的位次
- 油脂不能和碘发生反应
- 简单甘油酯可以命名为:三某脂酰甘油
- 皂化反应得到的高级脂肪酸盐称为肥皂
- 医学上的甘油三酯属于油脂
- 习惯上把在常温下呈液态的油脂称为脂肪
- 皂化值是指1g油脂完全皂化时所需氢氧化钾的毫克数。
- 油脂的加氢又称为油脂的硬化。
- 可以用碘值判断油脂的不饱和程度。
- 油脂包括油和脂肪
- 油脂是脂肪酸和甘油形成的酯
- 可以根据皂化值的大小,可以判断油脂中所含三酰甘油的平均分子量。
- 油脂是高级脂肪酸和甘油形成的甘油酯
- 油脂在碱性条件下水解反应,称为
- 油脂在空气中放置过久会产生难闻的气味,这种现象称为油脂的
- 简单的胺命名时以胺为母体
- 季铵碱是强碱
- 氨基是伯胺的官能团
- 氨分子中三个氢原子全被烃基取代得到季铵类化合物
- 伯仲叔胺和伯仲叔醇的分类方法不一样
- 叔丁胺是叔胺
- 氮原子上连有不同脂肪烃基,命名时较优先的烃基写在后面
- 对于比较复杂的胺,命名时可以将氨基作为取代基
- 氨分子中的三个氢都被取代属于仲胺
- N-乙基苯胺的结构式




- 下列化合物中对映异构体数目少于2n的是
- 属于S型的是
- 不含手性碳的化合物一定不是手性化合物。
- 有对称面和对称中心的化合物一定不是手性化合物。
- 下列那一对是相同化合物
- . 书写费歇尔投影式的时候,竖键上的两个基团朝向前方。
- 构型是S型的是
- 有关对映异构现象叙述正确的是
- 费歇尔投影式在纸面上旋转90°,其构型不变。
- 下列化合物酸性由强到弱排列顺序正确的是① α-丙酮酸 ② α-羟基丙酸 ③ 2-甲基丙酸 ④ 丙酸
- 溴乙酸的酸性大于乙酸的主要原因是分子中存在
- 下列化合物不能够发生碘仿反应的是
- 酮体包括β-丁酮酸、β-羟基丁酸和丙酮。
- 醛与醇的反应属于
- 稀碱条件下不能发生碘仿反应的是
- 不能与氢氰酸反应的是
- 用于保护醛基的反应是
- 下列化合物能与HCN发生亲核加成反应的是
- 下列化合物中,不能与NaHSO3饱和溶液反应的是
- 可以用新制备的氢氧化铜鉴别邻二醇。
- 苯酚可以和三氯化铁作用显颜色。
- 能与FeCl3显色的物质是
- 可与三氯化铁显色的是
- 邻二醇不能与新制备的氢氧化铜反应。
- 可鉴别邻多醇的是
- 遇碱性硫酸铜显蓝色的是
- 遇卢卡斯试剂,先浑浊的是
- 可鉴别甘油和丙醇的是
- 能与碱性硫酸铜发生反应,生成蓝色溶液的是
- 酸性最强的物质是
- 苯与溴的反应机理为
- 卢卡斯试剂的化学成分是
- 属于酚类的是
- 是活化基团的是
- 定位基 –Cl 属于
- 下列属于邻对位定位基的是
- 常见的稳定的单环烷烃是五元环和六元环。
- 苯环上的卤代反应属于加成反应。
- 苯与溴水反应的机制是
- 存在着p-p共轭效应的是
- 最稳定的是
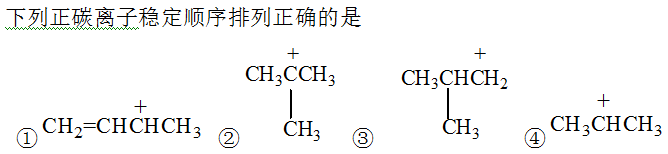
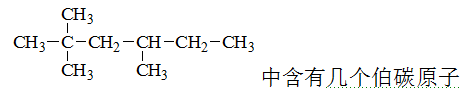
- 依据次序规则,最优先的是
- 下列最稳定的是
- 含伯、仲、叔、季碳原子的是
- 烯烃与溴化氢的反应(存在过氧化物)属于
- 存在顺反异构体的是
- 螯合物的配体是多齿配体,与中心原子形成环状结构,故螯合物稳定性大。
- 因配离子在水中很稳定,不易解离,所以是一种极弱的酸。
- 螯合环越大,螯合物就越稳定。
- 对于不同的配合物,Ks较大者配合物越稳定。
- 配合物Cu2[SiF6]的正确名称是
- 在pH=8.5的[Cu(NH3)4] SO4溶液中,存在平衡:[Cu(NH3)4]2+ Cu2+ + 4NH3。向溶液中分别加入以下试剂,使平衡向右移动的是
- 配合物(NH4)3[SbCl6]的中心离子氧化值和配离子电荷分别是
- 欲使CaCO3在水溶液中的溶解度增大,宜采用的方法是
- 二羟基四水合铝(Ⅲ)配离子的化学式是
- 下列配合物中,只含有多齿配体的是
- 在配合物[Co(en)3]2(SO4)3中,中心离子的配位数和氧化值分别是
- 2p能级上的3个原子轨道的形状和延伸方向完全相同,所以称为简并轨道。
- 下列液态物质同时存在取向力、诱导力、色散力和氢键的是:
- 水的反常沸点,归因于分子间存在氢键缔合作用
- H2O的沸点比H2S的沸点高得多,主要原因是
- C2H4中C原子的杂化方式为
- 下列化合物中存在p-π共轭的是( )
- 在杂化轨道理论中,正确的是
- He原子的1s轨道有两个电子,因此,He原子不能形成双原子分子
- 分子中键角最大的是
- 在下列分子或离子中,中心原子采用等性sp3杂化成键的是
- π键只能与α键同时存在,在共价双键和共价叁键中只能有一个α键
- 如果某一个原子没有单电子,则不能形成共价键
- 原子核外每一电子层最多可容纳2n2个电子,所以元素周期系第五周期有50种元素
- 电子总是尽可能地先占据能量最低的轨道,当能量最低的轨道已充满后,才依次进入能量较高的轨道。
- 下列符号表示的原子能级,不可能存在的是
- 表示原子轨道角度分布的函数是
- 根据Pauling原子轨道近似能级图,下列各能级中,能量最高的是
- 基态11Na 原子最外层电子的四个量子数可能是
- 在多电子原子中,原子核对核外某一电子的吸引力由于其余电子对该电子的排斥作用而被减弱,犹如减少了核电荷数,减少后的核电荷数称为有效核电荷数。
- 2p轨道的磁量子数可能有
- 轨道角动量量子数l=2的某一电子,其磁量子数m
- BaSO4在纯水中的溶解度与在生理盐水中溶解度相同。
- 在含有0.01 mol·L-1 Ca2+离子的溶液中,通入足量CO2的气体,将会产生CaCO3沉淀。
- IP和Ksp的表达形式类似,但其含义不同。Ksp表示难溶电解质的饱和溶液中离子浓度幂的乘积,仅是IP的一个特例。
- 由于Ksp (CaSO4)>( KspCaCO3),所以在固体CaSO4中加入Na2CO3溶液,CaSO4将会转化为 CaCO3。
- 两种难溶电解质,Ksp小的,溶解度一定小
- 欲增加Mg(OH)2在水中的溶解度,可采用的最佳方法是
- Mg(OH)2的溶度积表达式是
- 已知CaCO3的Ksp= 2.9×10-9,H2CO3的Ka1= 4.2×10-7,Ka2 = 5.6×10-11,将1.0 mol·L-1CaCl2溶液通入CO2气体至饱和,溶液中有无CaCO3沉淀?
- Ksp[Mg(OH)2]=5.61×10-12,Mg(OH)2 饱和溶液中[OH-]等于
- Ksp(PbI2) = 7.1×10-9,Ksp(Mn(OH)2) =2.06×10-13,Ksp[Pb(OH)2] = 1.2×10-15,Ksp(Mg(OH)2) = 5.61×10-12,根据溶度积常数中判断,在水中溶解度最大的是
- 若某人血液的pH=6.8,试判断他是
- 将缓冲溶液稀释后,缓冲容量不变 。
- 弱碱B-的解离常数pKb=6,由相同浓度的HB和B-组成的缓冲溶液,其pH是
- NH3·H2O(pKb=4.75)与其盐NH4Cl组成的缓冲溶液的缓冲范围是
- 用H3PO4 和NaOH配制pH=7.0的缓冲溶液,抗碱成分是
- 计算多元酸溶液的pH时,若Ka1/Ka2>100,可按一元酸处理
- 起始浓度不会影响两性物质溶液的pH值。
- 缓冲溶液是能够抵抗少量的强酸、强碱或有限的稀释而维持溶液pH不变的溶液。
- 对于缓冲溶液被稀释后,溶液的pH基本不变
- Cl-属于
- 渗透现象能减小半透膜两侧溶液的浓度差。
- 反渗透可以实现溶液的浓缩和海水的淡化。
- 医学上的等渗溶液,其渗透浓度为
- 下列几组用半透膜隔开的溶液,在相同温度下水从右向左渗透的是
- 用理想半透膜将0.02 mol·L-1 蔗糖溶液和0.02 mol·L-1 NaCl溶液隔开时,在相同温度下将会发生的现象是
- 与难挥发性非电解质稀溶液的渗透压有关的因素为
- 会使红细胞皱缩的是
- 红细胞置于其中会发生溶血的是
- 欲较精确地测定某蛋白质的相对分子质量,最合适的测定方法是
- 为阻止半透膜隔开的两种不同浓度的溶液间发生渗透现象,应在浓溶液液面上施加一额外压力,该压力是
- 以任意体积比混合生理盐水和50g·L-1葡萄糖溶液,红细胞置于其中将
答案:错
答案:错
答案:错
答案:错
答案:对
答案:对
答案:错
答案:对
答案:错
答案:错
答案:HF和H2O
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!