第四章 化学平衡:第四章,讲解化学反应中的化学平衡。4.1标准平衡常数:化学平衡的基本特征[单选题]
4.2标准平衡常数表达式及其应用:标准平衡常数表达式,多重平衡原理,判断反应进行的程度和判断化学反应的方向
4.3化学平衡的移动:浓度、温度、压强对平衡的移动
4.4自发变化和熵:自发变化、焓和自发变化
4.5Gibbs函数:Gibbs函数[变]判据、反应方向转变温度的估算
4.6例题讲解1:标准平衡常数的实验测定
4.7例题讲解2:计算平衡组成
4.8例题讲解3:浓度对化学平衡的影响
4.9例题讲解4:压强对化学平衡的影响
4.10例题讲解5:化学反应熵变的计算
4.1标准平衡常数:化学平衡的基本特征
4.2标准平衡常数表达式及其应用:标准平衡常数表达式,多重平衡原理,判断反应进行的程度和判断化学反应的方向
4.3化学平衡的移动:浓度、温度、压强对平衡的移动
4.4自发变化和熵:自发变化、焓和自发变化
4.5Gibbs函数:Gibbs函数[变]判据、反应方向转变温度的估算
4.6例题讲解1:标准平衡常数的实验测定
4.7例题讲解2:计算平衡组成
4.8例题讲解3:浓度对化学平衡的影响
4.9例题讲解4:压强对化学平衡的影响
4.10例题讲解5:化学反应熵变的计算
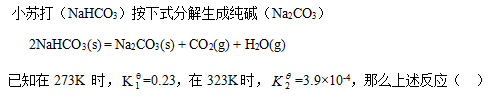 选项:[
选项:[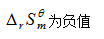 ,
, 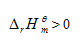 ,
, 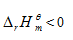 ,
, 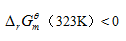 ]
] [判断题]体系中的自发过程必然是一个熵增的过程。
选项:[对, 错]
[单选题]熵减小的反应(或过程)是( )
选项:[固态I2的升华, CuSO4·5H2O晶体溶于水, NaCl晶体从溶液中析出,
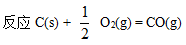 ]
][单选题]
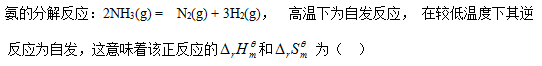 选项:[
选项:[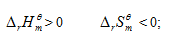 ,
, 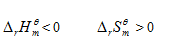 ,
, 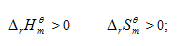 ,
, 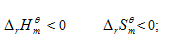 ]
][单选题]
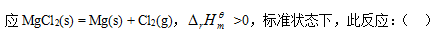 选项:[任何温度均不可能自发, 高温自发, 任何温度均自发, 低温自发]
选项:[任何温度均不可能自发, 高温自发, 任何温度均自发, 低温自发][判断题]298 K时查得C (金刚石)的绝对熵为2.43 J·mol-1·K-1 ,则C (石墨)的绝对熵为零。
选项:[对, 错]
[判断题]某化学反应在任何温度下都不能正向进行,则该反应的Δ H < 0 ,Δ S > 0 。
选项:[对, 错]
[单选题]
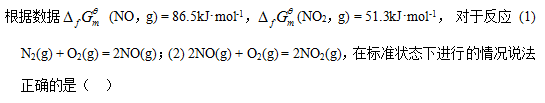 选项:[(1)能自发(2)不能, (1)和(2)都能自发, (2)能自发(1)不能, (1)和(2)都不能自发]
选项:[(1)能自发(2)不能, (1)和(2)都能自发, (2)能自发(1)不能, (1)和(2)都不能自发][单选题]
在298.15K和标准态时,下列反应均为非自发反应,其中在高温下仍为非自发反应的是( )
选项:[
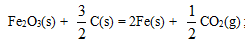 , 6C(s) + 6H2O(g) = C6H12O6(s)答案:D 难度:4
, 6C(s) + 6H2O(g) = C6H12O6(s)答案:D 难度:4, N2O4(g) = 2NO2(g)
,
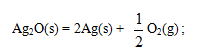 ]
][单选题]熵减小的反应(或过程)是( )
选项:[固态I2的升华, CuSO4·5H2O晶体溶于水, NaCl晶体从溶液中析出,
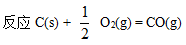 ]
][单选题]
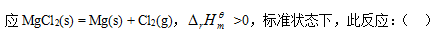 选项:[任何温度均自发, 高温自发, 低温自发, 任何温度均不可能自发]
选项:[任何温度均自发, 高温自发, 低温自发, 任何温度均不可能自发][单选题]
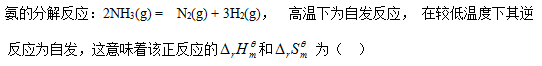 选项:[
选项:[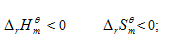 ,
, 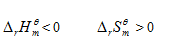 ,
, 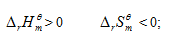 ,
, 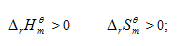 ]
][单选题]
在298.15K和标准态时,下列反应均为非自发反应,其中在高温下仍为非自发反应的是( )
选项:[
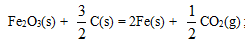 , 6C(s) + 6H2O(g) = C6H12O6(s)答案:D 难度:4
, 6C(s) + 6H2O(g) = C6H12O6(s)答案:D 难度:4,
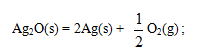 , N2O4(g) = 2NO2(g)
, N2O4(g) = 2NO2(g)]
[单选题]
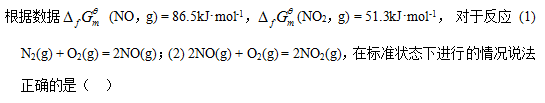 选项:[(1)能自发(2)不能, (1)和(2)都不能自发, (2)能自发(1)不能, (1)和(2)都能自发]
选项:[(1)能自发(2)不能, (1)和(2)都不能自发, (2)能自发(1)不能, (1)和(2)都能自发][单选题]
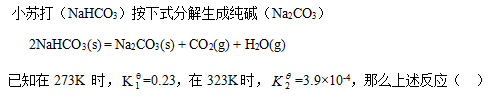 选项:[
选项:[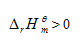 ,
, 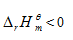 ,
, 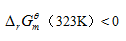 ,
, 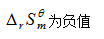 ]
][判断题]体系中的自发过程必然是一个熵增的过程。
选项:[对, 错]
[判断题]298 K时查得C (金刚石)的绝对熵为2.43 J·mol-1·K-1 ,则C (石墨)的绝对熵为零。
选项:[对, 错]
[判断题]某化学反应在任何温度下都不能正向进行,则该反应的Δ H < 0 ,Δ S > 0 。
选项:[对, 错]
温馨提示支付 ¥1.00 元后可查看付费内容,请先翻页预览!