第二章单元测试
- 进行氢氧化物沉淀时,为什么不能完全根据氢氧化物的Ksp来选择和控制溶液的pH值。
- 试比较无机沉淀剂分离与有机沉淀剂分离的优缺点,并举例说明。
- 试分别说明无机共沉淀剂和有机共沉淀剂的作用原理,并比较它们的优缺点。
- 今欲分离低碳钢中微量的镍应选择那种沉淀分离法?
- 已知FeS的Ksp=6.3×10-18,ZnS的Ksp=1.6×10-24,为了使它们完全分离,从理论上讲,溶液中的[S2+]和[H+]分别应控制在什么范围?可用什么缓冲溶液。假定
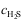 =[H2S]=0.1 molL-1,
=[H2S]=0.1 molL-1, 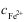 =0.1 molL-1。
=0.1 molL-1。 - 沉淀的溶解度因其共同离子的一种过量存在而增大的现象,叫做同离子效应。( )
- 当溶液中有与构成沉淀的离子不同的离子存在时,沉淀的溶解度增大,这种现象叫做盐效应。( )
- 氢氧化物沉淀大多为胶状沉淀,吸附力强,沉淀表面能吸附其它离子,因此分离效果很不理想。( )
- [S2-]和溶液中的pH值没有关系,改变溶液的pH值,必要可以改变[S2-]( )
答案:因为氢氧化物的沉淀不仅受到溶度积常数(Ksp)的影响,还受到溶液中其他离子存在的影响,如共同离子效应、配合效应等,这些因素会改变沉淀的实际溶解度,从而影响沉淀的完全程度。此外,pH值的控制还需要考虑其他弱酸根离子或弱碱阳离子可能的水解行为,以及过高的pH值可能导致的副反应或对设备的腐蚀问题。因此,不能仅依据氢氧化物的Ksp来选择和控制溶液的pH值。
答案:0
答案:无机共沉淀剂作用原理:无机共沉淀剂通过与待测组分形成难溶化合物或者通过吸附、包藏作用,使目标离子在主沉淀中共同沉淀下来,从而达到分离富集的目的。这类共沉淀剂主要包括氢氧化物、硫化物、磷酸盐等无机盐类。 有机共沉淀剂作用原理:有机共沉淀剂主要是高分子物质,如树脂、多糖、表面活性剂等。它们通过高分子链的缠绕、包裹以及静电吸附等作用,与目标离子结合形成复合物,一同沉淀出来。有机共沉淀剂能够提供更多的表面吸附位点,提高沉淀的选择性和回收率。 优点比较: - **无机共沉淀剂**:操作简单、成本低廉、适用范围广;可以实现对多种金属离子的同时沉淀。 - **有机共沉淀剂**:选择性高、可提高沉淀的完整性,减少目标组分的损失;能够有效去除干扰杂质,提高分析精度。 缺点比较: - **无机共沉淀剂**:选择性相对较低,可能共沉淀较多杂质;对低浓度样品的富集效果有限。 - **有机共沉淀剂**:成本较高,操作复杂;需要考虑有机物可能对后续分析步骤(如光谱分析)的影响。 综上,无机共沉淀剂和有机共沉淀剂各有优势,选择时需根据具体分析要求、目标物特性及实验室条件来决定。
答案:丁二酮肟沉淀法。
答案:无
A:错 B:对
答案:错
A:对 B:错
答案:对
A:对 B:错
答案:对
A:对 B:错
答案:错
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!
