第六章单元测试
- 标准电极电势表中的Eθ值是以氢电极作参比电极而测得的电势值。( )
- 电对的E和Eθ的值的大小都与电极反应式的写法无关。( )
- 对于电池反应Cu2+ + Zn = Cu + Zn2+,增加系统Cu2+ 的浓度必将使电池的电动势增大,根据电动势与平衡常数的关系可知,电池反应的
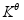 也必将增大。( )
也必将增大。( ) - 溶液中同时存在几种氧化剂,若它们都能被某一还原剂还原,一般说来,电极电势差值越大的氧化剂与还原剂之间越先反应,反应也进行得越完全。( )
- 反应Cr2O72-+ SO32-→ Cr3+ + SO42-在酸性介质中进行,反应式配平后。H2O的化学计量数的绝对值是( )
- 将反应Fe2+ + Ag+→Fe3+ + Ag构成原电池,其电池符号为( )
- 由镉电极浸在0.0100 mol·L-1镉离子溶液中所组成的半电池的电极电势是多少?已知:Eθ(Cd²+/Cd)=-0.403V( )
- 在酸性介质中,用KMnO4溶液滴定草酸盐,滴定应( )
- 称取0.5007g石灰石试样,将钙沉淀为CaC2O4,过滤、洗涤后,将沉淀溶解于硫酸中,以c(
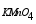 )=0.04408mol·L-1KMnO4溶液滴定至终点,消耗23.09mL,试样中CaCO3的质量分数为多少?(CaCO3的式量为100.0)( )
)=0.04408mol·L-1KMnO4溶液滴定至终点,消耗23.09mL,试样中CaCO3的质量分数为多少?(CaCO3的式量为100.0)( ) 已知Eθ(Ni2+/Ni)=-0.257V,测得某电极的E(Ni2+/Ni)=-0.21V,说明在该系统中必有( )
A:对 B:错
答案:错
A:对 B:错
A:对 B:错
A:对 B:错
A:4 B:8 C:2 D:1
A:(-)Pt∣Fe2+∣Fe3+‖Ag+∣Ag(+) B:(-)Pt∣Fe2+,Fe3+‖Ag+∣Ag∣Pt(+) C:(-)Pt∣Fe2+.Fe3+‖Ag+∣Ag(+) D:(-)Fe2+∣Fe3+‖Ag+∣Ag(+)
A:-0.344V B:-0.152V C:-0.285V D:-0.462V
A:在开始时缓慢进行,以后逐渐加快 B:始终缓慢地进行 C:开始时快,然后缓慢 D:象酸碱滴定那样快速进行
A:0.2247 B:0.2033 C:0.1016 D:0.5082
A:c(Ni2+)<1 mol·L-1 B:c(Ni2+)=1 mol·L-1 C:无法确定 D:c(Ni2+)>1 mol·L-1
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!