提示:内容已经过期谨慎付费,点击上方查看最新答案
分析化学(天津大学)
0.00200 mol·L-1K2Cr2O7溶液对Fe2O3(MFe2o3=159.7 g·mol-1)的滴定度(单位:mg/mL)为:
- HPO42-的共轭碱是:
当两电对的电子转移数均为2时,为使反应完全度达到99.9%,两电对的条件电位差至少应大于:
- 用佛尔哈德法测定Cl-时,未加硝基苯保护沉淀,分析结果会:
- 为标定HCl溶液可以选择的基准物是:
在络合滴定中,用回滴法测定Al3+时,若在pH=5~6时以某金属离子标准溶液回滴过量的EDTA,金属离子标准溶液应选( )
- 在用K2Cr2O7测定铁的过程中,采用二苯胺磺酸钠做指示剂(EθIn=0.86V),如果用K2Cr2O7标准溶液滴定前,没有加入H3PO4,则测定结果:
用EDTA滴定Bi3+时,消除Fe3+干扰宜采用( )
已知H3PO4的pKa1=2.12,pKa2=7.20,pKa3=12.36,调节磷酸盐溶液的pH值为6.0时,其各有关存在形式浓度间的关系是:
- 有四个学生从滴定管读同一体积( 单位:mL ) , 得到下面四个数据,正确的是:
以0.20 mol·L-1NaOH溶液滴定0.20 mol·L-1两性物质HA-(pKa1=3,pKa2=6)。化学计量点时的pH值为:
- 在下列四种表述中说明随机误差小的是:
(1)空白试验的结果可忽略不计
(2)用标准试样做对照试验,结果没有显著差异
(3)平行测定的标准偏差小
(4)几次测定的结果都十分接近 - 标定盐酸溶液常用的基准物有:
- 用KMnO4测定铁时,若在HCl介质中,其结果将:
Ag2CrO4在0.0010 mol∙L-1AgNO3溶液中的溶解度较在0.0010 mol∙L-1K2CrO4中的溶解度(已知
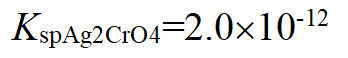 ):
):- 有一组平行测定所得的数据,要判断其中是否有可疑值,应采用:
- 用碘量法测定CuSO4中的Cu2+含量时,加入KSCN的作用是:
- 在K2Cr2O7定铁试验中钨酸钠用作:
- 将置于普通干燥器中保存的Na2B4O7·10H2O作为基准物质用于标定盐酸的浓度,则盐酸的浓度将:
下列各种弱酸、弱碱,能用酸碱滴定法直接滴定的是:
- 测定溶液中的SO42-,Fe3+中的SO42-时,欲使Fe3+以Fe(OH)3形式除去,则溶液酸度应控制在:
- Ca2+既无氧化性,又无还原性,用KMnO4法测定时,只能采用:
- 配制以下标准溶液必须用间接法配制的是:
- 以下银量法测定需采用返滴定方式的是:
- 用铁铵矾指示剂法测定下列离子时,会发生沉淀的转化而引起滴定误差的是:
- 在碘量法测铜的反应中,KI是作为:
用克氏定氮法测定一有机物中氮(MN=14.01 g·mol-1)的含量时,称取试样1.000 g,用50.00 mL0.4000 mol·L-1HCl吸收氨,过量的酸用0.2000 mol·L-1NaOH标准溶液回滴,用去10.00 mL。则该试样中氨的含量为:
已知某二元弱酸H2A的Ka1=10-3,Ka2=10-7。则NaHA稀溶液的pH值约为:
H3PO4的离解常数pKa1=2.12,pKa2=7.00,pKa3=12.36。由其分布曲线可知,pH=8.0的0.1 mol·L-1H3PO4溶液中各种存在形式平衡浓度之间的关系是:
- 对于n1=n2=1型的可逆对称氧化还原反应,如使反应能用于滴定分析,两个电对的条件电极电位差必须大于:
- 下列要求中属于重量分析对称量形式的要求的是( )
用
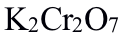 法测定
法测定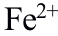 ,加入
,加入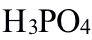 的主要目的是( )。
的主要目的是( )。- 下列物质不能用直接法配制标准溶液的是:
- 以下各种措施中,可以消除分析测试中的系统误差的是( )
下列叙述中正确的是( )。
碘量法的误差主要来源是( )。
- 下列仪器需要用所装溶液润洗三次的是( )。
统计学中对可疑值的取舍有( )方法。
以下说法中,叙述中正确的是( )
- 在一般情况下,碘量法的主要误差来源是:
- 有两组分析数据,要比较它们的测量精密度有无显著性差异,应当用Q检验法。( )
高锰酸钾法通常在强酸性溶液如
 溶液中进行。( )
溶液中进行。( )- 酸碱滴定中有时需要用颜色变化明显的变色范围较窄的指示剂即混合指示剂。( )
- 在写醋酸铵水溶液的质子平衡式时,应取铵根离子和醋酸根离子为零水准。( )
- 只要能够形成络合物,都适用于络合滴定法。( )
用
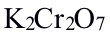 法测定
法测定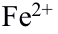 ,加入
,加入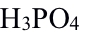 的一个作用是增加
的一个作用是增加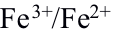 的电极电势数值,增大突跃范围。( )
的电极电势数值,增大突跃范围。( )- 在配位滴定法中,pH值越大,酸效应系数越大。( )
- 精密度是指测定值与真实值之间的符合程度。( )
- 滴定分析中,指示剂颜色突变时停止滴定,这一点称为化学计量点。( )
在EDTA滴定中,当
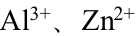 离子共存时,可用
离子共存时,可用 掩蔽
掩蔽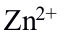 而测定
而测定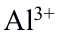 。( )
。( )
A:0.3200 B:9.582 C:1.600 D:0.9582
答案:96
A:H3PO4 B:PO43- C:OH- D:H2PO4-
答案:PO43-
A:0.36V B:0.09V C:0.27V D:0.18V
答案:0.18V
A:偏高 B:偏低 C:可能大可能小 D:无影响
答案:偏低
A:NaOH B:Na2S2O3 C:Na2SO3 D:Na2CO3
答案:Na2CO3
A:Mg2+ B:Bi3+ C:Zn2+ D:Ag+
A:偏高 B:正确 C:偏低 D:时高时低
A:加抗坏血酸 B:加NaOH C:加氰化钾 D:加三乙醇胺
A:[H3PO4]>[H2PO4-]>[HPO42-] B:[HPO42-]>[PO43-]>[H2PO4-] C:[HPO42-]>[H2PO4-]>[PO43-] D:[H2PO4-]>[HPO42-]>[H3PO4]
A:25.10 B:25.100 C:25.1 D:25
AI参考:正确答案是B:25.100。根据题目描述,四个学生从滴定管读同一体积,单位为mL,因此选项中需要包含小数点后两位,只有B选项符合要求。A、C、D选项都只包含整数部分或小数点前一位,不符合题目要求。因此,正确答案是B:25.100。'
A:4.5 B:8.5 C:5.5 D:9.5
AI参考:正确答案是【B】。化学计量点时为强碱滴定强酸溶液,离子方程式为:C(H^{+})总=[OH-]C=10^(-14)/C(OH-),溶液中C(OH-)=0.20mol/L,C(H+)=10^(-14)/0.20mol/L=5×10^(-14)/0.2mol/L,所以溶液的pH值为8.5。故答案为B。'
A:3,4 B:1,2 C:2,4 D:1,3
A:无水Na2CO3 B:邻苯二甲酸氢钾 C:草酸(H2C2O4·2H2O) D:CaCO3
A:偏高 B:准确 C:难确定 D:偏低
A:可能大可能小 B:小 C:大 D:相等
A:F检验 B:t检验 C: u检验 D:Q检验
A:掩蔽其他可与I-发生反应的物质 B:形成CuSCN沉淀,使I-释放出来,以增加反应物的浓度 C:用作摧化剂,使产生I2的速度加快 D:因CuI沉淀强烈吸附I2,加入KSCN使CuI沉淀转化为CuSCN,将I2释放出来
AI参考:正确答案是D:因CuI沉淀强烈吸附I2,加入KSCN使CuI沉淀转化为CuSCN,将I2释放出来。用碘量法测定CuSO4中的Cu2+含量时,加入KSCN的作用是因为CuI沉淀强烈吸附I2,加入KSCN使CuI沉淀转化为CuSCN,将I2释放出来。这样既能减少误差,又能提高测定的准确性。其他选项A、B、C都与问题无关。'
A:指示剂 B:还原剂 C:氧化剂 D:催化剂
AI参考:正确答案是【B:还原剂】。钨酸钠在定铁试验中用作还原剂,可以将铁离子还原为亚铁离子,便于后续的滴定分析。因此,答案为B。'
A:不能确定 B:偏低 C:偏高 D:无影响
A:0.01mol·L-1CH2ClCOOH(Ka=1.4x10-3) B:0.1mol·L-1C6H5NH2(Kb=4.6x10-10) C:1mol·L-1H3BO3(Ka=5.7x10-10) D:0.1mol·L-1(CH2)6N4(Kb=1.4x10-9)
A:在中性溶液中 B:在强酸性溶液中 C:在弱碱性溶液中 D:在弱酸性溶液中
A:间接滴定法 B:置换滴定法 C:直接滴定法 D:返滴定法
A:NaCl B:NaOH C:Na2C2O4 D:Na2CO3
AI参考:正确答案是【C:Na2C2O4】。标准溶液的配制方法有直接配制法和间接配制法,其中间接配制法又分为标定法和直接称量法。Na2C2O4需要用草酸钠作为基准物质进行标定,所以需要用间接法配制。而NaCl、NaOH和Na2CO3可以直接称量或溶解配制,所以为直接配制法。故本题答案为C。'
A:莫尔法测Cl- B:佛尔哈德法测Cl- C:AgNO3滴定CN-(生成Ag[Ag(CN)2]指示终点 D:吸附指示剂法测Cl-
A:Cl- B:SCN- C:I- D:Br-
A:氧化剂 B:还原剂 C:缓冲物质 D:催化剂
AI参考:在碘量法测铜的反应中,KI是作为还原剂。在碘量法中,碘化物被氧化为碘单质,而碘单质可以被碘量计(一种能检测碘的仪器)直接测量。在这个过程中,KI作为还原剂被消耗,同时铜离子被氧化为铜单质。因此,答案为B:还原剂。'
A:25% B:31% C:30.65% D:25.22%
AI参考:正确答案是C:30.65%。根据题意,试样质量为1.000g,吸收氨后剩余盐酸的浓度为0.4000mol/L × 50.00mL - 0.2000mol/L × 10.00mL = 3.8mol/L,则吸收的氨的物质的量为:3.8mol/L × 1.0mL = 3.8 × 10^-3mol。根据氮元素守恒,氨的物质的量等于试样中氮的物质的量,即:n(NH3) = n(N) = 3.8 × 10^-3mol又因为氮的摩尔质量为14.01g/mol,所以氨的质量为:m(NH3) = 3.8 × 10^-3mol × 17g/mol = 6.4 × 10^-3g因此,该试样中氨的含量为:x = (6.4 × 10^-3g) / 1g × 100% = 6.4%选项C为30.65%,与计算结果最接近。'
A:6.0 B:2.0 C:4.0 D:5.0
AI参考:正确选项是【D:5.0】。根据题意,二元弱酸H2A的Ka1=10-3,Ka2=10-7。由于NaHA是强碱弱酸盐,所以会发生酸碱电离和水解,但是其水解程度很小。因此,其溶液中的主要成分是HA-离子,它的浓度可以通过NaHA的浓度乘以它的电离常数Ka2来得到。而HA-离子又会水解,其水解平衡常数Kh可以通过其电离常数Ka和离子浓度乘积c(HA-)*c(H+)的比值得到。由于Ka2远小于Ka1,所以可以忽略HA-的水解,溶液中的主要成分仍然是HA-离子。因此,溶液中的氢离子浓度可以通过Ka2乘以溶液中HA-的浓度得到,即氢离子浓度近似等于Ka2乘以c(HA-)的倒数。根据题意,已知NaHA的浓度为1mol/L,Ka2=10-7,所以溶液中的pH值约为5.0。因此,答案为D。'
A:[HPO42-]>[H2PO4-] B:[H2PO4-]>[HPO42-] C:[PO43-]>[HPO42-] D:[H3PO4]>[H2PO4-]
A:1.0V B:0.35V C:0.1V D:0.2V
A:表面积要大; B:相对摩尔质量要大; C:组成要与化学式完全符合; D:要稳定;
A:提高酸度,使滴定趋于完全 B:同形成稳定的无色化合物,减少黄色对终点的干扰 C:减少的电极电位数值,增大突跃范围 D:增加的电极电位数值,增大突跃范围
AI参考:正确答案是B:同形成稳定的无色化合物,减少黄色对终点的干扰。加入指示剂的主要目的是为了提高滴定终点颜色的敏锐度,即减少黄色对终点的干扰。选项A、C、D都与滴定终点颜色的敏锐度无关,因此不是加入指示剂的主要目的。而选项B描述的是加入稳定无色化合物,减少黄色对终点的干扰,这与加入指示剂的主要目的相符。因此,答案为B。'
A:K2Cr2O7 B:CeSO4·2(NH4)2SO4·2H2O C:Na2S2O3·5H2O D:KMnO4
A:进行空白试验 B:增加测定次数 C:进行仪器校正 D:进行对照试验
A:为五位有效数字 B:为三位有效数字 C:pH=6.70为两位有效数字 D:4.1251修约为三位有效数字为4.13
A:滴定时酸度要求太苛刻 B:的挥发性 C:容易被空气中氧所氧化 D:指示剂变色不明显
A:试剂瓶 B:移液管 C:滴定管 D:容量瓶
A:F检验法 B:4Ƌ法 C:格鲁布斯法 D:Q检验法
AI参考:正确答案是:B:4Ƌ法 C:格鲁布斯法。统计学中对可疑值的取舍有4Ƌ法、格鲁布斯法等方法。其中,4Ƌ法是利用四分位数的方法剔除可疑值,格鲁布斯法是利用样本统计量与临界值进行比较,从而确定可疑值是否应该剔除。因此,选项B和C是正确答案。F检验法和Q检验法主要用于方差分析等统计推断中,与可疑值的取舍无关。'
A:精密度好,准确度就好 B:精密度是保证准确度的前提 C:方法误差属于系统误差 D:系统误差影响分析结果精密度
AI参考:正确选项为:B:精密度是保证准确度的前提 C:方法误差属于系统误差解释:A选项不准确,精密度和准确度是两个相关的概念,它们之间有联系但不是等同的。B选项正确,精密度是测量结果可重复性的一个指标,它是在准确度的基础上提出的,是保证准确度的前提。C选项正确,方法误差属于系统误差,因为它是由方法本身的因素引起的,在一定条件下保持不变。D选项有一定关系,系统误差的存在会导致分析结果的精密度变差,但是并不是说精密度和准确度完全相同。所以B和C选项是正确的。'
A:滴定速度稍快 B:I2的挥发 C:淀粉溶液加入过早 D:在酸性溶液中I-被空气中O2氧化
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
AI参考:正确答案是B:错。本题所述前提不成立,只有符合一定条件的配合物才能被滴定。要能被滴定,需要配合物有适当的稳定性,并且要有比较高的滴定突跃范围。因此,不是所有能够形成络合物的都适用于络合滴定法。'
A:错 B:对
AI参考:这是一个关于图片的使用及其功能的判断题。根据题干描述,图片的作用是用来增加电极电势数值,进而增大突跃范围。但实际上,图片并不能直接改变电极电势数值,电极电势是由电极材料、电解质溶液和温度等因素共同决定的。因此,答案为A:“错”。'
A:错 B:对
A:对 B:错
A:错 B:对
A:对 B:错
AI参考:正确答案是B:错。在EDTA滴定中,离子共存时,不能使用掩蔽剂。掩蔽剂的作用是消除干扰离子对滴定的影响,而如果使用掩蔽剂,则无法准确测定目标离子。因此,本题中的说法是错误的。'

