曲阜师范大学
- 某电子处在3d 轨道,它的轨道量子数n为___________,l为____________,m可能是____________________,____,____,____。
- 波函数 是描述核外电子运动状态的数学函数式,它和____________是同义词。电子云是 ____________ 的形象化表示,____,____。
- 下列各组量子数中,合理的一组是( )
- 下列电对的电极电势与pH无关的是( )
- 不是共轭酸碱对的一组物质是( )
- 按分子轨道理论,最稳定的顺磁性粒子是( )
- 已知KbΘ (NH3) = 1.8×10−5,则其共轭酸的KaΘ为( )
- 下列两个反应在某温度、100 kPa时都能生成C6H6 (g):① 2C(石墨) + 3H2(g) → C6H6 (g)② C2H4 (g) + H2 (g) → C6H6 (g),则代表C6H6 (g)标准摩尔生成焓的反应是( )
- 下列反应中,r HmΘ与产物的f HmΘ相同的是( )
- 下列各对物质中,分子间作用力最弱的是( )
- 对下列配合物稳定性的判断,不正确的是( )
- BF3分子的偶极矩数值为( )
- 使下列电极反应中有关离子浓度减小一半,而E值增加的是( )
- 某金属离子生成的两种配合物的磁矩分别为4.90 μB和0,则该金属离子可能是( )
- 已知Zn + 2H+ (a mol·dm‒3) = Zn2+ (1.0 mol·dm‒3) + H2 (1.013×105 Pa),E (Zn2+/Zn) = ‒0.76 V,下列原电池反应的电动势为0.46 V,则氢电极溶液中的pH为( )
- 已知反应A2 (g) + 2B2 (g) = 3C2 (g)在恒压和温度1000 K时的r Hm为40 kJ∙mol−1,r Sm为40 J∙mol−1∙K−1,则下列关系中正确的是( )
- 合成氨的原料气中氢气和氮气的体积比为3:1,若原料气中含有其他杂质气体的体积分数为4%,原料气总压为15198.75 kPa,则氮气的分压为( )
- 实验测得H2的扩散速率是一未知气体扩散速率的2.9倍,则该未知气体的相对分子质量约为( )
- 下列分子和离子中,中心原子杂化轨道类型为sp3d,且构型为直线型的是( )
- 已知H3PO4的Ka1Θ = 6.9×10−3,Ka2Θ = 6.1×10−8,Ka3Θ = 4.8×10−13,则在0.1 mol·dm−3 NaH2PO4溶液中离子浓度由大到小的顺序正确的是( )
- 下列电对的电极电势与pH无关的是( )
- 下列分子中,中心原子采取等性杂化的是( )
- 根据Nernst方程式计算MnO4–/Mn2+ 的电极电势E时,下列叙述不正确的是( )
- 下列各对元素中,第一电子亲和能大小排列顺序正确的是( )
- 某电池(‒)A|A2+ (0.1 mol·dm‒3) || B2+ (1.0×10‒2 mol·dm‒3) |B(+)的电动势E为0.27 V,则该电池的标准电动势E为( )
- 已知:FeS的KspΘ = 6.3×10−18,CuS的KspΘ = 6.3×10−36,H2S的KΘ = 1.4×10−20。溶液中FeCl2和CuCl2的浓度均为0.10 mol·dm−3,向其中通入H2S气体至饱和,沉淀生成情况为( )
- 在K[Co(C2O4)2(en)]中,中心离子的配位数为( )
- 3s电子的径向分布图有( )
- 下列分子中含有不同长度共价键的是( )
- 298 K时,反应2N2 (g) + O2 (g) = 2N2O (g) 的r UmΘ为166.5 kJ∙mol−1,则该反应的r HmΘ为( )
- 在0.10 mol·dm−3氨水中加入等体积的0.10 mol·dm−3下列溶液后,使混合溶液的pH最大的是( )
- 反应2SO2 (g) + O2 (g) = 2SO3 (g) 达平衡时,保持体积不变,加入惰性气体He,使总压力增加一倍,则( )
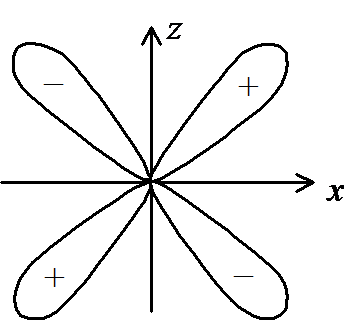 ,图中所示的原子轨道角度分布图是( )
,图中所示的原子轨道角度分布图是( ) - 若反应商等于1,下列关系正确的是( )
- 中心离子的3d电子排布为t2g3eg0的八面体配合物是( )
- 下列配合物中,肯定为无色的是( )
- 已知配合物的稳定常数K稳 [Fe(CN)63‒]>K稳 [Fe(CN)42‒],则下列描述正确的是( )
- 已知HClO:K = 3.4×10−8;H2CO3:K1 = 4.2×10−7,K2 = 5.6×10−11;H3PO4:K1 = 7.6×10−3,K2 = 6.3×10−8,K3 = 4.4 ×10−13。不能配制 pH = 7 左右的缓冲溶液的是( )
- 对于反应2Cl2 (g) + 2H2O (g) = 4HCl (g) + O2 (g) rHmΘ<0,将H2O (g),HCl (g),Cl2 (g),O2 (g) 混合并在反应达到平衡时,下列操作平衡不发生移动的是( )
- 在容器中加入相同物质的量的NO和Cl2,在一定温度下发生反应NO (g) + 1/2 Cl2 (g) = NOCl (g) 达平衡,此时对有关各物质的分压判断正确的是( )
- 难溶盐Ca3(PO4)2在a mol·dm−3 Na3PO4溶液中的溶解度s与溶度积KspΘ关系式中正确的是( )
- 下列物理量中,不属于体系的状态函数的是( )。
- 冰的熔化热为330.5 kJ∙mol−1,0 ºC时将1.0 g水凝结为冰时的ΔS为( )
- 已知电极反应ClO3- + 6H+ + 6e- = Cl- + 3H2O的ΔrGm⊙ = -839.6 kJ·mol‒1,则E⊙(ClO3-/Cl-) =( )
- Pb2+离子的价电子层结构是( )
- 下列物质中,f Hmθ不等于零的是( )。
- 下列说法中,正确的是( )
- 按原子半径由大到小排列,顺序正确的是( )
- 下列分子或离子中,不含有孤电子对的是( )
- 下列分子和离子中,中心原子的价层电子对几何构型为四面体,且分子空间构型为V形的是( )
答案:3, 2, 0, ±1, ±2
答案:波函数ψ 是描述核外电子运动状态的数学函数式,它和原子轨道是同义词。电子云是原子轨道的形象化表示,表示电子在核外空间出现的概率密度,表明电子在原子核外空间某区域出现的概率。
A:n = 3, l = 3, ml = +1, ms = −1/2
B:n = 4, l = 5, ml = −1, ms = +1/2
C:n = 3, l = 1, ml = +1, ms = +1/2
D:n = 4, l = 2, ml = +3, ms = −1/2
答案:n=3, l=1, m=+1, m s=+1/2
A:MnO4–/Mn2+
B:H2O2/H2O
C:S2O82–/SO42–
D:O2/H2O
答案:S2O82–/SO42–
A:HS−,S2−
B:H2O,OH−
C:NH3,NH2−
D:NaOH,Na+
答案:D: NaOH,Na+
A:O22+
B:O2−
C:O2
D:O2+
答案:A: O22+
A:5.6×10−10
B:1.8×10−9
C:5.6×10−5
D:1.8×10−10
答案:D: 1.8×10−10
A:反应①
B:反应②的逆反应
C:反应①的逆反应
D:反应②
答案:反应①
A:C (金刚石) = C (石墨)
B:H2 (g) + 1/2O2 (g) = H2O (g)
C:2H2 (g) + O2 (g) = 2H2O (l)
D:NO (g) + 1/2 O2 (g) = NO2 (g)
答案:H2 (g) + 1/2O2 (g) = H2O (g)
A:N2和O3
B:NH3和PH3
C:He和Ne
D:H2O和CO2
A:[HgCl4]2‒>[HgI4]2‒
B:[Fe(CN)6]3‒>[Fe(SCN)6]3‒
C:[Cu(NH3)4]2+>[Zn(NH3)4]2+
D:[AlF6]3‒>[AlBr6]3‒
A:0
B:1
C:2
D:0.5
A:Fe3+ + e‒ = Fe2+
B:Cu2+ + 2e‒ = Cu
C:2H+ + 2e‒ = H2
D:I2 + 2e‒ = 2I‒
A:Fe2+
B:Mn3+
C:Mn2+
D:Cr3+
A:10.2
B:2.5
C:5.1
D:3.0
A:r Gm = 0
B:所有关系都正确
C:r Um = r Hm
D:r Um = Tr Sm
A:3799.688 kPa
B:11399.06 kPa
C:10943.1 kPa
D:3647.7 kPa
A:2
B:16
C:4
D:8
A:ICl2-
B:IF3
C:SbF4-
D:ICl4-
A:Na+,H2PO4−,HPO42−,H3PO4,PO43−
B:Na+,H2PO4−,HPO42−,PO43−,H3PO4
C:Na+,HPO42−,H2PO4−,PO43−,H3PO4
D:Na+,HPO42−,H2PO4−,H3PO4,PO43−
A:MnO4‒/MnO42‒
B:H2O2/H2O
C:MnO2/Mn2+
D:IO3‒/I‒
A:CCl4
B:SF4
C:H2O
D:NCl3
A:H+ 浓度增大,则E增大
B:H+ 浓度的变化对E无影响
C:MnO4– 浓度增大,则E增大
D:Mn2+ 浓度增大,则E减小
A:Si<P
B:Cl>Br
C:O>S
D:F<C
A:0.33 V
B:0.24 V
C:0.27 V
D:0.30 V
A:只生成FeS沉淀,不生成CuS沉淀
B:先生成CuS沉淀,后生成FeS沉淀
C:只生成CuS沉淀,不生成FeS沉淀
D:先生成FeS沉淀,后生成CuS沉淀
A:6
B:3
C:5
D:4
A:3个峰
B:2个峰
C:1个峰
D:4个峰
A:SO3
B:KI3
C:NH3
D:SF4
A:146 kJ∙mol−1
B:328 kJ∙mol−1
C:164 kJ∙mol−1
D:82 kJ∙mol−1
A:HNO3
B:HCl
C:H2SO4
D:HAc
A:无法判断
B:平衡不发生移动
C:平衡向右移动
D:平衡向左移动
A:dx2-y2
B:dxy
C:dz2
D:dxz
A:∆rGm = ∆rGmΘ
B:∆rGm = 0
C:∆rHmΘ = T∆rSmΘ
D:∆rGmΘ = 0
A:[FeF6]3‒
B:[Cr(H2O)6]3+
C:[Co(CN)6]3‒
D:[Mn(H2O)6]2+
A:ScF3
B:MnF3
C:TiCl3
D:CrF3
A:E[ Fe(CN)63‒/ Fe(CN)42‒]>E( Fe3+/Fe2+)
B:E[ Fe(CN)63‒/ Fe(CN)42‒]<E( Fe3+/Fe2+)
C:E[ Fe(CN)63‒/ Fe(CN)42‒] = E( Fe3+/Fe2+)
D:无法判断
A:HClO–NaClO
B:NaHCO3–Na2CO3
C:NaH2PO4–Na2HPO4
D:H2CO3–NaHCO3
A:降低体系温度
B:加入氧气
C:增加容器体积
D:加入催化剂
A:p(NO) = p(NOCl)
B:p(NO) > p(Cl2)
C:p(NO) < p(Cl2)
D:p(NO) = p(Cl2)
A:KspΘ = s3·(s + a)2
B:KspΘ = (3s)3·(2s + a)2
C:KspΘ = s5
D:KspΘ = 108 s5
A:功W
B:焓H
C:热力学能U
D:压强p
A:1.21 J∙K−1
B:-330.5 J∙K−1
C:-1.21 J∙K−1
D:0
A:1.45 V
B:0.026 V
C:0.052 V
D:-1.45 V
A:6s26p2
B:5s25p2
C:6s2
D:5s25p65d106s2
A:C (石墨)
B:Cl2 (l)
C:Ne (g)
D:Fe (s)
A:水蒸气的生成热即是氢气的燃烧热
B:水的生成热即是氢气的燃烧热
C:水的生成热即是氧气的燃烧热
D:水蒸气的生成热即是氧气的燃烧热
A:Si Mg B
B:Mg Si B
C:B Si Mg
D:Mg B Si
A:H2O
B:H3O+
C:NH4+
D:NH3
A:HgCl2
B:SO2
C:OF2
D:CO2
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!