第六章单元测试
- 下列沉淀反应,不属于银量法的是( )。
- 沉淀溶解度的含义是( )。
- 能够提高沉淀溶解度的因素有( )。
- 均相沉淀法能够制备出颗粒大、杂质少的晶形沉淀,主要是因为( )。
- 将CaC2O4沉淀置于0.010 mol
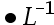 盐酸中,沉淀溶解时酸效应会( )。
盐酸中,沉淀溶解时酸效应会( )。 - 将MgNH4PO4置于蒸馏水,溶解平衡后[H+]=2.0
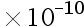 mol
mol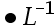 ,[Mg2+]=5.6
,[Mg2+]=5.6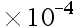 mol
mol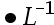 。已知NH3:Kb = 1.8
。已知NH3:Kb = 1.8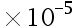 ;H3PO4:K1 = 7.6
;H3PO4:K1 = 7.6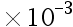 ,K2 = 6.3
,K2 = 6.3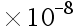 ,K3 = 4.4
,K3 = 4.4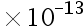 ,那么MgNH4PO4的溶度积常数等于( )。
,那么MgNH4PO4的溶度积常数等于( )。 - 将CaC2O4置于pH = 3.00的盐酸中,假设溶液原有H+浓度不受
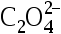 水解的影响,保持不变。已知CaC2O4:Ksp = 2.3
水解的影响,保持不变。已知CaC2O4:Ksp = 2.3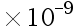 ;H2C2O4:K1 = 5.9
;H2C2O4:K1 = 5.9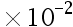 ,K2 = 6.4
,K2 = 6.4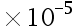 ,那么溶解度等于( )。
,那么溶解度等于( )。
A:
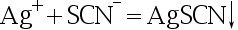
B:
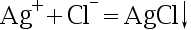
C:
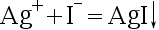
D:
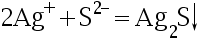
答案:
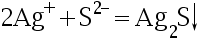
A:溶液中构晶阳离子和构晶阴离子的浓度之和
B:溶液中构晶阳离子的浓度
C:1 L溶液中沉淀分子从固相到液相的转移量
D:溶液中构晶阴离子的浓度
A:盐效应
B:酸效应
C:配位效应
D:同离子效应
A:增强了均相成核作用
B:快速沉淀
C:有效克服沉淀剂局部过浓问题
D:陈化作用
A:无法确定
B:不变
C:逐渐减弱
D:逐渐增强
A:1.8
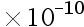
B:1.0
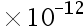
C:2.0
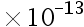
D:1.0
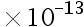
A:2.0
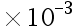 mol
mol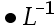
B:1.0
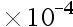 mol
mol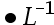
C:1.8
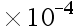 mol
mol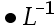
D:2.0
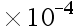 mol
mol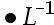
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!

