西安交通大学
- 熵增加的过程一定是自发过程。
- 主量子数n = 4的电子层,轨道总数为16,元素周期表中第四周期有16个元素。
- 熵增大于零的过程,一定是自发过程。( )
- 某反应的速率常数k =5.07×10-3 d -1,反应物转化90 %时所需的时间应为454.2 d 。( )
- 化学吸附多为单分子层吸附。( )
- 一定温度下的AgCl水溶液,其Ag+与Cl-离子浓度的乘积是一常数。
- 液体在固体表面上的吸附可分为分子吸附和离子吸附。( )
- 双分子反应一定是二级反应。( )
- 正、负吸附现象是矛盾的对立统一,负吸附就是解吸。( )
- 最外层电子构型为ns1~2的元素都在s区。

- 磁量子数m决定原子轨道在空间的取向。
- 主量子数n = 1时,有自旋方向相反的两个轨道。
- 蛋白质是两性聚电解质,其分子的带电符号与溶液的pH有关。( )
- 催化剂在反应前后所有性质都不改变。
- 双分子反应一定是基元反应。
- 不可逆过程就是过程发生后,系统不能再复原的过程。
- 氢原子1s电子云图中,小黑点越密的位置,电子出现的概率越大。
- 主量子数n = 4时,有4s、4p、4d、4f四条能量不同的轨道。
- 一个化学反应的级数越大,其反应速率也越大。
- 根据热力学知识,下列定义中不正确的是( )
体系在某一过程中,吸收的热
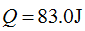 ,对外做功
,对外做功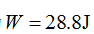 ,则环境的热力学能的变化
,则环境的热力学能的变化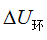 为 ( )
为 ( )- 若某反应的活化能为80KJ/mol,则反应温度由20℃增加到100℃时,其反应速率常数约为原来的 ( )
- 下列说法中,正确的是 ( )
- BaSO4在下列溶液中溶解度最大的是 ( )
- 一级反应的半衰期与反应物的初始浓度( )
- 某+2价离子的电子排布式为[Ar]3d5,该元素在周期表中属于( )
- 零级反应的半衰期公式是( )
- 基态19K原子最外层电子的四个量子数应是( )
- 氢原子的1s电子激发到4s或4p轨道时所需要的能量分别为E4s和E4p,它们的关系为( )
- 如果一个反应的吉布斯自由能变为零,则反应( )
- 体系对环境作20 kJ的功,并失去10 kJ的热给环境,则体系内能的变化是( )
- 已知反应A(g)=B(g)+C(g)是一级反应,在1×105 kPa下,A分解三分之一需60秒;在相同温度下,体系增压到2 ×105 kPa, A分解三分之一需 ( )
- 某反应,以log(-dc/dt)对logc作图得直线,如果该反应为二级,则直线的( )
- 多孔硅胶有强烈的吸水性能,硅胶吸水后其表面自由能将 ( )
- 将固体NH4NO3溶于水中,溶液变冷,则该过程的△G、△H、△S的符号依次是( )
- 下列原子中半径最大的是( )
- 在[I-] = 0.1 mol·L-1的溶液中,PbI2的溶解度(S)可表示为 ( )
- 增大反应物浓度,使反应速率增大的原因是 ( )
- 溶胶的光学性质是其高度分散性和不均匀性的反映,丁铎尔效应是最显著的表现,在下列光学现象中,它指的是( )
- 零级反应的速率( )
- 某反应在标准态和等温等压条件下,在任何温度都能自发进行的条件是( )
- 电子构型为[Ar]3d5可以表示 ( )
- 表面活性物质是 ( )
- 谋反应2A+B®C,实验测得其速率方程为v=kcAcB,由此可见该反应为( )
- 萘燃烧的化学反应方程式为:C10H8(s)+12O2(g)=10CO2(g)+4H2O(l),则在298K时,Qp与QV的差值(kJ·mol-1)是( )
- 关于溶液表面吸附的说法中正确的是( )
- 下列轨道中哪个是不合理的 ( )
- 物理吸附的作用力是( )
- CaF2饱和溶液的浓度为2´10-4 mol/L,则CaF2的溶度积为( )
- 在多电子原子中,决定电子能量的量子数为( )
- 升高温度使反应速度加快的主要原因是( )

A:对 B:错
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:对
A:对 B:错
答案:对
A:对 B:错
答案:B: 错 (但是,根据题目要求,您只需要给出答案,所以:A: 对) (原因是,对于一定温度下的AgCl水溶液,其Ag+与Cl-离子浓度的乘积确实是该温度下的溶度积常数Ksp,这是一个常数。) 请忽略解释部分,仅给出答案是题目要求的内容。
A:错 B:对
答案:对
A:错 B:对
答案:对
A:对 B:错
答案:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:
 B:
B: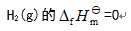 C:
C: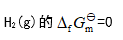 D:
D: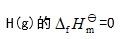
A:111.8J B: -111.8J C:-54.2J D:54.2J
A:2倍 B:5倍 C:4倍 D:3倍
A: 二级反应既是双分子反应 B: 反应级数随温度升高而增大 C: 反应级数只能由实验确定 D: 反应级数必是正整数
A:2 mol·L-1BaCl2 B:纯水 C:1 mol·L-1 NaCl D:1 mol·L-1 H2SO4
A:平方根呈正比 B:无关 C:呈反比 D:呈正比
A:ⅡB族 B:ⅡA族 C:VB族 D:ⅦB族
A:
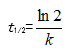 B:
B: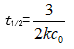 C:
C: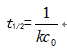 D:
D: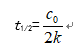
A:
选项D
B:选项B C:选项A D:选项C
A:
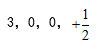 B:
B: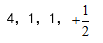 C:
C: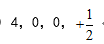 D:
D: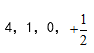
A: 选项D B: 选项B C: 选项A D: 选项C
A: E4s = E4p B:无法确定 C: E4s < E4p D: E4s > E4p
A:是吸热反应 B:处于平衡状态 C:是放热反应 D:能自发进行
A:30 kJ B:-30 kJ C:-10 kJ D:10 kJ
A:120秒 B:60秒 C:240秒 D:90秒
A:斜率=2 B:截距=2 C:截距/斜率=2 D:截距=0.3010
A:无法比较 B:不变 C:升高 D:降低
A:-,+,+ B:+,-,- C:-,+,- D:+,+,-
A: P B:Ca C: Mg D: As
A:
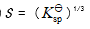 B:
B: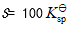 C:
C: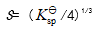 D:
D: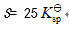
A:活化分子分数增加 B:单位体积的分子数增加 C:单位体积内活化分子总数增加 D:反应体系混乱度增加
A:散射 B:反射 C:透射 D:折射
A:与反应物浓度成反比 B:与反应物浓度无关 C:为零 D:与反应物浓度成正比
A:
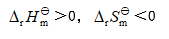 B:
B: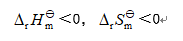 C:
C: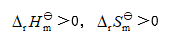 D:
D: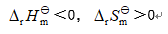
A:Fe2+ B: Mn2+ C:Ni2+ D: Co3+
A:能显著降低溶液表面张力的物质 B:能降低体系热力学能的物质 C:易溶于水的物质 D:能形成负吸附的物质
A:双分子反应,三级反应 B:三分子反应也是三级反应 C:一级反应 D:二级反应
A:2.48 B:4.95 C:-2.48 D:-4.95
A:定温下,表面张力不随浓度变化时,浓度增大,吸附量不变 B:饱和溶液的表面不会发生吸附现象 C:溶液的表面张力一定小于溶剂的表面张力 D:溶液表面发生吸附后表面吉布斯能增加
A:3f B:4p C:6d D:8s
A: 范德华力 B: 静电吸引力 C: 共价键力 D: 氢键力
A:3.2´10-11 B:8´10-4 C:4´10-4 D: 8´10-8
A:n和l B:l C:n, l, m D:n
A:活化能降低 B:活化分子百分数增加 C:碰撞频率增加 D:活化能升高
A:
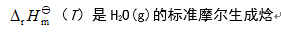 B:
B: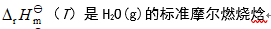 C:
C: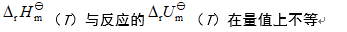 D:
D: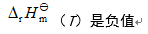
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!







