广州大学
- 建立化学平衡的条件是:在恒温条件下,封闭体系进行的可逆反应。
- 根据稀释定律,醋酸溶液被水稀释后,其离解度α增大,酸度也增大。
- 一个反应达到平衡的热力学特征是反应的∆G为0。
一个反应达到平衡的标志是
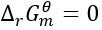
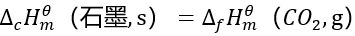
某化学反应的
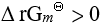 ,则该反应是不能发生的。
,则该反应是不能发生的。- 在反应体系中加入催化剂,不能改变反应的Δ H、ΔS、ΔG、ΔU。
- 恒温下,一个气相化学反应的总压强增大,其反应速率随之增大。
- 由化学反应等温式可以判断,反应商Q大于平衡常数K时,反应可正向进行。
- OF2分子空间构型为 “V” 字形,因此它是一个极性分子。
- 不会影响反应速率常数 k 的因素是
用能斯特公式计算电对
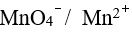 的非标准电极电势
的非标准电极电势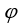 时,下列叙述中不正确的是
时,下列叙述中不正确的是 - 某氢电极与饱和甘汞电极( =+0.240 v)组成原电池 ,若要使电池电动势达到+0.299 v ,则溶液的 pH值是
- 下列关于速率常数k的说法中,不正确的是
标准Cu-Zn原电池的电动势=1.10 v ,如在铜半电池中加入少量固体
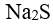 ,该原电池的电动势将
,该原电池的电动势将已知:
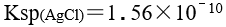 ,
,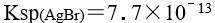 ,
,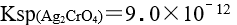 ,某溶液中含有 KCl ,KBr 和
,某溶液中含有 KCl ,KBr 和 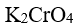 ,它们的浓度均为 ,向该溶液中逐滴加入
,它们的浓度均为 ,向该溶液中逐滴加入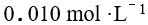 的
的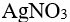 溶液时,最先沉淀和最后沉淀的是
溶液时,最先沉淀和最后沉淀的是某物质 B 的标准摩尔燃烧焓为
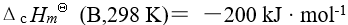 则该物质B 燃烧时的标准摩尔反应焓为( )
则该物质B 燃烧时的标准摩尔反应焓为( )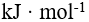
- 根据酸碱质子理论,下列各离子中,既可做酸,又可做碱的是
- 下列化合物中,键角最大的是
- 某反应在标准状态和等温等压条件下,在任何温度都能自发进行的条件是
- 在300 K时鲜牛奶大约 4 小时变酸,但在 277 K的温度下可保持 48 小时,则牛奶变酸的反应活化能(kJ·mol-1)是
- 对一定量的混合气体,下列说法中正确的是
- https://image.zhihuishu.com/zhs/teacherExam_h5/COMMONUEDITOR/202109/a0babc709c9e42d59ca2276b07a75b44.png
由反应式
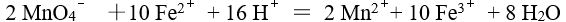 ,安排为电池 ,该电池的符号应是
,安排为电池 ,该电池的符号应是298 K 时,反应
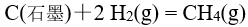 ,
,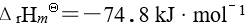 ,
,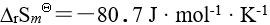 ,则平衡常数
,则平衡常数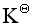 为
为反应
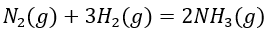 在恒容热量计内进行,生成2 mol
在恒容热量计内进行,生成2 mol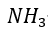 时放热82.7 kJ,则反应的
时放热82.7 kJ,则反应的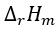
- 下列说法不正确的是
下列关于
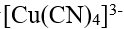 的空间构型及中心离子的杂化方式的叙述正确的是
的空间构型及中心离子的杂化方式的叙述正确的是- 关于歧化反应,正确的叙述是
下列物质中,
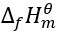 不等于0的是
不等于0的是- 根据化学反应等温方程式,要使反应自发进行的条件是
- 下列各物质的键中极性最小的是
- 在HAc-NaAc组成的缓冲溶液中,若[HAc] > 则该缓冲溶液抵抗外加酸或碱的能力为
- https://image.zhihuishu.com/zhs/teacherExam_h5/COMMONUEDITOR/202109/d8b3e36d15c341f1bc0703db8f66faec.png
- 24号Cr原子的价层电子构型是
- https://image.zhihuishu.com/zhs/teacherExam_h5/COMMONUEDITOR/202109/f6d7d2ab2f914b0b8d62901b5f5bff2e.png
- 对于任何一个化学变化,影响平衡常数数值的因素是
已知
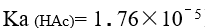 ,
,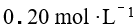 HAc溶液和的 NaAc 溶液等体积混合后,其 pH 值为
HAc溶液和的 NaAc 溶液等体积混合后,其 pH 值为已知
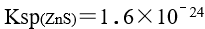 欲使0.10 mol的ZnS在1.0 L的HCl中恰好全部溶解,则该HCl的浓度
欲使0.10 mol的ZnS在1.0 L的HCl中恰好全部溶解,则该HCl的浓度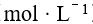 应为
应为已知有以下三个热化学方程式:
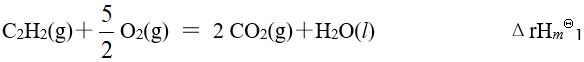

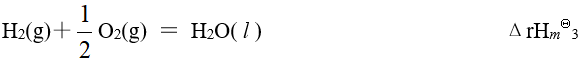
则
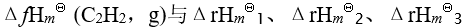 的关系为
的关系为- https://image.zhihuishu.com/zhs/teacherExam_h5/COMMONUEDITOR/202109/68473585a93046dbabceb5f1ee4632dd.png
根据酸碱质子理论,
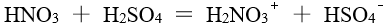 ,正反应中的酸是
,正反应中的酸是- 下列化合物中,相同浓度水溶液的pH 值最高是
- 增加反应物浓度,反应速率加快的主要原因是
- 下列关于分子间作用力说法正确的是
- 体系对环境作20 kJ的功,并失去10 kJ 的热给环境,则体系内能的变化为
在
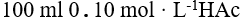 溶液中,加入少量NaAc 固体,溶液的pH 值的变化情况是
溶液中,加入少量NaAc 固体,溶液的pH 值的变化情况是 - 在标准铜锌原电池中,若向铜半电池内加入一定量的氢氧化钠 ,则原电池的电动势将
- 恒压下某反应的正反应活化能为Ea ,逆反应的活化能为Ea’ ,则 Ea -Ea’ 等于该反应的
- 下列热力学函数中数值不为零的是
A:对 B:错
答案:A:对
A:对 B:错
答案:错
A:错 B:对
答案:对
A:错 B:对
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:A:错
A:对 B:错
答案:错
A:对 B:错
A:反应温度 B:反应的活化能 C:催化剂 D:反应物浓度
A:
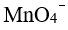 增大
增大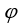 值增大
值增大
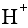 浓度变化对
浓度变化对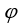 值无影响
值无影响
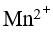 浓度增大则
浓度增大则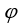 值减小
值减小
A:2 B:1 C:4 D:3
A:通常温度越高,反应的k值越大 B:Ea是k与T之间关系中的主要参数 C:A 、B两反应,Ea (A) > Ea (B) ,则B反应的k一定比A反应的k大 D:一定温度下,反应的k值主要取决于反应物的本性
A:并不改变 B:小于1.10v C:大于1.10v D:等于1.10v
A:
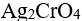 和AgCl
B:AgBr 和 AgCl
C:一齐沉淀
D:
和AgCl
B:AgBr 和 AgCl
C:一齐沉淀
D:AgBr 和 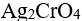
A:0 B:200 C:40 D:-200
A:CO32- B:[Fe(H2O)4(OH)2]+ C:H3O+ D:NH4+
A:
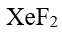
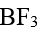
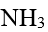
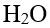
A:
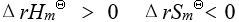
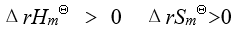
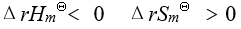

A:5.75 B:90.65 C:74.66 D:38.57
A:恒温下,总压强改变时,各组分的分压随之改变。 B:恒温下,体积改变时,各组分的摩尔分数随之改变。 C:恒容下,温度改变时,体系的总压不变。 D: 恒压下,温度改变时,各组分的体积分数随之改变
A:1 / 6 B:1 / 2 C:1 / 4 D:1 / 8
A:
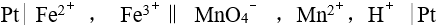
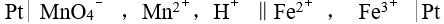
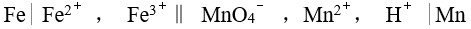
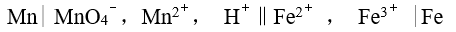
A:
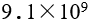
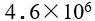
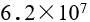

A:
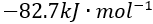
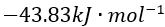
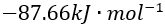
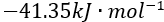
A:用HCl 溶液中和 pH 相同 、体积相等的 和 NaOH 溶液 ,所需 HCl 的量相等 B:用HCl 中和物质的量浓度相同 、体积相等的 KOH 和 溶液 ,所需HCl的量相等
A:
平面正方形,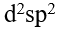 杂化
杂化
正四面体,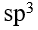 杂化
杂化
变形四边形,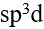 杂化
杂化
平面正方形,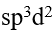 杂化
杂化
A:同一物种里两种原子之间发生的氧化还原反应 B:两种物种里两种原子之间发生的氧化还原反应 C:两种物种里同种原子之间发生的氧化还原反应 D:同一物种里同种原子之间发生的氧化还原反应
A:Ne(g) B:
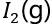
A:
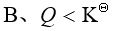
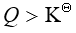
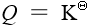
没有
A:LiH B:HI C:HCI D:HBr
A:抗酸碱能力相同 B:抗酸能力 < 抗碱能力 C:抗酸能力 > 抗碱能力 D:尚无法判断
A:
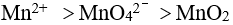
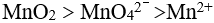 C:
C: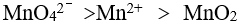
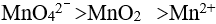
A:
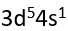
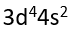
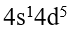
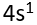
A:
 得到电子,
得到电子,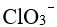 失去电子
失去电子
 是还原剂,
是还原剂,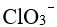 是氧化剂
C:碘的氧化数由0增至+5,氯的氧化数由+5降为0
D:此反应为氧化还原反应
是氧化剂
C:碘的氧化数由0增至+5,氯的氧化数由+5降为0
D:此反应为氧化还原反应
A:反应产物的浓度 B:体系的总压力 C:体系的温度 D:反应物的浓度
A:4.75 B:3.95 C:5.13 D:8.78
A:2.6 B:
0.3
C:2.2 D:3.1A:
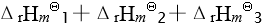
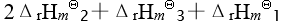
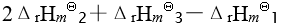
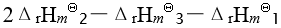
A:-30 B:无法确定 C:< 30 D:30
A:
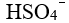
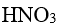
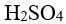
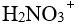
A:
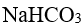
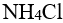
HAc
D: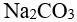
A:反应物的活化能下降 B:反应物的活化分子百分数增加 C:反应物的活化分子数增加 D:单位时间内分子间碰撞数增加
A:分子型物质的沸点总是随相对分子质量增大而增大 B:色散力存在于所有相邻分子间 C:大多数含氢化合物中都存在氢键 D:极性分子间只存在取向力
A:+10 kJ B:-10 kJ C:-30 kJ D:+30 kJ
A:变大 B:变小 C:无法判断 D:不变
A:不变 B:变大 C:无法判断 D:变小
A:ΔU B:-ΔU C:Δ H D:-Δ H
A:
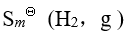
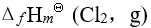
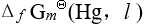
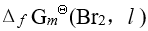
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!

