提示:内容已经过期谨慎付费,点击上方查看最新答案
物理化学
- 影响沸点升高常数和凝固点降低常数值的主要因素是( )
- 温度为T时,纯液体A的饱和蒸汽压为
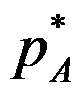 ,化学势为
,化学势为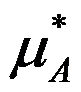 ,在1
,在1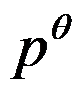 时,凝固点为
时,凝固点为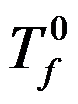 ,向A溶液中加入少量溶质形成稀溶液,该溶质是不挥发的,则
,向A溶液中加入少量溶质形成稀溶液,该溶质是不挥发的,则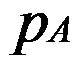 、
、 、
、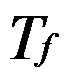 的关系是( )
的关系是( ) - 两只各装有1kg水的烧杯,一只溶有0.01mol蔗糖,另一只溶有0.01molNaCl,按同样速度降温冷却,则:( )
- 25℃时水的饱和蒸气压为3.168kPa, 此时液态水的标准生成吉布斯自由能fGm为-237.19kJ·mol-1,则水蒸气的标准生成吉布斯自由能为:( )
- 等温等压下,在A和B组成的均相体系中,若A的偏摩尔体积随浓度的改变而增加,则B的偏摩尔体积将:( )
- 理想气体从状态p1,V1,T 等温膨胀到p2,V2,T,此过程的ΔA 与ΔG 的关系为( )
- ΔG=0 的过程应满足的条件是( )
- 下列哪个封闭体系的内能和焓仅是温度的函数( )
- 1mol理想气体(1)经定温自由膨胀使体积增加1倍;(2)经定温可逆膨胀使体积增加1倍;(3)经绝热自由膨胀使体积增加1倍;(4)经绝热可逆膨胀使体积增加1倍。在下列结论中何者正确?( )
- 某气体的状态方程服从p(Vm - b) = RT,其中b为常数,则为:( )
- 下面的表述中不正确的是( )
- 在一定温度和压力下,对于一个化学反应,能用以判断其反应方向的是:( )
- 关于三相点, 下面的说法中正确的是( )
- 区别单相系统和多相系统的主要根据是( )
- 加入惰性气体对哪一个反应能增大其平衡转化率?( )
- 2mol A物质和3mol B物质在等温等压下混和形成液体混合物,该系统中A和B的偏摩尔体积分别为1.79 10-5m3·mol-1, 2.15 10-5m3·mol-1, 则混合物的总体积为:( )
- 从多孔硅胶的强烈吸水性能说明在多孔硅胶吸水过程中,自由水分子与吸附在硅胶表面的水分子比较,两者化学势的高低如何?( )
- 关于克劳修斯-克拉佩龙方程下列说法错误的是( )
- 在一绝热恒容箱中, 将NO(g)和O2(g)混合,假定气体都是理想的, 达到平衡后肯定都不为零的量是( )
- 氢气进行不可逆循环( )
- 有下述两种说法:
(1) 自然界中,风总是从化学势高的地域吹向化学势低的地域 (2) 自然界中,水总是从化学势高的地方流向化学势低的地方。
上述说法中,正确的是:( ) - 已知苯一乙醇双液体系中,苯的沸点是353.3K, 乙醇的沸点是351.6K, 两者的共沸组成为:含乙醇47.5%(摩尔分数),沸点为341.2K。 今有含乙醇77.5%的苯溶液,在达到气、液平衡后,气相中含乙醇为y2,液相中含乙醇为 x2。 若将上述溶液精馏,则能得到:( )
- 已知373K时液体A的饱和蒸气压为133.24kPa,液体B的饱和蒸气压为66.62kPa。设A和B形成理想溶液,当溶液中A的物质的量分数为0.5时,在气相中A的物质的量分数为:( )
- 某体系状态A径不可逆过程到状态B,再经可逆过程回到状态A,则体系的ΔG和ΔS满足下列关系中的哪一个 ( )
- 下列各式哪个表示了偏摩尔量:( )
- 化学反应的热力学平衡常数
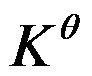 数值的大小只表明了反应能进行的程度,并不能直接说明反应的自发方向。( )
数值的大小只表明了反应能进行的程度,并不能直接说明反应的自发方向。( ) - 偏摩尔量因为与浓度有关,所以它不是一个强度性质。 ( )
- 根据热力学第二定律
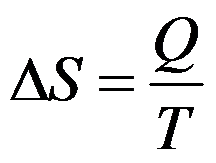 ,能得出
,能得出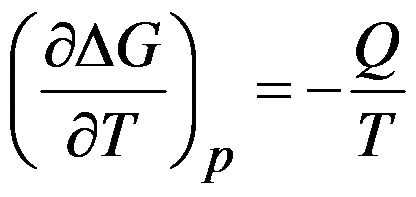 ,从而得到
,从而得到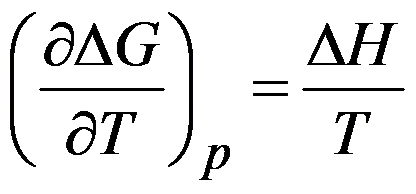 。 ( )
。 ( ) - 在标准压力下加热某物质,温度由T1上升到T2,则该物质吸收的热量为
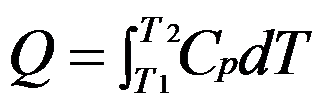 ,在此条件下应存在ΔH=Q的关系。( )
,在此条件下应存在ΔH=Q的关系。( ) - 可逆过程中,体系对环境做功最大,而环境对体系做功最小。( )
- 如同理想气体一样,理想液态混合物中分子间没有相互作用力。( )
- 多相反应的平衡常数与参加反应的固体存在量无关。( )
- 公式
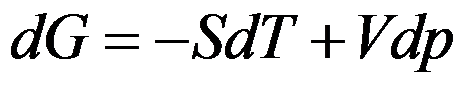 只适用于可逆过程。( )
只适用于可逆过程。( ) - 部分互溶双液系总以互相共轭的两相平衡共存。( )
- 单组分系统的熔点随压力的变化可用克劳休斯-克拉佩龙方程解释。( )
- 双组分体系中,易挥发组分在气相中的组成大于其在液相中的组成。( )
- 理想混合气体中任意组分B的逸度就等于其分压力pB。( )
- 二元液系中若A组分对拉乌尔定律产生正偏差,那么B组分必定对拉乌尔定律产生负偏差。( )
- 自由能G是一状态函数,从始态I到终态II,不管经历何途径,DG总是一定的。( )
- 理想气体反应,定温定容条件下添加惰性组分时,平衡将向体积减小的方向移动。( )
- 处于两相平衡的1molH2O(l)和1molH2O(g),由于两相物质的温度和压力相等,因此在相变过程中ΔU=0,ΔH=0。( )
- 化学反应的平衡浓度不随时间而变化,但随起始浓度的变化而变化;化学反应的热力学平衡常数不随时间变化也不随起始浓度变化而变化。( )
- 在工业上,从反应体系中将产物移出,从而促使化学平衡正向移动提高产率。( )
- 封闭体系中,由状态1经定温、定压过程变化到状态2,非体积功
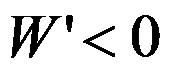 ,且有
,且有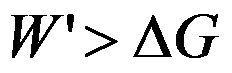 和
和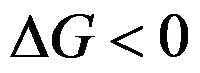 ,则此变化过程一定能发生。( )
,则此变化过程一定能发生。( ) - 完全互溶双液系T-x图中,溶液的沸点与纯组分的沸点的意义是一样的。( )
- 在水的三相点,冰、水、水蒸气三相共存,此时的温度和压力都有确定值,体系的自由度为0。( )
- 将克—克方程的微分式用于纯物质的液气两相平衡,因为ΔvapHm>0,所以随着温度的升高,液体的饱和蒸气压总是升高的。( )
- 相图中的点都是代表体系状态的点。( )
- Q和W不是体系的性质,与过程有关,所以Q + W也由过程决定。 ( )
- 可以利用化学反应的
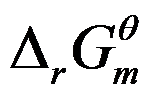 来判断反应的自发方向:
来判断反应的自发方向: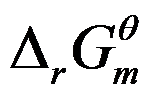 <0,反应正向进行;
<0,反应正向进行;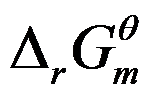 >0,反应逆向进行;
>0,反应逆向进行;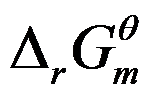 =0,化学反应达到平衡。( )
=0,化学反应达到平衡。( )
A:溶质本性 B:溶剂本性 C:温度和压力 D:温度和溶剂本性
答案:(A)溶剂本性
A: B: C: D:
答案:pA*> pA μA*>μA Tf*>Tf
A:两杯同时结冰 B:视外压而定 C:溶有蔗糖的杯子先结冰 D:溶有NaCl的杯子先结冰
答案:(A)溶有蔗糖的杯子先结冰
A:-245.04kJ·mol-1 B:-228.60kJ·mol-1 C:-245.76kJ·mol-1 D:-229.34kJ·mol-1
答案:-228.60kJ/mol
A:减小 B:不变 C:不一定 D:增加
答案:减小
A:ΔA>ΔG B:ΔA=ΔG C:ΔA<ΔG D:无确定关系
A:等温等压且非体积功为零的过程 B:可逆绝热过程 C:等温等容且非体积功为零的过程 D:等温等压且非体积功为零的可逆过程
A:稀溶液 B:理想溶液 C:所有气体 D:理想气体
A:S1=S2,S3=S4=0 B:S1=S4,S2=S3 C:S1= S2= S3= S4 D:S1= S2=S3,S4=0
A:等于零; B:小于零 ; C:大于零; D:不能确定 。
A:在定压下, 固体混合物都不会有确定的熔点 B:在定压下, 纯固体物质不一定都有确定的熔点 C:在定压下, 纯液态物质有确定的唯一沸点 D:在定温下, 液体的平衡蒸气压与外压有关
A:rHm B:rGm C:rGm D:Kp
A:纯物质和多组分系统均有三相点 B:三相点是纯物质的三个相平衡共存时的温度和压力所决定的相点 C:三相点就是三条两相平衡线的交点 D:三相点的温度可随压力改变
A:物质组成是否相同 B:物理性质是否相同 C:化学性质是否相同 D:物理性质和化学性质是否都相同
A:CO(g) + H2O(g) = CO2(g) + H2(g) B:CH3COOH(l) + C2H5OH(l) = H2O(l) + C2H5COOH3(l) C:C6H5C2H5(g) = C6H5C2H3(g) + H2(g) D:3/2 H2(g) + 1/2 N2(g) = NH3(g)
A:9.6710-5m3 B:1.00310-4m3 C:9.8510-5m3 D:8.9510-5m3
A:相等 B:不可比较 C:前者高 D:前者低
A:该方程既适用于液-气平衡又适用于固-气平衡 B:该方程假定与固相或液相平衡的气体为理想气体 C:该方程假定气体的体积远大于液体或固体的体积 D:该方程仅适用于液-气平衡
A:ΔH, ΔS, ΔG B:ΔS, ΔU, W C:Q, ΔU, ΔH D:Q, W, ΔU
A:ΔU>0 B:ΔS>0 C:ΔS<0 D:ΔS=0
A:(1) B:(1)和(2) C:(2) D:都不对
A:纯乙醇 B:纯乙醇和恒沸混合物 C:纯苯 D:纯苯和恒沸混合物
A:1/3 B:2/3 C:1/2 D:1
A:ΔG < 0, ΔS < 0 B:ΔG > 0, ΔS > 0 C:ΔG > 0, ΔS = 0 D:ΔG = 0, ΔS = 0
A: B: C: D:
A:对 B:错
A:对 B:错
A:错 B:对
AI参考:B:对。热力学第二定律指出,在一个封闭系统中,能量转化和传递的方向是单向的,并且不具有循环性。因此,根据热力学第二定律,不可能从单一热源获取热量并将其完全转化为有用功而不产生其他影响或损失。因此,选项A是错误的,而选项B是正确的。'
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
AI参考:答案是B:错。在工业上,通过移除反应产物来促进化学平衡正向移动可以提高产率是不正确的。通常,通过控制反应条件(如温度、压力、浓度等)来改变反应速率,从而控制产物的生成量。通过移除产物来改变反应速率通常不会对产率产生积极影响,因为这不会改变反应进行的程度。因此,判断题表述错误。'
A:错 B:对
A:对 B:错
AI参考:A. 对。完全互溶双液系T-x图中,溶液的沸点与纯组分的沸点表示的含义是一样的,都是指该物质在该温度下的蒸发温度。'
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
AI参考:答案是B:错。判断一个反应的自发方向需要通过焓变和熵变来判断,而不仅仅是看化学反应的速率。根据焓变和熵变的不同组合,可以得出不同类型反应的自发方向。因此,不能仅通过化学反应的速率来判断反应的自发方向。'
温馨提示支付 ¥2.20 元后可查看付费内容,请先翻页预览!







