第二章单元测试
nmol某气体的恒容下由T1加热到T2,其熵变为ΔS1,相同量的气体在恒压下由T1加热到T2,其熵变为ΔS2,则ΔS1与ΔS2的关系为 ( )。
- 一理想气体在500 K时作等温膨胀,已求得系统的熵变ΔS=10 J∙K−1。若此过程中系统做功仅是最大功的1/10,则系统从热源中吸热( )。
1 mol理想气体从p1、V1、T1分别经:(a) 绝热可逆膨胀到p2、V2、T2;(b) 绝热恒外压膨胀到p3、V3、T3,若p2 = p3,则 ( )。
- 下列等温混合过程的熵变为 ( )。1mol O2(p, V) + 1mol N2 (p, V)
 O2、N2 (p, 2V)
O2、N2 (p, 2V) - 101.3 kPa下的水经下列两个不同过程变为373.2 K、101.3 kPa 下的水汽:(1)等温等压可逆蒸发;(2)向真空蒸发。则(1)、(2)两个过程中,下列关系正确的是 ( )。
下列各过程中
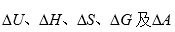 均为零的是 ( )。
均为零的是 ( )。- 下列过程中可直接用dH = TdS + Vdp公式进行计算的过程是 ( )。
- 下面关系式中不正确的是 ( )。
- 某一化学反应的热效应除以反应温度T,即得此反应的
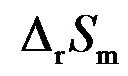 。( )
。( ) - 有两个可逆Carnot热机,在高温热源温度为500 K,低温热源分别为300 K和250 K之间工作,若两者分别经一个循环后所作的功相等,则两个热机的效率相等,但两个热机自低温热源吸收的热量和向高温热源放出的热量不等。( )
理想气体进行等温膨胀,从p1、V1状态膨胀到p2、V2状态,其
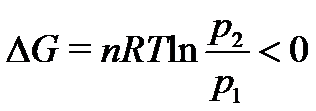 ,则该过程自发进行。( )
,则该过程自发进行。( )- (a) H2和O2在绝热钢瓶中发生反应生成水;(b) 液态水在373 K和101.3 kPa下蒸发成水蒸汽。(a)和(b)两个过程的热力学函数ΔA的变化均大于零。( )
A:
ΔS1 =ΔS2
ΔS1>ΔS2
ΔS1<ΔS2
ΔS1 =ΔS2 = 0
答案:
ΔS1<ΔS2
A:500 J
B:5000 J
C:-500 J
D:-5000 J
A:
T3>T2, V3>V2,S3>S2
T3 = T2, V3 = V2,S3=S2
T3<T2,V3>V2,S3<S2
T3>T2,V3<V2,S3<S2
A:不确定
B:ΔS>0
C:ΔS=0
D:ΔS<0
A:ΔH1<ΔH2,ΔG1=ΔG2=0
B:ΔH1=ΔH2,ΔG1=ΔG2=0
C:ΔH1>ΔH2,ΔG1=ΔG2=0
D:ΔH1=ΔH2,ΔG1= 0,ΔG2<0
A:
H2在一体积恒定的绝热容器中燃烧
C:理想气体的Joule-Thomson 节流过程
D:冰在273.15 K、101.3 kPa下融化
A:363.2 K的水蒸气在101.3 kPa压力下凝聚为水
B:CO(g)进行绝热不可逆膨胀
C:电解水制取氢气和氧气
D:N2(g)和H2(g)混合在298.2 K、pӨ压力下生成NH3 (g)
A:
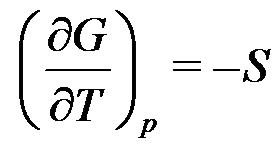
B:
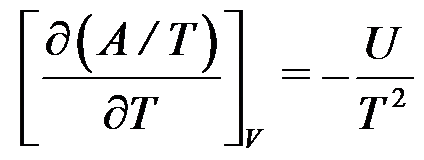
C:
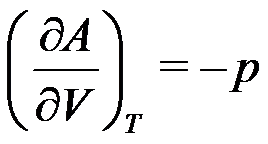
D:
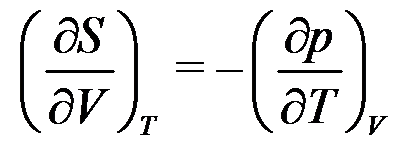
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!



