第三章单元测试
关于偏摩尔量的表达式,正确的是( )。
由A和B两种液体组成的混合物溶液的体积与下面哪些因素无关?
定温、定压下,A和B组成的均相系统,若A的偏摩尔体积随系统的组成的变化而增大,那么B的偏摩尔体积随系统组成的变化将( )。
关于化学势的表达式,正确的是( )。
下列关于化学势的关系式,不正确的是( )。
关于气体化学势的描述,不正确的是( )。
关于拉乌尔定律,下列描述哪个是正确的( )。
对理想溶液的形成过程,下列表达式不正确的是( )。
- 在相同温度和压力下,相同质量摩尔浓度的食盐水和葡萄糖水的渗透压是一样的。
- 稀溶液的凝固点降低、沸点升高等依数性均是因为稀溶液导致溶剂的蒸气压降低。
下列表达式与拉乌尔定律无关的是( )。
恒温时,在
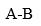 双液系中,若增加A组分使其分压
双液系中,若增加A组分使其分压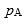 上升,则B组分在气相中的分压
上升,则B组分在气相中的分压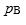 将( )。
将( )。保持压力不变,在稀溶液中溶剂的化学势
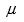 随温度降低而( )。
随温度降低而( )。理想液态混合物的混合性质是( )。
温度为
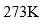 ,压力为
,压力为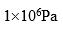 下液态水和固态水的化学势
下液态水和固态水的化学势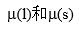 之间的关系为( )。
之间的关系为( )。在等温、等压条件下,溶剂A和溶质B形成一定浓度的稀溶液,采用不同浓度表示的话,则( )。
下列哪个不是稀溶液的依数性( )。
有4杯换不同溶质相同浓度
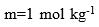 的水溶液,分别测其沸点,沸点升高的最多的是( )。
的水溶液,分别测其沸点,沸点升高的最多的是( )。A和B的摩尔体积没有相关性,二者形成的混合液中,二者的偏摩尔体积之间也没有相关性。
定温定压条件下,混合体系中,组分B的偏摩尔量也是其化学势。
混合体系的某组分的广度性质,其偏摩尔量与其物质的量的乘积具有加和性。
只有在等温、等压、除B以外的其他组分的量保持不变时,某广度性质对组分B的物质的量的偏微分才称为偏摩尔量。
偏摩尔体积是强度性质,因此由A和B组成的混合系统,不论系统的组成如何变化,A和B的偏摩尔体积不变
混合体系中,某组分B用Gibbs自由能表示的化学势也是其偏摩尔量。
混合体系中,某组分B的化学势可以用U、H、A、G对组分B的物质的量的偏微分表示,因限定条件不同,所以,四种热力学函数表示的化学势数值也不同。
自发进行的相转移过程,组分B总是由化学势较大的一相流向化学势较小的一相。
溶剂中溶入挥发性溶质,肯定会引起溶液的蒸气压升高。
标准态是人为规定的某些特定状态。
在相同温度和压力下,纯溶剂的蒸气压大于其混合溶液的蒸气压。
在相同温度和压力下,纯溶剂的化学势大于其在稀溶液中的化学势。
在100 kPa下,往纯水中加入少量KCl,与纯水相比,此稀溶液的沸点升高。
A:
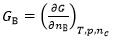 B:
B: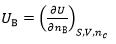
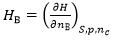 D:
D: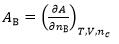
答案:
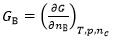
A:A的摩尔体积 B:A的物质的量 C:温度 D:B的物质的量
A:增大 B:减小 C:
相等
A:
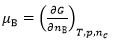 B:
B: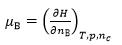 C:
C: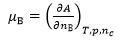 D:
D: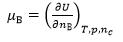
A:
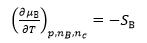 B:
B: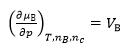 C:
C: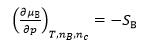 D:
D: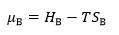
A:纯理想气体化学势是温度和压力的函数。 B:相同温度和压力下,纯理想气体化学势大于其在混合气体中的化学势。 C:混合理想气体化学势是温度、压力和组成的函数。 D:
相同温度和压力下,纯理想气体化学势小于其在混合气体中的化学势。
A:表明稀溶液的溶剂的蒸气压与溶剂在溶液中的摩尔分数的关系 B:
表明稀溶液的溶质的蒸气压与溶剂在溶液中的摩尔分数的关系
C:表明稀溶液的溶剂的蒸气压与溶质在溶液中的摩尔分数的关系 D:表明稀溶液的溶质的蒸气压与溶质在溶液中的摩尔分数的关系A:
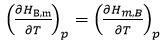 B:
B: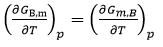 C:
C: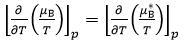 D:
D: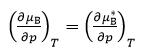
A:对 B:错
A:错 B:对
A:
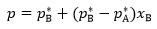 B:
B: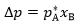 C:
C: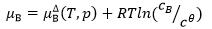 D:
D: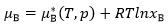
A:不变 B:不确定 C:上升 D:下降
A:不确定 B:降低 C:不变 D:增大
A:
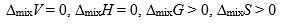 B:
B: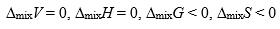 C:
C: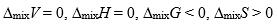 D:
D: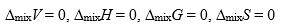
A:
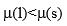 B:
B: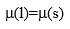 C:
C: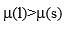 D:无确定关系
D:无确定关系
A:溶液中A和B的活度因子不变 B:溶液中A和B的活度不变 C:溶液中A和B的标准化学势不变 D:溶液中A和B的化学势不变
A:凝固点降低 B:渗透压 C:凝固点升高 D:沸点升高
A:
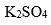 B:
B: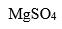 C:
C: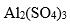 D:
D: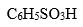
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对



