提示:内容已经过期谨慎付费,点击上方查看最新答案
物理化学
- 公式
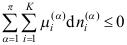 是适用于封闭系统不做非体积功时的相变化和化学变化过程的可逆性判据。( )
是适用于封闭系统不做非体积功时的相变化和化学变化过程的可逆性判据。( ) - 对于工作在300K和800K两热源间的可逆热机,其
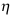 是一个定值。( )
是一个定值。( ) - 如果一次法所得反应级数nt大于初速率法所得反应真级数nc,预示产物对反应有阻滞作用。( )
- 对于二元系,理论上可存在的最大相数是3个。( )
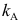 的量纲为浓度·时间1,则该反应为零级反应( )
的量纲为浓度·时间1,则该反应为零级反应( )- 在式
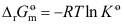 中,
中,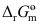 是化学反应达到平衡时的摩尔反应吉布斯函数。( )
是化学反应达到平衡时的摩尔反应吉布斯函数。( ) - 对于化学反应而言,
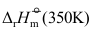 总是大于
总是大于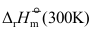 。( )
。( ) - 苯和乙醇二元系具有最低恒沸点,恒温时溶液的蒸汽总压随着液相组成的变化出现极大值,恒压时溶液的沸点随着液相组成的变化出现极小值。( )
- 在温度为
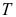 时,理想气体化学反应的恒压热效应
时,理想气体化学反应的恒压热效应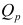 与恒容热效应
与恒容热效应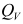 之间的换算关系为
之间的换算关系为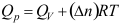 ,其中
,其中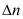 为反应前后物质的量的变化。( )
为反应前后物质的量的变化。( ) - 对于反应
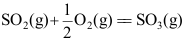 ,其标准摩尔反应焓就等于
,其标准摩尔反应焓就等于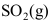 的标准摩尔燃烧焓。( )
的标准摩尔燃烧焓。( ) - T=300K、p=0.2MPa的纯理想气体的化学势与其标准态化学势之差=( )
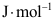 。
。 - 当化学反应
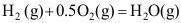 达平衡时,下列式子正确的是( )。
达平衡时,下列式子正确的是( )。 - 一定温度压力下,二元混合物的摩尔体积可表示为
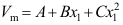 ,则组分1的偏摩尔体积正确的表达式为( )。
,则组分1的偏摩尔体积正确的表达式为( )。 - 二元系的气液平衡相图(恒压相图)中,恒沸点处的自由度为( )。
- 对于理想气体化学反应
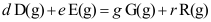 ,标准压力分别取为
,标准压力分别取为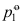 和
和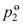 ,相应的标准平衡常数为
,相应的标准平衡常数为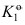 和
和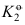 ,如
,如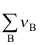 =0,则
=0,则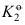 ( )
( )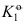 。
。 - 压力为1.0M Pa的范德华气体向真空绝热膨胀,直至压力降至
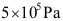 为止。在此膨胀过程中,气体所做的功W( )0。
为止。在此膨胀过程中,气体所做的功W( )0。 - 1mol理想气体的
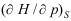 在0.1MPa、300K条件下等于( )。
在0.1MPa、300K条件下等于( )。 - 一混合物的总组成为xo,闪蒸为平衡的气液两相。气相物质的量为nV,组成为yV;液相物质的量为nL,组成为xL,则杠杆规则的表达式为( )。
- 下列反应中,不是基元反应的是( )。
- 已知H2O(l)的标准摩尔生成焓为
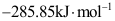 ,标准摩尔生成吉氏函数为
,标准摩尔生成吉氏函数为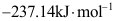 ,以下理解错误的是( )。
,以下理解错误的是( )。 - 对于纯物质,其
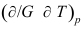 ( )0。
( )0。 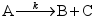 为零级反应,
为零级反应,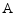 的初始浓度为
的初始浓度为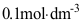 ,半衰期为20 min,则当反应40min时,A的浓度为( )。
,半衰期为20 min,则当反应40min时,A的浓度为( )。- 对于
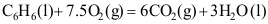 ,其
,其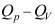 等于( )RT。
等于( )RT。 - 考察压力接近于零时,Z随p变化的斜率
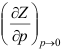 ,发现低温时,
,发现低温时,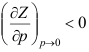 ,高温时
,高温时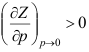 ,其间必有一温度使
,其间必有一温度使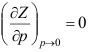 ,这一温度称为( )。
,这一温度称为( )。 - 恒沸混合物(二元系)在气、液两相平衡共存时,自由度计算正确的是( )。
- 根据
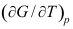 和
和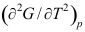 ,对于纯物质,下列关于G与T关系描述正确的是
,对于纯物质,下列关于G与T关系描述正确的是
( ) - 对于连串反应,下列说法错误的是( )
- 当A和B二元系的
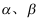 两相达到相平衡时,下列式子中正确的是( )
两相达到相平衡时,下列式子中正确的是( ) - 对峙反应
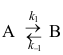 ,当温度一定时由纯A开始,下列说法正确的是( )
,当温度一定时由纯A开始,下列说法正确的是( ) - 关于以逸度表示的平衡常数
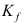 ,下列说法正确的是( )
,下列说法正确的是( ) - 关于溶液,下列说法正确的是 ( )
- 描述平行反应
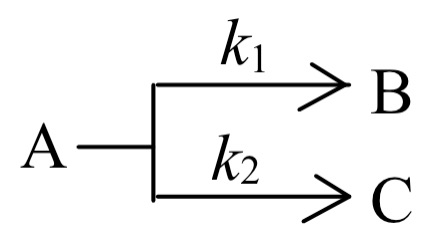 的特点时,以下正确的是( )
的特点时,以下正确的是( ) - 在101325Pa下,1mol某纯液体在其正常沸点时蒸发为气体,下列性质中不发生变化的是(( )
- 298.15K时,下列各热性质中( )的值为零。
- 对于二元理想混合物的气液平衡相图(恒压相图),以下说法正确的是( )
- 在临界点处,以下说法不正确的是( )
- 在一定温度下,反应(NH4)2CO3(s) = 2NH3(g)+ CO2(g) + H2O(g)的标准平衡常数为
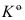 ,分解压力为p,设各气体均视为理想气体,则下列关系式正确的是( )
,分解压力为p,设各气体均视为理想气体,则下列关系式正确的是( ) - 水和异丁醇形成部分互溶系统,关于水和异丁醇的气液液平衡相图,以下说法正确的是( )
- 关于表面活性剂,下列说法正确的是( )
- 对于二元理想混合物的气液平衡相图(恒温相图),以下说法正确的是( )
A:错 B:对
答案:对
A:错 B:对
答案:正确AI参考:正确答案是B:对。可逆热机对外做功时,其工作物质从高温热源吸收热量,再向低温热源放出热量,这两个过程是可逆的,因此其效率为100%,即对外做的功为定值。对于工作在300K和800K两热源间的可逆热机,其效率为1,所以其输出功是一个定值。因此,这个判断题是正确的。'
A:对 B:错
AI参考:答案是B:错。一次法是指通过实验数据直接求得的反应级数,初速率法是指根据反应开始一段时间内的反应速率与反应物浓度的乘积进行反应级数分析的方法。如果一次法所得反应级数nt大于初速率法所得反应真级数nc,并不能预示产物对反应有阻滞作用,因为这两种方法得出的级数并不能直接反映产物的阻滞作用。因此,这个判断题是错误的。'
A:错 B:对
AI参考:正确答案是B:对。二元系理论上可存在的最大相数是3个,选项表述正确。'
A:错 B:对
答案:二级反应AI参考:答案:B。根据题目描述,该反应的速率方程为浓度·时间1,符合零级反应的特征,因此该反应为零级反应。所以答案是B,即对。'
A:错 B:对
答案:错
A:错 B:对
AI参考:答案是B:对。根据题目描述,两个图像中的反应物质在不同条件下的化学反应速率是不同的,通常在浓度、温度、压力等因素的影响下,反应速率会发生变化。因此,无法确定总是大于的关系,需要具体分析实际情况。所以,这个判断题是正确的。'
A:错 B:对
AI参考:正确答案是B:对。苯和乙醇二元系具有最低恒沸点,恒温时溶液的蒸汽总压随着液相组成的变化出现极大值,恒压时溶液的沸点随着液相组成的变化出现极小值。因此,本题说法正确。'
A:对 B:错
答案:ΔrH = ΔrU + ΔnRT AI参考:答案是A:对。根据理想气体反应的恒压热效应和恒容热效应的定义,可以得知两者之间的关系为ΔHp = ΔHv + ΔnRT,其中ΔHp为恒压热效应,ΔHv为恒容热效应,Δn为反应前后物质的量的变化,R为气体常数,T为温度。因此,本题中的换算关系是正确的。'
A:对 B:错
AI参考:答案:B:错。题目描述了两个反应焓,需要分析的是这两个反应焓之间的关系。题目中没有给出这两个反应的具体信息,无法判断它们之间的关系。因此,该题描述不完整,无法做出正确的判断。'
A:1728.95 B:1529.95 C:1629.95
A: B: C:
AI参考:正确答案是C。化学反应平衡时,各物质的浓度不变,反应速率也保持不变,即正逆反应速率相等。因此,正确选项为C,即平衡时,v正=v逆。其他选项中A、B中的速率数值或方向变化不符合平衡条件。'
A: B: C:
AI参考:答案:B推理过程:二元混合物组分1的偏摩尔体积等于组分1的摩尔体积乘以组成1在混合物中的分率。由于题干给出的条件是一定温度压力下,二元混合物的摩尔体积,所以摩尔体积与偏摩尔体积的单位相同。由于二元混合物中组分1的摩尔体积与摩尔分数是成正比的,所以组分1的偏摩尔体积应为v₁-x₁V。综上可得本题的答案为B。其中v₁表示组分1的摩尔体积,x₁表示组成1在混合物中的摩尔分数,V为混合物的摩尔体积。此处选择B项作为答案。A项与C项属于无意义选项,应排除。偏摩尔量是由物质的量不均匀性而引起的物理量,所以摩尔体积不变,分子之间的相互作用就不会变,因为分子的空间位置不发生变化。如果改变了相互作用,说明物质是宏观均匀的。也就是说如果偏摩尔量与分子间相互作用力无关的话,偏摩尔量不会变化。由于组分摩尔体积等于组分在混合物中的摩尔分数乘以混合物的摩尔体积,因此只要将题干中给出的摩尔体积公式两边同乘上组分2的摩尔分数,就得到混合物中组分1的摩尔分数表达式为v₁/V。由此可见选项B表述正确。因此,本题答案为B选项。'
A:1 B:0 C:2
A:= B:< C:>
AI参考:根据题目中的图像信息,当p/po=1时,标准平衡常数k等于1。而题目中给出的p/po值分别为0.5和2,均小于1,因此标准平衡常数k应该小于1。所以,正确答案是B:<。'
A:= B:> C:<
A: B: C:
AI参考:正确答案是C:0.1MPa。根据理想气体状态方程PV=nRT,其中P为压强,V为体积,n为摩尔数,R为气体常数,T为绝对温度。所以,在已知条件下的理想气体体积为1mol时,其压强为0.1MPa。因此,本题答案为C选项。'
A: B: C:
AI参考:根据题目,我们知道这是一个平衡的闪蒸系统,其总组成为x,存在气液两相,气相物质的量为nV,组成为yV,液相物质的量为nL,组成为xL。杠杆规则是用来描述系统中各组分浓度的关系的。在闪蒸系统中,气液两相的组成是相互关联的,因此我们可以将气相和液相的组成相加得到总组成,即(yV+xL)。所以,杠杆规则的表达式为(nV+(yV+xL))=(nL+x),因此选项C是正确答案。'
A:H2+I2 →2HI B:Pb(C2H5)4 →Pb+4C2H5· C:I+H2→HI+H
AI参考:C项,“I + H2→HI+H”不是基元反应。基元反应是指在化学反应中,能够直接且明确表示出反应步骤的反应,即一步完成,不涉及或少量涉及中间化合物的反应。而C选项中,I与H2的反应步骤需要分为两步才能完成,即先形成HI,再与H结合形成H2,因此不属于基元反应。因此,本题的正确选项是C:I + H2→HI+H。'
A:如通过电解由水制备氢气且 =1mol,则至少输入电功237.14kJ B:如反应在电池中可逆进行且 =1mol,则对外作的电功最多为237.14kJ C:如反应在电池中可逆进行且 =1mol,则对外作的电功最多为285.85kJ
A:> B:< C:=
AI参考:正确答案是A:>。根据题目描述,对于纯物质,其属性之间的关系应该用大于号(>)表示。因此,选项A是正确的。选项B和C都不符合题目要求。'
A: B:0 C:
AI参考:由题可知,这是一个零级反应,即反应速率与反应物的浓度无关,只与反应体系的总体大小有关。因此,反应物的浓度在反应过程中保持不变。初始浓度为1,半衰期为20 min。在40 min时,已经经过了两个半衰期加一个半衰期的一半,即反应了约83%的初始浓度。所以,A的浓度为:B. 0所以,正确选项为B。'
A:-1.5 B:0.5 C:1.5
AI参考:从题目中给出的两个
A:临界温度 B:波义耳温度 C:沸点
AI参考:正确答案是B:波义耳温度。在考察压力接近于零时,Z随p变化的斜率随着温度的变化而变化,低温时斜率变大,高温时斜率变小,在中间一定有一个温度,使得斜率为零,这个温度就是波义耳温度。所以答案是B。注意:题目中的图像是一个理想气体状态方程的图像,其中p表示压力,V表示体积,T表示温度,Z表示压缩因子。这个图像并不是一个具体的化学反应或物理现象的图像,而是用来描述理想气体状态变化的。因此,这个问题的答案并不是关于具体的化学反应或物理现象的,而是关于理想气体状态方程的一般规律的。'
A: B: C:
A:因为 ,所以G随T的增大而增大 B:因为 ,所以G随T的变化曲线向下凹 C:因为 ,所以G随T的变化曲线向上凸 D:因为 ,所以G随T的增大而减小
A:前步反应的产物为下步反应的反应物 B:中间产物的浓度在反应过程中有极大值 C:复合反应速率主要决定于反应速率较大的那一个反应。 D:凡是连串反应均可提出恒稳态假设
A: , B: , C: , D: ,
AI参考:正确选项为 C: , 。 当A和B二元系的两个相达到相平衡时,它们之间的物质交换达到平衡状态,不会发生明显的物质转移或化学反应。因此,选项C中的符号“”表示物质的平衡状态,是正确的。选项A、B、D中的符号均表示物质的存在或转移,不符合题目要求。"
A:起始时A的消耗速率最快 B:反应进行的净速率是正逆反应速率之差 C: 的值是恒定的 D:达到平衡时正逆反应的速率系数相等
A: 是只决定于反应本性和温度的常数 B:仅对于理想气体反应, 才是只决定于反应本性和温度的常数 C: 的量值与 的取值有关 D: 与系统总压和各物质的平衡组成无关
A:理想稀溶液中,溶剂的蒸汽压服从拉乌尔定律、溶质的蒸汽压服从亨利定律 B:稀的理想溶液中,所有组分的蒸汽压均服从拉乌尔定律 C:理想溶液中,所有组分的蒸汽压均服从拉乌尔定律 D:稀的理想溶液中,溶剂的蒸汽压服从拉乌尔定律、溶质的蒸汽压服从亨利定律
A:反应物消耗速率主要决定于反应速率较大的那个反应 B:反应产物B和C的量之比等于两个平行反应的速率系数之比 C:和的比值不随温度而变 D:反应的总速率等于两个平行的反应速率之和
AI参考:正确选项为:B:反应产物B和C的量之比等于两个平行反应的速率系数之比 平行反应的特点是:在一定条件下,几个反应同时发生,相互之间无影响。其特点是对于一定的温度下物质的物理状态保持不变(比值关系不随温度变化而变化)。在这个体系中所有的化学反应之间总有一种或几种化学反应在达到平衡之前速度大一些。总的来说,如果对两种物质的混合物中某种成分进行研究时,就会发现物质的化学组成是有一种以上的化学反应所共同决定的一种比较复杂状态。这种情况下反应物同时消耗速率不等,各物质变化的比例不一样,不能将两个平行反应的反应速率简单相加。所以D选项错误。因此A选项和C选项描述不准确。反应的速率系数是一个与反应物浓度无关的常数,因此反应产物B和C的量之比等于两个平行反应的速率系数之比,所以B选项正确。 以上内容仅供参考,建议咨询专业人士获取更准确的信息。"
A:U B:V和密度 C:蒸汽压和蒸发焓 D:G
A: B: C: D:
AI参考:正确选项为【B】和【C】。 因为根据热力学第二定律,不可能从单一热源吸热使之完全变为有用功,而其他方面没有变化,所以选项B和C的热性质为零。选项A和D的热性质不是零,例如焓是一个状态函数,会随着物质的变化而变化。所以选择B和C。"
A:液相线表达沸点随液相组成的变化 B:气相线为露点线 C:液相线为泡点线 D:气相线表达饱和蒸汽组成随温度的变化
A:范德华气体的临界压缩因子等于1 B:范德华气体的临界压缩因子等于0.375 C:实际气体的临界压缩因子等于1 D:实际气体的临界压缩因子等于0.375
A: B: C: D:
AI参考:正确选项为B。 标准平衡常数表示反应达到平衡时生成物浓度幂之积与反应物浓度幂之积的比值。在(NH4)2CO3(s) = 2NH3(g) + CO2(g) + H2O(g)反应中,根据题目要求,只考虑温度、压力等影响平衡的因素,因此无需分析浓度。对于气体反应,压力对平衡常数的影响可以忽略不计,因为气体反应的平衡常数只与温度有关。因此,选项B是正确的。 需要注意的是,对于其他类型的反应,压力可能会对平衡常数产生影响,需要根据具体反应和条件进行计算和分析。"
A:相图中气相线表达露点随气相组成的变化 B:相图中液液平衡曲线表达溶解度随温度的变化 C:相图中液相线表达泡点或沸点随液相组成的变化 D:当系统处于三相线上时,水相、醇相和气相三相共存
AI参考:正确选项是:A:相图中气相线表达露点随气相组成的变化;C:相图中液相线表达泡点或沸点随液相组成的变化。 A选项描述的是气液平衡相图中的气相线,它通常用来表示随着气相组成的变化,露点是如何变化的。C选项描述的是液液平衡相图中的液相线,它通常用来表示随着液相组成的变化,泡点或沸点是如何变化的。B选项描述的是液液平衡相图中的溶解度曲线,通常用于描述温度如何影响物质的溶解度。在多组分系统中,三相线是指气相、液相和固相之间的平衡点,当系统处于三相线上时,三相共存。所以,D选项也是正确的。"
A:表面活性剂可改变固体表面的润湿性能 B:表面活性剂可降低不易溶于水的物质在水中的溶解度 C:表面活性剂可在溶液表面定向排列 D:表面活性剂可显著增大溶液的表面张力
A:气相线处于液相线的下方,为曲线 B:气相线表达溶液的蒸气压或饱和蒸汽的总压随气相组成的变化 C:液相线表达溶液的蒸气压或饱和蒸汽的总压随液相组成的变化 D:液相线为直线是理想混合物的一个特征







