第三章测试1.
氢原子的原子轨道能量取决于量子数:
A:n和l; B:n; C:l; D:m。
答案:B
2.
对某原子中的各电子来说,其主量子数n≤3,则原子处于基态时:
A:只有s电子; B:只有s电子和p电子; C:有s、p和d电子。 D:只有p电子; 3.
第三周期元素的基态原子中,不可能出现d电子,主要依据是:
A:洪特(Hund)规则 B:泡里(Pauli)不相容原理 C:能量守恒原理 D:能级交错 4.
按照核外电子的排布规则,预测原子序数从1~100的100种元素的原子中,具有3d电子的元素有:
A:60种 B:70种; C:80种; D:50种。 5.
下列基态离子中,具有d7电子构型的是:
A:Fe3+; B:Ni2+; C:Fe2+。 D:Co2+; 6.
首先提出微观粒子运动波动方程式的科学家是:
A:普朗克(Planck); B:玻尔(Bohr); C:鲍林(Pauling)。 D:薛定谔(SchrÖdinger); 7.
原子序数为33的元素,其原子在n=4,l=1,m=0的轨道中电子数为:
A:3; B:2; C:1; D:4。 8.
对下图所示,正确的叙述是:
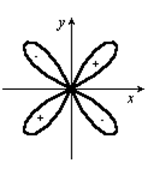
A:图形表示dxy原子轨道角度分布图; B:图形表示dxy电子云角度分布图。 C:图形表示dxy原子轨道的形状; D:图形表示dyz原子轨道角度分布图; 9.
已知某元素+3价离子的电子排布式为1s22s22p63s23p63d5,该元素在周期表中属于:
A:Ⅷ族; B:ⅤB族; C:ⅤA族。 D:ⅢB族; 10.
第二周期中N的第一电离能比它前后相邻的C和O都要大。
A:错 B:对
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!