第四章 酸碱滴定法概述:本章是化学分析法中介绍的第一种滴定分析法,在全面灌输滴定分析法思路的基础上重点介绍酸碱质子理论、酸碱指示剂、酸碱滴定法基本原理及酸碱滴定法的应用。4.1酸碱质子理论:重点介绍酸碱质子理论[单选题]用
4.2水溶液中重要酸碱反应及共轭酸碱对Ka、Kb关系:以酸碱质子理论为前提介绍水溶液中的重要酸碱反应及共轭酸碱对Ka、Kb关系
4.3酸碱指示剂定义及作用原理:介绍酸碱指示剂的定义、作用原理、理论变色范围及变色点。
4.4几种重要的酸碱指示剂及使用注意事项:介绍了甲基橙、甲基红、酚酞等几种常见的酸碱指示剂及其使用注意事项。
4.5酸碱滴定法基本原理:一元强酸(碱)的滴定:重点介绍一元强酸(碱)的滴定曲线绘制,滴定突跃的定义及影响因素、指示剂的选择、滴定速度的把握等。
4.6酸碱滴定法基本原理:一元弱酸(碱)的滴定:重点介绍一元弱酸(碱)的滴定曲线绘制,滴定突跃的影响因素、弱酸弱碱可被准确滴定的可行性判据、指示剂的选择等。
4.7酸碱滴定法基本原理:多元弱酸(碱)的滴定:介绍了多元弱酸(碱)的滴定情况,详细介绍了磷酸和碳酸钠的滴定。
4.8酸碱标准溶液的配制和标定:介绍了HCl和NaOH标液的配制和标定。
4.9酸碱滴定法的应用实例:介绍了酸碱滴定法在实际中的应用如铵盐中和有机化合物中氮含量的测定、食醋总酸度的测定、混合碱的测定等。
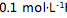 HCl滴定
HCl滴定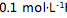
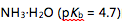 的pH突跃范围是6.3-4.3。用
的pH突跃范围是6.3-4.3。用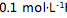 HCl滴定
HCl滴定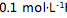 某一元碱
某一元碱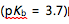 的pH突跃范围是( )选项:[6.3-3.3 , 6.3-4.3 , 7.3-3.3, 7.3-4.3 ]
的pH突跃范围是( )选项:[6.3-3.3 , 6.3-4.3 , 7.3-3.3, 7.3-4.3 ] [单选题]用
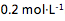 HCl滴定
HCl滴定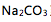 至第一计量点,此时可选用的指示剂是( )选项:[酚酞 , 甲基红 , 甲基橙 , 中性红]
至第一计量点,此时可选用的指示剂是( )选项:[酚酞 , 甲基红 , 甲基橙 , 中性红][判断题]强碱滴定弱酸时,滴定突跃范围大小受酸碱浓度和弱酸的
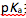 控制。( )选项:[错, 对]
控制。( )选项:[错, 对][多选题]实验室中常用来标定HCl的基准物质有( )选项:[NaOH , 邻苯二甲酸氢钾, 基准
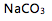 , 硼砂 ]
, 硼砂 ][多选题]下列物质中,哪几种不能用标准强碱直接滴定( )选项:[苯酚
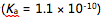 ,
, 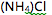 , 邻苯二甲酸氢钾
, 邻苯二甲酸氢钾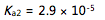 ,
, 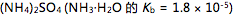 ,
, 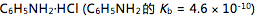 ]
][单选题]已知邻苯二甲酸氢钾的摩尔质量为
 ,用它标定
,用它标定 的NaOH溶液(20-30 mL),应称取邻苯二甲酸氢钾约多少g( )选项:[0.1 g, 0.5 g , 0.05 g , 0.25 g ]
的NaOH溶液(20-30 mL),应称取邻苯二甲酸氢钾约多少g( )选项:[0.1 g, 0.5 g , 0.05 g , 0.25 g ][单选题]酸碱滴定中选择指示剂的原则是( )选项:[
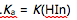 , 指示剂的变色范围全部或部分落入滴定的pH突跃范围内, 指示剂的变色范围与化学计量点完全符合, 指示剂的变色范围应完全落在滴定的pH突跃范围内]
, 指示剂的变色范围全部或部分落入滴定的pH突跃范围内, 指示剂的变色范围与化学计量点完全符合, 指示剂的变色范围应完全落在滴定的pH突跃范围内][单选题]用
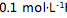 HCl滴定
HCl滴定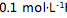 NaOH时的pH突跃范围是9.7 - 4.3。用
NaOH时的pH突跃范围是9.7 - 4.3。用 HCl滴定
HCl滴定 NaOH时的pH突跃范围是( ) 选项:[8.7-5.3 , 7.7-4.3 , 9.7-4.3, 9.7-5.3 ]
NaOH时的pH突跃范围是( ) 选项:[8.7-5.3 , 7.7-4.3 , 9.7-4.3, 9.7-5.3 ][单选题]按照酸碱质子理论,
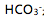 是( )选项:[两性物质 , 缓冲溶液, 碱 , 酸 ]
是( )选项:[两性物质 , 缓冲溶液, 碱 , 酸 ][单选题]以NaOH滴定
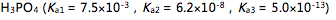 至生成
至生成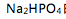 时溶液的pH值为( )选项:[10.7, 9.8 , 7.7 , 4.7 ]
时溶液的pH值为( )选项:[10.7, 9.8 , 7.7 , 4.7 ]
温馨提示支付 ¥1.00 元后可查看付费内容,请先翻页预览!

