第三章 化学反应速率:第三章,主要介绍化学反应速率,了解浓度、温度以及催化剂对化学反应速率的影响。3.1化学反应速率的概念:平均速率与瞬时速率 反应速率方程式 反应级数[单选题]
3.2浓度对反应速率的影响:初始速率法测试反应速率方程式 浓度随时间的变化关系
3.3温度对反应速率的影响:Arrhenius 方程及应用
3.4反应速率理论:碰撞理论要点及能量关系
3.5催化剂与催化作用:催化剂种类、特征及应用
3.6例题讲解1:反应速率方程式确定
3.7例题讲解2:本节讲解例题
3.8例题讲解3:本节讲解例题
3.1化学反应速率的概念:平均速率与瞬时速率 反应速率方程式 反应级数
3.2浓度对反应速率的影响:初始速率法测试反应速率方程式 浓度随时间的变化关系
3.3温度对反应速率的影响:Arrhenius 方程及应用
3.4反应速率理论:碰撞理论要点及能量关系
3.5催化剂与催化作用:催化剂种类、特征及应用
3.6例题讲解1:反应速率方程式确定
3.7例题讲解2:本节讲解例题
3.8例题讲解3:本节讲解例题
 选项:[
选项:[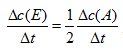 ,
, 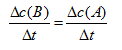 ,
, 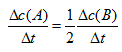 ,
, 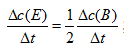 ]
] [单选题]二级反应的速率系数k是( )
选项:[量纲不定的参数, 无量纲的参数, 量纲为mol2·L-2·s-1的参数, 量纲为mol-1·L·s-1的参数]
[单选题]
 选项:[N-M, M-3N, 3N-M, M-N]
选项:[N-M, M-3N, 3N-M, M-N][单选题]对于催化剂特性的描述,不正确的是( )
选项:[催化剂在反应前后其化学性质和物理性质皆不变, 加入催化剂不能实现热力学上不可能进行的反应, 催化剂只能缩短反应达到平衡的时间而不能改变平衡状态, 催化剂不能改变产物平衡组成]
[单选题]生物化学工作者常将37℃时的速率常数与27℃时的速率常数之比称为Q10。若某反应的Q10为2.5 , 则它的活化能(kJ·mol-1)为( )
选项:[96
, 152, 71, 134]
[单选题]升高温度可以增加化学反应速率,主要是因为 ( )
选项:[降低了反应的活化能, 升高了反应的活化能, 增加了活化分子分数, 增加了分子总数]
[单选题]下列叙述中正确的是( )
选项:[反应物浓度升高,活化分子总数升高,反应加快, 催化剂能降低反应活化能,增大正反应速率,降低逆反应速率, 反应级数必等于化学计量式中相应物种的计量数, 反应温度升高,活化分子分数降低,反应加快]
[单选题]
在600 K时,反应:2NO+ O2→2NO2(g)的实验数据如下:
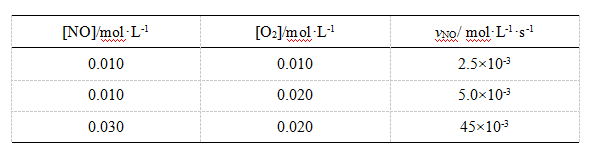
上述反应的速率方程式为: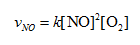
[单选题]
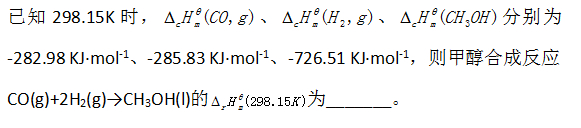 选项:[-128.13 KJ·mol—1, 256.26 KJ·mol--1, -726.51 KJ·mol--1, 128.13 KJ·mol—1]
选项:[-128.13 KJ·mol—1, 256.26 KJ·mol--1, -726.51 KJ·mol--1, 128.13 KJ·mol—1][单选题]
 选项:[3119.4 kJ, -1559.7kJ, -3119.4 kJ, 1559.7kJ]
选项:[3119.4 kJ, -1559.7kJ, -3119.4 kJ, 1559.7kJ][单选题]
在600 K时,反应:2NO+ O2→2NO2(g)的实验数据如下:

上述反应的速率方程式为: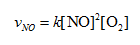
[单选题]
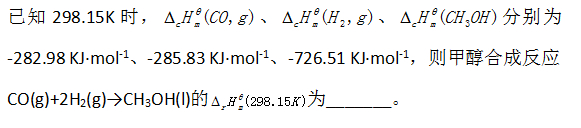 选项:[-128.13 KJ·mol—1, 128.13 KJ·mol—1, -726.51 KJ·mol--1, 256.26 KJ·mol--1]
选项:[-128.13 KJ·mol—1, 128.13 KJ·mol—1, -726.51 KJ·mol--1, 256.26 KJ·mol--1][单选题]
 选项:[M-N, M-3N, 3N-M, N-M]
选项:[M-N, M-3N, 3N-M, N-M][单选题]二级反应的速率系数k是( )
选项:[量纲不定的参数, 量纲为mol2·L-2·s-1的参数, 量纲为mol-1·L·s-1的参数, 无量纲的参数]
[单选题]
 选项:[
选项:[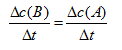 ,
, 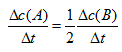 ,
, 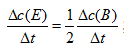 ,
, 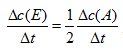 ]
][单选题]对于催化剂特性的描述,不正确的是( )
选项:[催化剂在反应前后其化学性质和物理性质皆不变, 加入催化剂不能实现热力学上不可能进行的反应, 催化剂只能缩短反应达到平衡的时间而不能改变平衡状态, 催化剂不能改变产物平衡组成]
[单选题]下列叙述中正确的是( )
选项:[催化剂能降低反应活化能,增大正反应速率,降低逆反应速率, 反应物浓度升高,活化分子总数升高,反应加快, 反应温度升高,活化分子分数降低,反应加快, 反应级数必等于化学计量式中相应物种的计量数]
[单选题]升高温度可以增加化学反应速率,主要是因为 ( )
选项:[升高了反应的活化能, 增加了分子总数, 增加了活化分子分数, 降低了反应的活化能]
[单选题]生物化学工作者常将37℃时的速率常数与27℃时的速率常数之比称为Q10。若某反应的Q10为2.5 , 则它的活化能(kJ·mol-1)为( )
选项:[96
, 152, 134, 71]
[单选题]
 选项:[1559.7kJ, 3119.4 kJ, -3119.4 kJ, -1559.7kJ]
选项:[1559.7kJ, 3119.4 kJ, -3119.4 kJ, -1559.7kJ]
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!