第五章 酸碱反应和配位反应:第五章介绍化学反应中最经典的酸碱反应以及配位反应。5.1酸碱质子理论:历史回顾、酸碱质子理论、酸和碱的相对强弱[单选题]1 mol·L-1 NaOH溶液里比1 mol·L-1 的NH3水中( )
5.2水的解离平衡和溶液的pH:水的解离平衡、溶液的pH的表示
5.3弱酸、弱碱的解离平衡:一元弱酸、弱碱的解离平衡、多元弱酸的解离平衡、盐类的水解反应
5.4缓冲溶液:同离子效应、缓冲溶液组成、缓冲溶液pH的计算、缓冲范围和缓冲能力
5.5配位化合物:配合物的组成、命名和分类
5.6配位反应与配位平衡:配合物的解离常数和稳定常数、配体取代反应和 电子转移反应、配合物稳定性
5.7例题讲解1:一元弱酸的pH的计算
5.8例题讲解2:多元弱酸的pH的计算
5.9例题讲解3:盐类的pH的计算
5.10例题讲解4:缓冲溶液pH的计算
5.11例题讲解5:配位平衡计算
5.1酸碱质子理论:历史回顾、酸碱质子理论、酸和碱的相对强弱
5.2水的解离平衡和溶液的pH:水的解离平衡、溶液的pH的表示
5.3弱酸、弱碱的解离平衡:一元弱酸、弱碱的解离平衡、多元弱酸的解离平衡、盐类的水解反应
5.4缓冲溶液:同离子效应、缓冲溶液组成、缓冲溶液pH的计算、缓冲范围和缓冲能力
5.5配位化合物:配合物的组成、命名和分类
5.6配位反应与配位平衡:配合物的解离常数和稳定常数、配体取代反应和 电子转移反应、配合物稳定性
5.7例题讲解1:一元弱酸的pH的计算
5.8例题讲解2:多元弱酸的pH的计算
5.9例题讲解3:盐类的pH的计算
5.10例题讲解4:缓冲溶液pH的计算
5.11例题讲解5:配位平衡计算
选项:[H+浓度小, 所含的OH-多, H+浓度大, 所含的H+少]
[单选题]H2S水溶液中,最多的粒子是(H2O分子除外)( )
选项:[H2S, S2-, H+, HS-]
[单选题]含有0.10 mol·L-1 HCl 的 0.10 mol·L-1 HAc溶液中,表示正确的是( )
选项:[c (H+) = c(Ac-), c(H+) >> c(Ac-), c(H+) < c(Ac-)]
[单选题]相同浓度的下列盐溶液的pH值,由小到大的顺序是NaA NaB NaC NaD (A. B. C. D都为弱酸根),则各对应酸在同浓度同温度下,离解度最大的酸是( )
选项:[HA, HC , HD, HB]
[单选题]
 选项:[
选项:[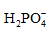 ,
, 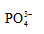 ,
, 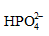 ,
, 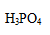 ]
][单选题]用HCl溶液中和pH相同、体积相等的Ba(OH)2和NaOH溶液,所需HCl的量相等。( )
选项:[错, 对]
[单选题]酸碱反应的方向是强酸与强碱反应生成弱酸和弱碱。 ( )
选项:[对, 错]
[单选题]
在多元弱酸的稀溶液中,其酸根的浓度近似等于其最后一级的离解平衡常数。 ( )
[单选题]
0.10mol·L-1弱酸溶液的pH是等于1。 ( )
[单选题]
对于弱电解质溶液,同离子效应使其离解度减小,盐效应使其离解度增加。 ( )
[单选题]含有0.10 mol·L-1 HCl 的 0.10 mol·L-1 HAc溶液中,表示正确的是( )
选项:[c(H+) >> c(Ac-), c(H+) < c(Ac-), c (H+) = c(Ac-)]
[单选题]1 mol·L-1 NaOH溶液里比1 mol·L-1 的NH3水中( )
选项:[所含的H+少, H+浓度大, H+浓度小, 所含的OH-多]
[单选题]H2S水溶液中,最多的粒子是(H2O分子除外)( )
选项:[ H+, S2-, H2S, HS-]
[单选题]
 选项:[
选项:[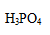 ,
, 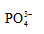 ,
, 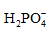 ,
, 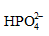 ]
][单选题]用HCl溶液中和pH相同、体积相等的Ba(OH)2和NaOH溶液,所需HCl的量相等。( )
选项:[错, 对]
[单选题]酸碱反应的方向是强酸与强碱反应生成弱酸和弱碱。 ( )
选项:[对, 错]
[单选题]
在多元弱酸的稀溶液中,其酸根的浓度近似等于其最后一级的离解平衡常数。 ( )
[单选题]
0.10mol·L-1弱酸溶液的pH是等于1。 ( )
[单选题]相同浓度的下列盐溶液的pH值,由小到大的顺序是NaA NaB NaC NaD (A. B. C. D都为弱酸根),则各对应酸在同浓度同温度下,离解度最大的酸是( )
选项:[HC , HB, HD, HA]
[单选题]
对于弱电解质溶液,同离子效应使其离解度减小,盐效应使其离解度增加。 ( )
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!