第七章 氧化还原反应:第七章,认识氧化还原反应,理解电极电势。7.1氧化还原反应:氧化值的定义、氧化还原反应方程式的配平[单选题]
7.2电化学电池:原电池的构造、电解池与Faraday定律、原电池电动势的测定、原电池的最大功与Gibbs函数
7.3电极电势:介质的酸碱性、难溶化合物的形成、配合物的形成对电极电势的影响
7.4电极电势的应用:本节讲解稀溶液的依数性。
7.1氧化还原反应:氧化值的定义、氧化还原反应方程式的配平
7.2电化学电池:原电池的构造、电解池与Faraday定律、原电池电动势的测定、原电池的最大功与Gibbs函数
7.3电极电势:介质的酸碱性、难溶化合物的形成、配合物的形成对电极电势的影响
7.4电极电势的应用:本节讲解稀溶液的依数性。
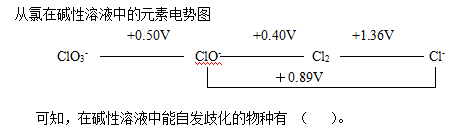 选项:[4种, 2种, 1种, 3种]
选项:[4种, 2种, 1种, 3种] [单选题]
向原电池(-)Zn|Zn2+(1mol·L-1)||Cu2+(1mol·L-1)|Cu(+)的正极溶液中通入H2S气体,则原
电池的电动势( )。
[单选题]下列氧化剂中,氧化性随溶液中氢离子浓度的增大而增强的是( )。
选项:[
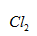 ,
, 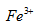 ,
, 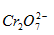 ,
, 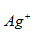 ]
][单选题]
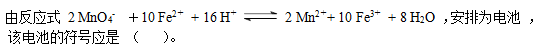 选项:[ Mn| MnO4- -,Mn2+, H+‖Fe2+ , Fe3+ |Fe , Pt| Fe2+(c1) , Fe3+(c2)‖MnO4- (c3) ,Mn2+(c4),H+ (c5)|Pt;, Fe| Fe2+ (c1), Fe3+(c2)‖MnO4- (c3),Mn2+(c4), H+(c5) |Mn;, Pt| MnO4- (c1) ,Mn2+(c2),H+(c3) ‖Fe2+(c4) , Fe3+(c5) |Pt;]
选项:[ Mn| MnO4- -,Mn2+, H+‖Fe2+ , Fe3+ |Fe , Pt| Fe2+(c1) , Fe3+(c2)‖MnO4- (c3) ,Mn2+(c4),H+ (c5)|Pt;, Fe| Fe2+ (c1), Fe3+(c2)‖MnO4- (c3),Mn2+(c4), H+(c5) |Mn;, Pt| MnO4- (c1) ,Mn2+(c2),H+(c3) ‖Fe2+(c4) , Fe3+(c5) |Pt;][单选题]能组成原电池的反应都是氧化还原反应。
选项:[错, 对]
[单选题]同种金属与其盐溶液也能组成原电池,其条件是两个半电池中离子浓度不同。
选项:[错, 对]
[单选题]因为H2O2 的氧处在中间价态,所以 H2O2 参与电极反应时,溶液的酸碱度与该电极反应毫无关系。
选项:[错, 对]
[单选题]氧化还原电对的标准电极电势越高,表示该电对的氧化态氧化还原能力越强。
选项:[对, 错]
[单选题]氧化还原反应达平衡时,标准电动势和标准平衡常数都为零。
选项:[对, 错]
[单选题]
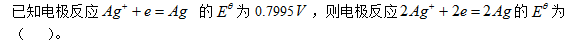 选项:[
选项:[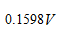 ,
, 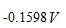 ,
, 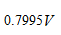 ,
, 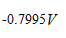 ]
][单选题]
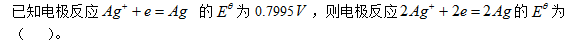 选项:[
选项:[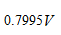 ,
, 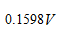 ,
, 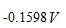 ,
, 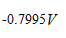 ]
][单选题]下列氧化剂中,氧化性随溶液中氢离子浓度的增大而增强的是( )。
选项:[
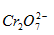 ,
, 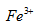 ,
, 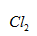 ,
, 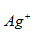 ]
][单选题]
向原电池(-)Zn|Zn2+(1mol·L-1)||Cu2+(1mol·L-1)|Cu(+)的正极溶液中通入H2S气体,则原
电池的电动势( )。
[单选题]
 选项:[3种, 4种, 2种, 1种]
选项:[3种, 4种, 2种, 1种][单选题]
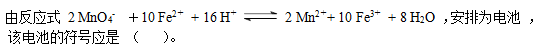 选项:[ Mn| MnO4- -,Mn2+, H+‖Fe2+ , Fe3+ |Fe , Fe| Fe2+ (c1), Fe3+(c2)‖MnO4- (c3),Mn2+(c4), H+(c5) |Mn;, Pt| MnO4- (c1) ,Mn2+(c2),H+(c3) ‖Fe2+(c4) , Fe3+(c5) |Pt;, Pt| Fe2+(c1) , Fe3+(c2)‖MnO4- (c3) ,Mn2+(c4),H+ (c5)|Pt;]
选项:[ Mn| MnO4- -,Mn2+, H+‖Fe2+ , Fe3+ |Fe , Fe| Fe2+ (c1), Fe3+(c2)‖MnO4- (c3),Mn2+(c4), H+(c5) |Mn;, Pt| MnO4- (c1) ,Mn2+(c2),H+(c3) ‖Fe2+(c4) , Fe3+(c5) |Pt;, Pt| Fe2+(c1) , Fe3+(c2)‖MnO4- (c3) ,Mn2+(c4),H+ (c5)|Pt;][单选题]能组成原电池的反应都是氧化还原反应。
选项:[对, 错]
[单选题]氧化还原电对的标准电极电势越高,表示该电对的氧化态氧化还原能力越强。
选项:[对, 错]
[单选题]氧化还原反应达平衡时,标准电动势和标准平衡常数都为零。
选项:[错, 对]
[单选题]同种金属与其盐溶液也能组成原电池,其条件是两个半电池中离子浓度不同。
选项:[错, 对]
[单选题]因为H2O2 的氧处在中间价态,所以 H2O2 参与电极反应时,溶液的酸碱度与该电极反应毫无关系。
选项:[对, 错]
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!