第六章单元测试
- 下列叙述中正确的是 ( )
- 第二周期各对元素的第一电离能大小次序如下,错误的是 ( )
- 多电子原子中,以下列量子数表征的电子,其能量最高的是( )
- 某元素最高能级组成电子构型
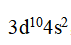 ,则该元素位于周期表( )
,则该元素位于周期表( ) - 下列各对元素中,性质最相似的是( )
- 电子在原子核外运动的能级越高,它与原子核的距离就越远。任何时候1s电子总比2s电子靠近原子核,因为
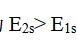 。( )
。( ) - 原子中某电子的各种波函数,代表了该电子可能存在的各种运动状态,每一种状态可视为一个轨道。( )
- 镧系收缩是由于随着原子序数的增加,镧系元素新增的电子填充在(n-2)f分层中,使有效核电荷数增加更为缓慢,从而造成原子半径减小的幅度更小。( )
- 某原子中,n= 4,l=2的轨道中电子最多可有10个。( )
- 电离能越小的金属元素,其金属性越弱。( )
A:2p轨道是哑铃形的,2p电子沿“∞”字轨道运动 B:n=2,l=1,m=0的原于轨道为
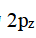 轨道
C:主量子数n=2时,只有2s和2p这两个原子轨道
D:氢原子核外只有一个电子,也只能有一个原子轨道
轨道
C:主量子数n=2时,只有2s和2p这两个原子轨道
D:氢原子核外只有一个电子,也只能有一个原子轨道答案:n=2,l=1,m=0的原于轨道为
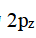 轨道
轨道A:F<Ne B:B<C C:Li< Be D:N<O
A:2,1,-1,+1/2 B:2,0,0,-1/2 C:3,2,-1,+1/2 D:3,1,1,+1/2
A:ds区 B:d区 C:p区 D:S区
A:Mg 和Al B:Co和Ni C:Nb和Ta D:Li和Mg
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
A:对 B:错
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!
