中国石油大学(华东)
- 冰在室温下自动融化成水,是熵增起了重要作用的结果。 ( )
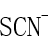 作为配体时,S可以作为配位原子,N也可以作为配位原子,因此
作为配体时,S可以作为配位原子,N也可以作为配位原子,因此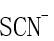 是多齿配体。( )
是多齿配体。( )- 根据酸碱质子理论,在
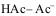 共轭酸碱对中HAc为弱酸,
共轭酸碱对中HAc为弱酸,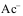 为强碱。( )
为强碱。( ) - 化学热力学中,标准状态条件是指压力为101.325 kPa,温度为298.15 K。( )
- https://image.zhihuishu.com/zhs/onlineexam/ansewerImg/202304/fe32df241b944e5eba9478d575fc3ac9.png
- 一般说来,分子间范德华力与分子大小有关,结构相似的情况下,分子越大,范德华力也越大。 ( )
- 核外电子的能量只与主量子数有关。 ( )
- 二元弱酸的的纯水溶液中负二价离子的浓度近似等于
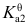 。( )
。( ) - AgCl和
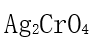 的溶度积分别为
的溶度积分别为 则AgCl的溶解度大于
则AgCl的溶解度大于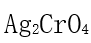 的溶解度。 ( )
的溶解度。 ( ) - 凡以
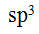 杂化轨道成键的分子,其分子构型必为正四面体。 ( )
杂化轨道成键的分子,其分子构型必为正四面体。 ( ) - 一个s轨道和3个p轨道,形成一个
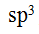 杂化轨道。 ( )
杂化轨道。 ( ) - 对不同类型的难溶电解质,不能认为溶度积大的在纯水中的溶解度也一定大。 ( )
- s电子与s电子间配对形成的共价键一定是σ键,而p电子与p电子间配对形成的共价键一定是π键。 ( )
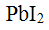 和
和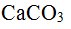 的溶度积均近似为
的溶度积均近似为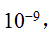 ,从而可知在它们的饱和溶液中,前者的
,从而可知在它们的饱和溶液中,前者的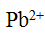 浓度与后者的
浓度与后者的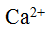 浓度近似相等。( )
浓度近似相等。( )- 因为Q、W不是系统所具有的性质,而与途径有关,所以热力学过程中(Q-W)的值也应由具体的途径决定。( )
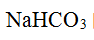 的热稳定性小于
的热稳定性小于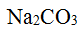 的热稳定性,其主要原因是H+的反极化作用强。 ( )
的热稳定性,其主要原因是H+的反极化作用强。 ( )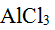 能与碳酸钠溶液作用,生成的沉淀能够溶于氢氧化钠溶液。 ( )
能与碳酸钠溶液作用,生成的沉淀能够溶于氢氧化钠溶液。 ( )- 配离子的电荷数等于中心体的电荷和配体电荷的代数和。 ( )
- 在SiC晶体中不存在独立的SiC分子。( )
- 15 K时,元素指定单质的
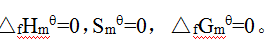 。( )
。( ) 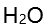 的沸点是100
的沸点是100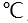 ,
,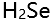 的沸点是-42
的沸点是-42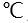 ,前者比后者高的主要原因是( )。
,前者比后者高的主要原因是( )。- 在温度T和压力p时理想气体反应:
(1)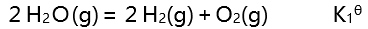
(2)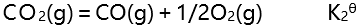
则反应(3):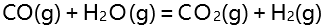 的
的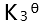 应为( )。
应为( )。 - 反应
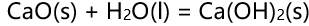 在298.15 K和标准态下是自发的,其逆反应在高温下变为自发进行的反应。那么正反应是( )。
在298.15 K和标准态下是自发的,其逆反应在高温下变为自发进行的反应。那么正反应是( )。 - 下列哪一种叙述不能解释温度对化学反应速率的影响( )
- 对于一个反应来说,下列说法中正确的是( )。
- 下列对于功和热的描述中,正确的是( )。
- 下列反应中,熵减少的是( )。
- 向含有KCl、KBr、
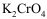 浓度均为0.01
浓度均为0.01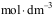 的溶液中逐滴加入0.01
的溶液中逐滴加入0.01 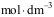 的
的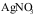 溶液时,最先和最后析出的沉淀分别是( )
溶液时,最先和最后析出的沉淀分别是( )
已知: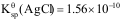 ,
,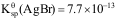 ,
,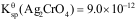
- 某温度下,反应
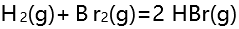 的标准平衡常数
的标准平衡常数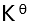 ,则反应
,则反应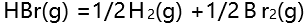 的标准平衡常数为( )。
的标准平衡常数为( )。 - 某温度,反应
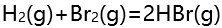 的标准平衡常数
的标准平衡常数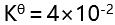 ,
,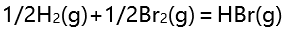 的标准平衡常数为( )。
的标准平衡常数为( )。 - 温度不变,向
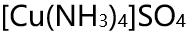 水溶液中继续通入氨气,以下说法正确的是( )。
水溶液中继续通入氨气,以下说法正确的是( )。 - 下述氧化物的水合物碱性最强的是( )。
- 下述关于离子的变形性描述正确的是( )。
- 将醋酸铵溶于烧杯中的水中,烧杯壁发冷,则该过程的
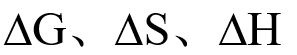 的符号依次是是( )。
的符号依次是是( )。 - 已知1g 的纯水在101325Pa下,当温度由287.7K升高1K后,吸热2.1 J得功2.1 J,则其内能的变化量为( )。
已知
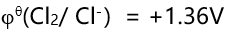 ,在下列电极反应中标准电极电势为+1.36V 的电极反应是( )。
,在下列电极反应中标准电极电势为+1.36V 的电极反应是( )。- 某元素的最高氧化数为+7,在同族元素中它的原子半径最小,该元素是( )。
- 已知反应
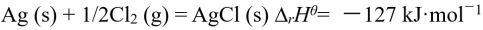 ,标准状态下,该反应能够正向自发进行的温度条件是( )。
,标准状态下,该反应能够正向自发进行的温度条件是( )。 - 已知难溶电解质
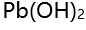 的
的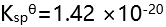 ,则其在纯水中的溶解度为( )。
,则其在纯水中的溶解度为( )。 - 已知
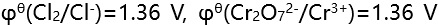
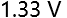 ,则在标准态下,反应
,则在标准态下,反应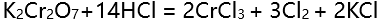 的方向为( )。
的方向为( )。 - 氮原子的2p能级电子分布为
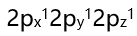 ,这样的排布方式遵循了( )。
,这样的排布方式遵循了( )。 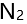 分子之间的作用力有( )。
分子之间的作用力有( )。- 已知反应在某温度下
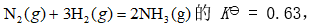 反应达到平衡时,在恒容条件下,若再通入一定量的
反应达到平衡时,在恒容条件下,若再通入一定量的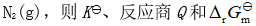 的关系是( )。
的关系是( )。 - 若某反应的
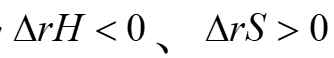 , 则其自发进行的条件是( )。
, 则其自发进行的条件是( )。 - 如果反应容器的体积增大为原来的2倍,则基元反应
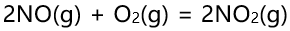 的速率将( )。
的速率将( )。 - 某元素原子的价电子构型为
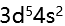 ,它的原子中未成对电子数为 ( )。
,它的原子中未成对电子数为 ( )。 - 在温度T的标准状态下,若已知反应A
 2B的标准反应焓变
2B的标准反应焓变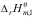 ,与反应2A
,与反应2A C的标准反应焓变
C的标准反应焓变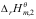 ,则反应C
,则反应C 4B的标准反应焓变
4B的标准反应焓变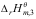 与
与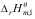 及
及 的关系为
的关系为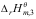 =( )。
=( )。 - 下述氧化物属于酸性氧化物的是( )。
- 无水
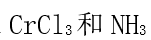 能形成配合物,若加
能形成配合物,若加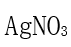 溶液只能从该配合物的水溶液中沉淀出 2/3 的
溶液只能从该配合物的水溶液中沉淀出 2/3 的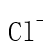 ,该配合物是( )。
,该配合物是( )。 - 在下列哪个原子轨道中的一个电子能量较高?( )
A:对 B:错
答案:对
A:错 B:对
答案:错
A:错 B:对
答案:对
A:错 B:对
答案:错
A:对 B:错
答案:
A:对 B:错
答案:对
A:对 B:错
答案:错
A:错 B:对
答案:对
A:对 B:错
答案:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:氢键 B:共价键 C:分子量 D:范德华力
A:
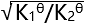 B:
B: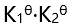 C:
C: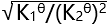 D:
D: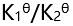
A:
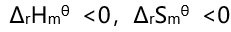 B:
B: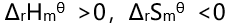 C:
C: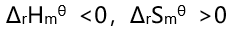 D:
D: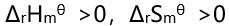
A:升高温度,使较多的分子获得能量而成为活化分子,增加了活化分子百分数,加快了反应速率 B:升高温度,使活化分子百分数增加,加快了反应速率 C:升高温度,改变了反应的历程而降低了反应的活化能,加快了反应速率 D:升高温度,使分子间碰撞次数增加,加快了反应速率
A:活化能越小,反应速率越快 B:活化能越大,反应速率越快 C:
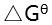 越负,反应速率越快
D:
越负,反应速率越快
D: 越负,反应速率越快
越负,反应速率越快
A:都是状态函数,始终态确定,其值也确定 B:都是过程函数,对应于某一状态有一确定的数值 C:都是过程函数 D:都是状态函数,变化量与途径无关
A:
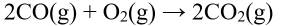 B:
B: C:
C: D:
D: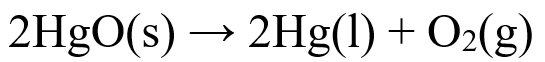
A:AgBr,
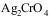 B:AgBr,AgCl
C:AgCl,
B:AgBr,AgCl
C:AgCl,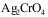 D:
D: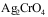 ,AgCl
,AgCl
A:
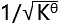 B:
B: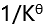 C:
C: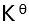 D:
D: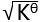
A:5 B:
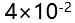 C:
C: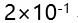 D:25
D:25
A:
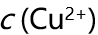 减小
B:
减小
B: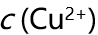 增大
C:
增大
C: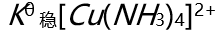 增大
D:
增大
D: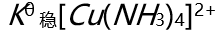 变小
变小
A:
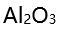 B:MgO
C:
B:MgO
C: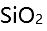 D:
D: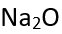
A:
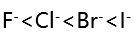 B:
B: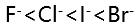 C:
C: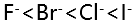 D:
D: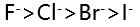
A:负,正,正 B:正,正,负 C:负,正,负 D:正,负,负
A:4.2 J B:-4.2 J C:无法确定 D:0 J
A:
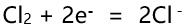 B:
B: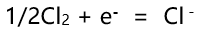 C:其他都是
D:
C:其他都是
D: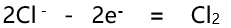
A:Cr B:Mn C:Cl D:Cu
A:
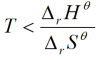 B:任何温度均可自发
C:
B:任何温度均可自发
C: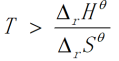 D:任何温度均不可自发
D:任何温度均不可自发
A:
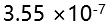 B:
B: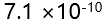 C:
C: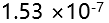 D:
D: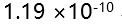
A:正反应自发 B:逆反应自发 C:无法确定 D:平衡状态
A:能量最低原理 B:泡利不相容原理 C:洪特规则特例 D:洪特规则
A:取向力 B:诱导力 C:色散力 D:氢键
A:
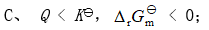 B:
B: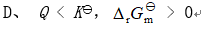 C:
C: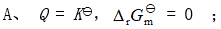 D:
D: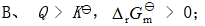
A:高温自发 B:任意温度都自发 C:低温自发 D:任意温度都非自发
A:增大为原来的 8 倍 B:减小为原来的 1/8 C:增大为原来的 4 倍 D:减小为原来的 1/4
A:5 B:1 C:3 D:0
A:2
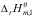 +
+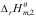 B:2
B:2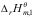 -
-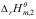 C:
C: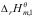 -2
-2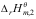 D:
D: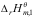 +
+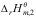
A:CaO B:
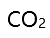 C:MgO
D:AgO
C:MgO
D:AgO
A:
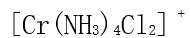 B:
B: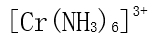 C:无法判断
D:
C:无法判断
D: 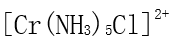
A:
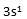 B:
B: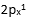 C:
C: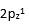 D:
D: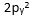
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!


