浙江工业大学
- 合成氨反应中,硫化氢对铁催化剂的中毒是可逆中毒。( )
- n型半导体有利于氧的吸附,可用于加氢、脱氢及选择性氧化反应。( )
- 对同一类型的沸石分子筛通过离子交换也可以改变其孔口大小。( )
- TOF指单位时间内每个活性中心上转换反应物分子的数量。( )
- 活性位是在催化剂中真正起催化作用的那部分原子或原子基团。( )
- 能提供质子的为B酸。( )
- 过渡金属氧化物催化剂在催化氧化反应过程当中,特别是对烃类氧化反应中,反应产物中的氧往往不是直接来自气相中的氧,而是来自金属氧化物中的晶格氧。( )
- 将低硅沸石通过脱铝提高其硅铝比,可以提高分子筛的酸性。( )
- 络合催化中的18规则是指中心离子(或原子)的d电子数越多,其配位体数越少。其中以总价电子数为18的络合物最为稳定。( )
- 负载金属催化剂在高分散时金属的物理化学特性可能发生变化。( )
- 催化剂的稳定性是指催化剂在使用条件下具有稳定活性的时间。( )
- 化学吸附是单层吸附。( )
- 吸附碱的红外光谱(IR)法可以判断酸中心的类型。( )
- 烷烃与L酸中心反应可以生成正碳离子中间体。( )
- 能接受电子对的为L碱。( )
- 酸碱理论分为( )。
- 下列选项中影响CO不同吸附态因素的有( )
- 化学吸附时,双方电子重新分配的结果可能( )
- 煅烧过程可以使催化剂( )
- 催化剂的稳定性包括( )。
- 助催化剂按功能可分为( )。
- 以下可以生成p型半导体的方法有( )
- 下列具有催化氧化性的分子筛有( )
- 吸附热随覆盖度增大而下降的原因( )
- 分子筛择形催化的形式有( )
- 催化剂在催化反应时能够 ( )
- 沉淀法制备催化剂过程中,主要影响因素有( )
- 对p型半导体加入施主型杂质后,( )
- 助催化剂( )
- 金属催化剂的特性有哪些( )
- 下列哪一个因素与毒物分子在催化剂表面上的覆盖程度即覆盖因子关系不大( )
- 在用压汞法测孔结构时( )
- 下列哪种制备方法是控制均匀沉淀的有效方法( )
- 下列描述错误的是( )
- 以下表述正确的是( )
- 对n型半导体加入受主型杂质后,( )
- 关于过渡金属氧化物的电子性质描述不正确的是( )
- 下列哪种物质属于本征半导体( )。
- 用浸渍法制备
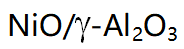 催化剂时,当焙烧温度为500-600℃,会发生( )
催化剂时,当焙烧温度为500-600℃,会发生( ) - 原子轨道通过线性组合成分子轨道时,( )
- 络合催化过程中的活化方式之一的氧化加成使中心金属离子发生( )。
- 加氢变环己烷反应所使用的催化剂是( )
- 合成氨反应混合气中,水蒸汽与硫化氢会使铁催化剂的中毒,其中( )
- MgO载体是( )
- 对n型半导体加入施主型杂质后,( )
- 下列哪一种物质在过渡金属上的化学吸附最强( )
- 在沉淀法制备窄分布的大颗粒催化剂时,要控制( )
- 以下不属于n型半导体生成方法的是( )
- 对氮气有化学吸附作用的金属是( )
- 下列不属于n型半导体的是( )。
A:错 B:对
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:A: 错
A:对 B:错
答案:对
A:对 B:错
答案:A: 对
A:错 B:对
答案:B: 对
A:错 B:对
答案:A: 错
A:对 B:错
答案:对
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:酸碱质子理论
B:软硬酸碱理论
C:酸碱电离理论
D:酸碱电子理论
A:覆盖度
B:温度和压力
C:金属的类别
D:浓度
A:共享电子,组成共价键
B:电负性差别较小,形成共价键
C:电负性略有差别,形成极性键
D:电负性差别较大,组成离子键
A:失去化学键合的水或二氧化碳
B:改变孔径分布
C:调整固体表面,使达到所要求的状态
D:形成活性相
A:抗毒稳定性
B:化学稳定性
C:耐热稳定性
D:机械稳定性
A:调变型助催化剂
B:扩散型助催化剂
C:结构型助催化剂
D:毒化型助催化剂
A:含有过量金属原子的非化学计量化合物
B:向氧化物晶格间隙掺入电负性大的杂质原子
C:含有正离子缺位的非化学计量化合物
D:用低价正离子取代晶格中的正离子
A:A型分子筛
B:TS-1 分子筛
C:X型分子筛
D:ZSM-5 分子筛
A:表面不均匀性
B:吸附物种之间的相互作用
C:使用固体中不同的电子能级
D:活性位数量的减少
A:分子交通控制的择形催化
B:过渡状态限制的择形催化
C:反应物的择形催化
D:产物的择形催化
A:降低反应活化能,改变热力学平衡常数
B:降低反应活化能,改变反应历程
C:加快正向反应速度,降低逆向反应速度
D:缩短达到反应平衡所需要的时间
A:温度
B:搅拌
C:浓度
D:pH值
A:费米能级升高
B:更难给出电子
C:逸出功降低
D:电导率变大
A:可以改变活性组分的电子效应
B:可以提高载体的稳定性
C:本身对某一反应有很好的活性
D:加入的量一般小于催化剂总量的10%
A:对双原子分子,容易进行解离吸附,从而进行各类反应
B:由于吸附中心的多样性,也就造成竞争反应的同时发生,降低了金属催化剂的选择性
C:金属催化剂通常是以金属晶体的形式存在,而且具有多种晶体结构,由此也为化学吸附提供多种吸附中心
D:由于这些中心相互靠近,有利于被吸附物种相互作用而进行反应
A:物分子在空间运动占有的有效体积
B:毒物分子的物理吸附能力
C:毒物分子的性质
D:毒物分子的结构
A:样品孔半径越大,所需汞压越大
B:样品孔半径越小,所需汞压越小
C:样品孔半径越大,所需汞压越小
D:样品孔半径与所需汞压无关
A:在金属盐溶液中加
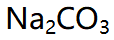 作沉淀剂
作沉淀剂B:在金属盐溶液中加醋酸作沉淀剂
C:在金属盐溶液中加尿素作沉淀剂并加热
D:在金属盐溶液中加NaOH作沉淀剂
A:当一个轨道已被一个电子占据,若要将第二个电子填入此轨道并与之配对时,克服的排斥作用需要的能量为电子成对能
B:过渡金属络合物的催化与过渡金属的d电子状态无关
C:配位体将孤对电子配位到络合物中心离子的空轨道中,形成的化学键为配价键
D:不同几何构型的配合物,中心金属离子用于形成σ配键和π配键的d轨道是不同的,由轨道对称性来决定
A:电子配对能的影响是使电子尽可能分占不同d轨道,并保持自旋平行
B:电子配对能的影响是使电子优先占据能量较低的轨道
C:分离能的影响是使电子尽可能分占不同d轨道,并保持自旋平行
D:分离能的影响是使电子优先占据能量较高的轨道
A:电导率变小
B:逸出功降低
C:更容易给出电子
D:费米能级升高
A:过渡金属氧化物与过渡金属都可作为氧化还原反应催化剂,而前者由于其耐热性、抗毒性强,而且具有光敏、热敏、杂质敏感性,更有利于催化剂性能调变,因此应用更加广泛
B:过渡金属氧化物中金属离子的内层价轨道与外来轨道作用不会发生劈裂
C:过渡金属氧化物中的金属阳离子的d电子层容易失去电子或夺取电子,具有较强的氧化还原性能
D:过渡金属氧化物具有半导体性质
A:单晶硅
B:MgO
C:NiO
D:
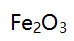
A:
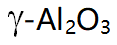 的晶相转变
的晶相转变B:NiO的挥发损失
C:
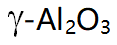 孔结构破坏
孔结构破坏D:NiO与
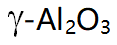 固态反应生成
固态反应生成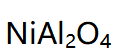
A:轨道能级改变
B:能级低于原子轨道的称为成键轨道
C:轨道数目改变
D:能级高于原子轨道的称为成键轨道
A:配位数不变,氧化态不变
B:二者都减小
C:配位数增加,氧化态增加
D:配位数增加,氧化态减小
A:
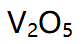
B:CuO
C:
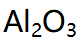
D:
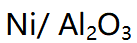
A:水蒸汽是不可逆中毒,硫化氢是可逆中毒
B:两者皆为可逆中毒
C:两者皆为不可逆中毒
D:水蒸汽是可逆中毒,硫化氢是不可逆中毒
A:酸性载体
B:两性载体
C:碱性载体
D:中性载体
A:电导率变小
B:逸出功升高
C:更难给出电子
D:费米能级升高
A:直链烷烃
B:环烷烃
C:炔烃
D:烯烃
A:长大速率比成核速率快
B:长大速率与成核速率相当
C:长大速率比成核速率慢
D:与成核速率和长大速率无关
A:含有过量金属原子的非化学计量化合物
B:含有正离子缺位的非化学计量化合物
C:用高价正离子取代晶格中的正离子
D:向氧化物晶格间隙掺入电负性小的杂质原子
A:Fe
B:Ag
C:Mn
D:Na
A:ZnO
B:
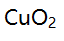
C:CuO
D:NiO
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!

