第六章测试1.
在标准条件下,下列反应均向正方向进行:
Cr2O72- +6Fe2+ +14H+ = 2Cr3+ +6Fe3+ +7H2O
2Fe3+ +Sn2+ = 2Fe2+ +Sn4+
他们中间最强的氧化剂和最强的还原剂是 ()
A:Cr2O72-和Fe3+ B:Sn2+和Fe3+ C:Cr3+和Sn4+ D:Cr2O72-和Sn2+
答案:D
2.
对于反应 Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,其ΔrGm=–nFE,式中n等于()
A:1 B:12 C:6 D:3 3.
25℃时,将铂丝插入含有Sn4+ 和Sn2+ 离子浓度分别为0.1和0.01mol·L-1 的溶液中,电对的电极电位为()
A:
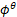 +0.0592
B:
+0.0592
B: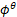 -0.0592
C:
-0.0592
C: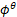 +0.0592/2
D:
+0.0592/2
D: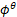 -0.0592/2
E:
-0.0592/2
E: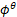 4.
4.已知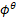 MnO4-/Mn2+=1.49V,若其他物质均处于标态,当pH=2时,此电对的电极电位是
MnO4-/Mn2+=1.49V,若其他物质均处于标态,当pH=2时,此电对的电极电位是
A:1.50V B:1.03V C:0.89V D:1.30V E:1.39V 5.
某氧化还原反应的标准电动势Eθ>0,则应有
A:ΔrGmθ<0,Kθ<1 B:ΔrGmθ<0,Kθ>1 C:ΔrGmθ>0,Kθ>1 D:ΔrGmθ>0,Kθ<1 6.
知原电池中两电极的标准电极电位值,就能判断该电池自发进行的方向。
A:对 B:错 7.
电池标准电动势越大,氧化还原能力越大,反应速率越快。
A:错 B:对 8.
标准电极电位和标准平衡常数一样,都与反应方程式的化学计量系数有关。
A:对 B:错 9.
两电对组成原电池,标准电极电位大的电对中的氧化型物质在电池反应中一定是氧化剂。
A:错 B:对 10.
往银电极中加入一定量的氯化钠,电极电位降低。
A:错 B:对
温馨提示支付 ¥4.99 元后可查看付费内容,请先翻页预览!







