提示:内容已经过期谨慎付费,点击上方查看最新答案
物理化学(下)(湖南科技大学)
- 根据DLVO理论,溶胶相对稳定的主要因素是: ( )
- 下列溶液中哪个溶液的摩尔电导最大: ( )
- 选取速率控制步骤、稳态近似与平衡态近似分别应用于:( )
- 阿伦尼乌斯活化能与阈值的关系正确的是?( )
- 反应
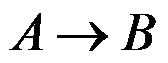 ,开始时反应系统中只有反应物
,开始时反应系统中只有反应物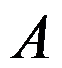 ,若
,若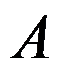 完全转化为
完全转化为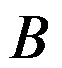 所需时间为
所需时间为 ,而该反应的半衰期为
,而该反应的半衰期为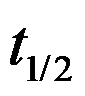 ,测得
,测得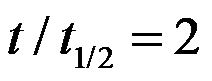 ,则此反应的级数为:( )
,则此反应的级数为:( ) - 胶束的出现标志着表面活性剂的: ( )
- 当一反应物的初始浓度为 0.04
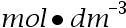 时,反应的半衰期为 360 s,初始浓度 为 0.024
时,反应的半衰期为 360 s,初始浓度 为 0.024 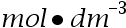 时,半衰期为 600 s,此反应为:( )
时,半衰期为 600 s,此反应为:( ) - 一个化学系统吸收光子之后,将引起下列哪种过程? ( )
- 有两个电池如下所示,电动势分别为
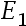 和
和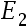 :
: 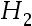 (p)│
(p)│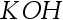 (0.1 mol/kg)│
(0.1 mol/kg)│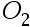 (p)和
(p)和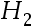 (p)│
(p)│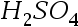 (0.0l mol/kg)│
(0.0l mol/kg)│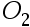 (p) 比较其电动势大小: ( )
(p) 比较其电动势大小: ( ) - 一根毛细管插入水中,液面上升的高度为h,当在水中加入少量的NaCl,这时毛细管中液面的高度为:( )
- 已知空气中的某一肥皂泡半径为r,如果肥皂水溶液的表面张力为γ, 则肥皂泡内的附加压力ΔP应为:( )
- 下列说法不正确的是?( )
- 下列物质在水中产生正吸附的是:( )
- 工业上为了将不同蛋白质分子分离,通常采用的方法是利用溶胶性质中的: ( )
- 某反应,当反应物反应掉5/9所需时间是它反应掉1/3所需时间的2倍,则该反应是:( )
- 对由各种方法制备的溶胶进行半透膜渗析和电渗析的目的是 ( )
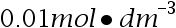 的下列各溶液中,电导率最大的是 ( )
的下列各溶液中,电导率最大的是 ( )- 丁铎尔现象是光射到粒子上发生下列哪种现象的结果?( )
- 有机液体与水形成W/O型还是O/W型乳状液与乳化剂的HLB值有关,一般是:( )
- 某反应速率常数与各基元反应速率常数的关系为
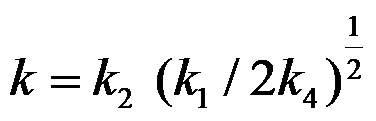 ,则该反应的表观活化能Ea与各基元反应活化能的关系为:( )
,则该反应的表观活化能Ea与各基元反应活化能的关系为:( ) - 当一定的直流电通过一电解质溶液时,在阴极上析出金属的量正比于:( )
- 在一个密闭的容器中,有大小不同的两个水珠,长期放置后会发生: ( )
- 反应A+B→C+D的活化能Ea=30
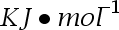 。在500K下,升高温度1K时,反应速率常数增加的倍数为n1;若同一反应在1000K下,升高温度1K时,反应速率常数增加的倍数为
。在500K下,升高温度1K时,反应速率常数增加的倍数为n1;若同一反应在1000K下,升高温度1K时,反应速率常数增加的倍数为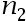 。那么
。那么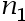 与
与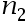 之间的大小关系为:( )
之间的大小关系为:( ) - 使用同一电导池分别测定浓度为
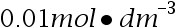 和
和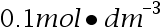 的两种不同电解质溶液,其电阻分别为1000 Ω与500 Ω,则它们的摩尔电导率之比是:( )
的两种不同电解质溶液,其电阻分别为1000 Ω与500 Ω,则它们的摩尔电导率之比是:( ) - 下列哪种反应类型不是复合反应?( )
- 下列有关催化剂性质的说法, 不正确的是 ( )
- 在电池中,当电池反应达到平衡时,电池的电动势等于 ( )
- 纯水的表面张力是指恒温恒压组成时水与哪类相接触时的界面张力: ( )
- 溶胶中的胶体粒子处在等电态,是指该胶粒处于的状态是:( )
- 有关电导率和摩尔电导率的说法正确的是?( )
- 对于物理吸附,下列哪一条描述不正确 ( )
- 下列电解质溶液中,离子平均活度系数最大的是: ( )
- 当电池中有电流通过时,随着电流密度增大, ( )
- 在溶胶的下列现象中,哪一个与光的散射作用有关? ( )
- 固液界面的接触角是指:( )
- 涉及溶液表面吸附的说法中正确的是: ( )
- 表面活性物质加入到溶液中,则会发生下列哪种变化?( )
- 电动势与温度的关系为:
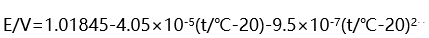 , 298 K时电池可逆放电,则:( )
, 298 K时电池可逆放电,则:( ) - 下面关于催化剂的叙述中, 哪一点是不正确的?( )
- 对于反应A→P, 如果反应的半衰期与A的初始浓度无关, 则该反应为 ( )
- 某反应在一定条件下平衡的转化率为25%,当有催化剂存在时,其转化率应当。( )
- 相同温度下,无限稀时HCl、KCl、
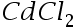 三种溶液,下列说法中不正确的是 ( )
三种溶液,下列说法中不正确的是 ( ) - 对于气相基元反应,下列条件:①温度降低②活化熵越负③活化焓越负④分子有效碰撞直径越大。能使反应速率变大的条件是:( )
- 下面说法与DLVO理论不符的是: ( )
- 对于基元反应,几分子反应就是几级反应。( )
外压和温度相同时,微小液滴的蒸气压比平面液体的蒸气压小。
- 零级反应的半衰期与初始反应物的初始浓度成正比,一级反应的半衰期与初始浓度无关,二级反应的半衰期与初始浓度成反比。( )
A:布朗运动使胶粒很难聚结 B:离子氛重叠时产生的电性斥力占优势 C:胶粒表面存在双电层结构 D:胶粒和分散介质运动时产生ζ电位
答案:离子氛重叠时产生的电性斥力占优势
A:0.001 mol/L的KCl水溶液 B:0.0001 mol/L的KCl水溶液 C:0.1 mol/L的KCl水溶液 D:0.01 mol/L的KCl水溶液
答案:0.001MHCl水溶液
A:反应最快步、中间产物的浓度不变、决速步前有快平衡反应 B:反应最快步、中间产物的浓度变化率为零、有快平衡反应 C:反应最慢步、中间产物的浓度变化率为零、决速步前有快平衡反应 D:反应最慢步、中间产物的浓度不变、决速步前有快平衡反应
AI参考:正确选项是D:反应最慢步、中间产物的浓度不变、决速步前有快平衡反应。选取速率控制步骤时,通常选择反应最慢的步骤作为速率控制步骤,这样可以更准确地反映反应速率。在中间产物浓度不变的情况下,可以忽略中间产物对反应速率的影响,从而简化模型。决速步前有快平衡反应是指反应物首先在快平衡状态下发生反应,这个步骤对反应速率的影响较小,因此可以忽略不计。因此,这三个步骤可以应用于反应最慢步、中间产物的浓度不变、决速步前有快平衡反应的情况。'
A:Ea=Ec-0.5RT B:Ea=Ec+0.5RT C:Ea=Ec+RT D:Ea=Ec-RT
答案:Ea=Ec+0.5RT
A:零级 B:二级 C:3/2级 D:一级
AI参考:答案:D推理过程:反应级数是指反应速率与浓度的关系,一般用r表示,其表达式为r=k[C]^m由题意可知,该反应的反应速率与反应物浓度的乘积成正比,即r=k[A][B][C]又因为该反应的半衰期为一级反应,所以该反应为一级反应。因此,答案为D。注:该题中的图片文件无法正常打开,所以无法给出图片中所示的反应方程式。'
A:降低表面张力的作用下降 B:溶解已达到饱和 C:分子间作用超过它与溶剂的作用 D:分子远未排满溶液表面
答案:降低表面张力的作用下降
A:1 级反应 B:2 级反应 C:1.5 级反应 D:0级反应
答案:2 级反应
A:过程不能确定 B:引起光化学反应 C:产生荧光或磷光 D:发生无辐射跃迁
A:< B:= C:不能确定 D:>
AI参考:正确答案是A。由于图中所表示的是两个电池符号及连接方式的图片,并不能明确得知其物质,也就无法通过摩尔电导率来进行比较。在这种情况下,比较两个电动势大小就只能凭直观的感受或简单的规律来分析,图中给出的是一个A>一个B,所以选A。这个题目看似简单,但是确实很容易让人出错。我们在处理这样的题目时,一定要细心观察图片中的信息,明确题目的要求,再进行分析和判断。'
A:小于h B:大于h C:无法确定 D:等于h
A:ΔP=γ/2r B:ΔP=γ/4r C:ΔP=4γ/r D:ΔP=2γ/r
A:电导为电阻的倒数,可以通过测得电阻来测定导体的电导 B:对于一个制作好的电导池,其电极的横截面积与长度的比值为定值,称为电导池常数 C:电解质溶液的电导一般采用高频交流电源测定 D:电导率与电阻率也互为倒数,电阻率越大,电导率越小
A:蔗糖 B:氢氧化钠 C:油酸钠(十八烯酸钠) D:食盐
A:扩散 B:电泳 C:电渗 D:沉降
A:零级反应 B:一级反应 C:二级反应 D:3/2 级反应
A:除去过多的电解质离子,提高稳定性 B:除去小胶粒,提高均匀性 C:除去杂质,提高纯度 D:除去过多的溶剂,提高浓度
A:NaCl溶液 B:HCl溶液 C:CHCOOH溶液 D:NaAc溶液
AI参考:【单选题】
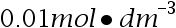 的下列各溶液中,电导率最大的是(B:HCl溶液)。电导率是衡量物质导电能力的指数,数值越大,导电能力越强。对于电解质溶液,离子浓度越大,电导率越大。HCl是强电解质,在水中完全电离,生成氢离子和氯离子,因此其电导率最大。而NaCl溶液、CHCOOH溶液、NaAc溶液都是电解质溶液,但是其电离程度不如HCl,因此电导率相对较小。因此答案为B。'
的下列各溶液中,电导率最大的是(B:HCl溶液)。电导率是衡量物质导电能力的指数,数值越大,导电能力越强。对于电解质溶液,离子浓度越大,电导率越大。HCl是强电解质,在水中完全电离,生成氢离子和氯离子,因此其电导率最大。而NaCl溶液、CHCOOH溶液、NaAc溶液都是电解质溶液,但是其电离程度不如HCl,因此电导率相对较小。因此答案为B。'A:折射 B:散射 C:反射 D:透射
A:HLB值小,不易形成W/O型 B:HLB值大,易形成O/W型 C:HLB值大,易形成W/O型 D:HLB值小,易形成O/W型
A:Ea= E2 +1/2(E1- E4) B:Ea= E2 + (E1- 2E4)1/2 C:Ea= E2 + E1- E4 D:Ea=E2 +1/2E1 - E4
AI参考:单选题答案为【B】某反应速率常数与各基元反应速率常数的关系为已知反应,则该反应的表观活化能Ea与各基元反应活化能的关系为Ea= E2 + (E1- 2E4)1/2。这个结论是在基元反应速率公式的基础上,通过将速率常数相加得到的。具体来说,对于基元反应1的反应速率公式为r1 = k1A1,其中k1是速率常数,A1是反应物浓度。对于整个反应,反应速率r = kA,其中k是表观速率常数,A是反应混合物的总体浓度。因此,k = k1 + k2 + ... + kn,其中ki是基元反应i的速率常数。根据这个关系式,可以得出表观活化能Ea的计算公式:Ea = E2 + (E1 - 2*ki2)。根据这个公式,基元反应i的速率常数ki已经由题目所给的值代入计算。最终结果就是Ea= E2 + (E1- 2E4)1/2。其他选项的公式都是错误的,因为题目中并没有给出任何信息表明反应是基元反应的总和。所以选择B选项。'
A:电解质溶液的温度 B:阴极的表面积 C:电解质溶液的浓度 D:通过的电量
AI参考:当一定的直流电通过一电解质溶液时,在阴极上析出金属的量正比于通过的电量。因此,正确答案是D。在其他条件相同的情况下,通过的电量越多,阴极上析出的金属量也越多。电解质溶液的温度、阴极的表面积和电解质溶液的浓度可能会影响金属的析出过程,但并不是决定性的因素。'
A:大水珠变小,小水珠变大 B:大水珠,小水珠均变小 C:大水珠变大,小水珠变大 D:大水珠变大,小水珠变小
A:大 B:无法确定 C:大 D:两者相等
A:5:1 B:1:5 C:1:20 D:20:1
AI参考:正确答案是C:1:20。根据摩尔电导率定义式:摩尔电导率 = 电阻值 / (电解质的摩尔浓度 × 体积),可知摩尔电导率与电阻值成反比,与电解质的摩尔浓度成正比。因此,浓度不同的两种电解质溶液,它们的摩尔电导率之比等于它们的电阻之比除以它们的摩尔浓度之比。已知两种溶液的电阻分别为1000Ω和500Ω,摩尔浓度未知,因此它们的摩尔电导率之比为1:20。'
A:连串反应 B:平行反应 C:基元反应 D:对行反应
AI参考:正确答案是B:平行反应。平行反应是一种独立的化学反应,与其他的复合反应类型(连串反应、基元反应、对行反应)没有必然联系,因此不属于复合反应类型。其他选项A、C、D都是复合反应类型。'
A:催化剂可改变反应的平衡常数 B:催化剂可降低反应的表观活化能 C:催化剂在反应前后化学性质不变 D:催化剂有特殊的选择性
A:TΔS B:零 C:ΔH D:–zEF
A:饱和了水蒸气的空气 B:饱和水蒸气 C:空气 D:含有水蒸气的空气
A:热力学电势为零 B:斯特恩电势为零 C:ξ电势为零 D:无法判断的状态
AI参考:正确答案是C:ξ电势为零。溶胶中的胶体粒子处在等电态,是指该胶粒处于的状态是ξ电势为零。等电状态意味着胶粒的电位为零,此时胶粒的扩散层最厚,稳定性最大。因此,C选项是正确答案。A、B、D选项都不正确,因为热力学电势、斯特恩电势和电位等概念与胶体等电状态无关。'
A:摩尔电导率是指相距1米,横截面积为1平方米的两个电极之间充满1mol电解质时溶液的电导 B:电导率是指单位立方体溶液的电导 C:摩尔电导率是指电解质溶液浓度为1mol/L时单位立方体溶液的电导 D:电导率是指电解质溶液浓度为1mol/L时单位立方体溶液的电导
A:吸附可以是单分子或多分子层 B:吸附力来源于范德华力 C:吸附热较小 D:吸附速率较小
AI参考:对于物理吸附,下列哪一条描述不正确 ( B:吸附力来源于范德华力)。物理吸附是由分子间范德华力所造成的表面层的分子排列有序化而产生的吸附。它属于较弱的吸引力吸附,吸附热较小,吸附速率也较小。因此,描述中不正确的选项是B,吸附力来源于范德华力。'
A:0.01 mol/kg NaCl B:0.01 mol/kg CuSO4 C:0.01 mol/kg LaCl3 D:0.01 mol/kg CaCl2
A:阳极电极电势和阴极电极电势都降低; B:阴极电极电势升高,阳极电极电势降低; C:阳极电极电势升高,阴极电极电势降低; D:阳极电极电势和阴极电极电势都升高;
A:沉降平衡 B:丁铎尔效应 C:布郎运动 D:电泳
A:g-l界面经过液体至s-l界面间的夹角 B:g-s界面经过固相至s-l界面间的夹角 C:l-g界面经过气相和固相至s-l界面间的夹角 D:g-l界面经过气相至g-s界面间的夹角
AI参考:选项B是正确的。接触角是指液体在固体表面形成的液-固界面与固-液界面间的夹角。在固液界面上,液体铺展在固体表面时,接触角为零;液体润湿固体时,接触角较小;而当液体不能润湿固体时,接触角较大。因此,固液界面的接触角是描述固液两相界面之间相互作用的一个重要参数。选项A中的g-l界面是指固-液界面,而题目中提到的固液界面是g-s界面,因此不正确。选项C中的l-g界面是指气-液界面,与题目中的固液界面无关。选项D中的g-l界面是指固-气界面,也不符合题目要求。因此,选项B是正确的答案。'
A:溶液表面发生吸附后表面自由能增加 B:饱和溶液的表面不会发生吸附现象 C:定温下表面张力不随浓度变化时,浓度增大,吸附量不变 D:溶液的表面张力一定小于溶剂的表面张力
A:溶液的, B:溶液的, C:溶液的, D:溶液的,
AI参考:正确选项是C:溶液的。表面活性物质加入到溶液中,会导致溶液的表面张力减小,从而使溶液变得更稀薄。这是由于表面活性物质具有降低表面张力的特性,因此将其加入到溶液中可以改变溶液的性质。选项A、B、D都与题目描述不符。'
A:Q > 0 B:Q = 0 C:不能确定 D:Q < 0
A:催化剂能加速反应但不参与反应 B:催化剂可以降低反应的活化能 C:催化剂不影响反应的平衡常数 D:催化剂只能加速热力学上可行的反应
AI参考:正确答案是A:催化剂能加速反应但不参与反应。催化剂在化学反应中能改变反应的速率,但是它本身在反应前后质量和化学性质都不变,并不参与反应。因此选项A是不正确的。选项B、C、D都是关于催化剂的正确叙述。'
A:二级反应 B:零级反应 C:一级反应 D:三级反应
AI参考:选项 C 一级反应是正确的。解释:题目中提到反应的半衰期与A的初始浓度无关,这意味着反应速率与初始浓度成正比,即反应速率与初始浓度的平方根成正比。这种反应类型符合一级反应的定义,即反应速率与初始浓度的一次方成正比。因此,选项C是一级反应,是正确的答案。'
A:大于25% B:不能确定 C:等于25% D:小于25%
A:离子的迁移数相同 B:离子的淌度相同 C:离子的迁移速率不一定相同 D:离子的摩尔导电率相同
A:③④ B:①④ C:①②④ D:②④
A:胶粒间的斥力本质上是所有分子范德华力的总和 B:溶胶是否稳定决定于胶粒间吸引作用和排斥作用的总效应 C:胶粒间的斥力本质上是双电层的电性斥力 D:胶粒周围存在离子氛,离子氛重叠越大,胶粒越不稳定
A:错 B:对
A:错 B:对
A:对 B:错
AI参考:答案是B:错。零级反应的半衰期与初始反应物的初始浓度无关,一级反应的半衰期与初始浓度成正比,二级反应的半衰期与初始浓度成正比。因此,这个说法是错误的。'
温馨提示支付 ¥1.80 元后可查看付费内容,请先翻页预览!

