山东第一医科大学
- 自由基是带有孤对电子的原子或基团。
- 如果确定了一个有机化合物的分子式,那么它的结构也就可以确定了。
- 烯烃和炔烃都能发生亲电加成和亲核加成反应。
- 烷烃按系统命名法命名时,主链一般选择支链数最多的碳链。
- 在氨水中加入氯化铵时,溶液的pH将降低
- 顺反异构体的物理性质和生理活性一般都不同。
- Z-E构型命名法与顺反构型命名法之间没有必然的联系。
- 醇醛缩合是指在稀碱条件下,醇与醛的缩合反应。
- 共轭效应包括p-π、π-π共轭效应。
- 炔烃的两个碳原子周围存在两对pi电子,电子云密度比烯烃碳原子要高,所以更易与亲电试剂发生反应。
- 氢键是一种特别强的分子间作用力,对物质的物理性质,化学性质及几何形状都有一定的影响。
- 对于脱水反应,2-丁醇脱水的主要产物是1-丁烯。
- 苦味酸就是2,4,6-三硝基苯酚,其酸性强于苯酚。
- 极性分子一定由极性共价键形成,非极性分子一定由非极性共价键形成。
- 顺-2-丁烯在质子酸催化下可以发生构型转化,生成反-2-丁烯。
- 乙醇可以和金属钠发生反应,产物为乙醇钠和氢气,该反应比钠与水的反应剧烈。
- 含有对称因素的分子,虽然含有手性C原子但是没有手性。
- 关于几种有机化合物酸性从强到弱的顺序为:苯酚>水>乙醇。
- 如何除去醚中的过氧化物( )
- 下列物质中,与乙醇能形成较强氢键作用的化合物有哪些?
- 下述羧酸中,哪些是自然界广泛存在的?
- 因为胶体的性质而产生的现象是( )
- 下列化合物中,能与三氯化铁溶液显色( )
- 下列属于不溶液的是( )
- 下列化合物与席夫试剂不发生显色反应的是( )
- 下列化合物能与卢卡斯试剂反应的是( )
- 关于粗分散系统,下列说法错误的是( )。
- 从缓冲溶液的定义来看,不能组成缓冲溶液的体系是
- 下列各组分子间同时存在取向力、诱导力、色散力和氢键的是( )
- 己烯的同分异构体中,哪种最易发生催化加氢反应?
- 下列混合溶液中( )是缓冲溶液:
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201906/74ef8b2ce1c343e0880eff9701fa1f49.png
- 下列化合物中,和Tollens试剂作用不产生银镜的是( )
- 关于溶液的渗透方向,下列说法正确的是( )。
- 25℃时0.10mol·L-1H2S溶液加水使浓度变为0.05mol·L-1,则( )
- 分子中所有碳原子共平面的是( )
- 下列自由基,最稳定的是( )
- 现有0.20mol/l HCl溶液与0.20mol/l 氨水,两种溶液等体积混合,混合溶液的pH=?
- 下列哪种作用力不属于分子间作用力。( )
- 关于溶胶的电泳现象,下列说法不正确的是( )。
- 下列试剂中,可与烯烃进行反马氏规则加成的是( )。
- 下列化合物既能与金属钠反应产生氢气又可以与NaOH反应的是( )。
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201906/094fbf497fae48fabb2b825f5014c76a.png
- 下列分子中,哪种存在对映异构体?
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201905/bc755a7df6e543c490c3cd88c9a9042d.png
- 下列化合物中哪个能量最低?
- 具有共轭关系的酸碱对,Ka和Kb的关系为( )
- 水的三相点是水、冰、水蒸气三者可共存且相互平衡的温度、压力条件,所对应的温度为 0.01℃,则在此温度下,水所承受的外压为
- 鉴别2-甲基环丙烷和2-甲基丙烯,可采用( )
- 决定NaHCO3~Na2CO3缓冲体系pH值的因素是( )
- 当某基态原子的N电子层上有2个电子时,该原子的M电子层一定有
- 符号n用来表示( )。
- 0.3mol·L-1葡萄糖溶液与0.3mol·L-1NaCl溶液产生的渗透压大小( )。
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201906/317200f2e1574da9a6e437c5bcadccc6.png
- 禁止使用工业酒精配置饮料酒,是因为工业酒精中含有下列物质中的( )。
- 内消旋酒石酸无旋光性的原因是 ( )
- 乙醇与二甲醚是什么异构体( )。
- 常见缓冲溶液中起抵抗外加少量强酸作用的是
- 关于杂化轨道的类型,下列说法不正确的是( )。
- 医学上等渗溶液的渗透浓度范围为( )。
- 下列不是有机化合物的是( )
- 同离子效应与盐效应的关系,正确的说法是
- 关于物质的量,下列表示方法错误的是( )。
- 下列物质的分子是由极性共价键形成的非极性分子为( )
A:错 B:对
答案:错
A:错 B:对
答案:错
A:错 B:对
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:降低
A:对 B:错
答案:对
A:错 B:对
答案:对
A:对 B:错
答案:错
A:错 B:对
答案:A
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:环己酮 B:亚硫酸钠 C:都可以 D:苯乙酮 E:硫酸亚铁
A:甲苯 B:丙酮 C:苯乙烯 D:乙腈
A:
己二酸
B:2-羟基苯甲酸
C: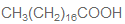
2-羟基丙酸
A:Fe(OH)3 胶体通电,阴极处颜色加深 B:阳光在含灰尘的室内形成光的通路 C:花粉在水面上作布朗运动 D:石膏使豆浆变成豆腐
A:对-甲苯酚 B:水杨酸 C:阿司匹林 D:丙醇 E:苯甲醇
A:咖啡 B:豆浆 C:牛奶 D:矿泉水
A:苄基醇 B:苯乙酮 C:环己酮 D:苯乙醛
A:
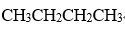 B:
B: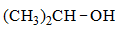 C:
C: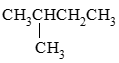 D:
D: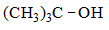 E:
E: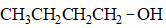
A:分散相离子的直径小于100nm B:粗分散系统为非均相系统 C:分散相和分散介质会自动分离 D:粗分散系统为不稳定的多相系统
A:NaAc B:HAc-NaAc
A:
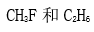 B:
B: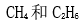 C:
C: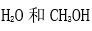 D:苯和
D:苯和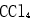
A:1-己烯 B:2,3-二甲基丁烯 C:2-甲基-2-戊烯 D:2-己烯
A:100mL 0.1mol·L-1的NH3·H2O与50mL0.1mol·L-1的NaOH混合。 B:50mL 0.2mol·L-1的HCl与100mL 0.1mol·L-1的NH3·H2O混合。 C:100mL 0.1mol·L-1的NH3·H2O与50mL0.1mol·L-1的HCl混合。 D:100mL 0.1mol·L-1的HCl与50mL0.1mol·L-1的NH3·H2O混合。
A:
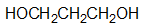 B:
B: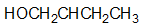 C:
C: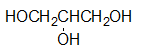 D:
D: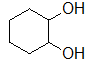
A:丙酮 B:乙醛 C:甲醛 D:甲酸
A:总是浓溶液一方往稀溶液一方渗透 B:总是从纯溶剂一方往溶液一方渗透 C:总是稀溶液一方往浓溶液一方渗透 D:总是从纯溶剂一方往溶液一方,或者从稀溶液一方往浓溶液一方渗透
A:电离常数增大 B:电离度增大 C:电离常数减少 D:电离度减少
A:CH3CH=CHCH3 B:
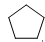 C:
C: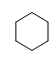 D:CH3CH=CHCH(CH3)2
D:CH3CH=CHCH(CH3)2
A:
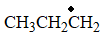 B:
B: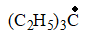 D:
D: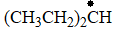
A:6.1 B:4.8 C:5.1 D:4.0
A: 氢键力 B: 诱导力 C: 取向力 D:色散力
A:溶胶的分散相粒子在分散介质中的定向移动 B:带有负电荷的溶胶粒子,电泳时移向正极 C:中性粒子,电泳时不移动 D:带有正电荷的溶胶粒子,电泳时移向负极
A:HBr B:HI C:HCl D:HF
A:
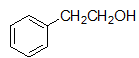 B:
B: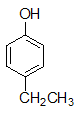 C:
C: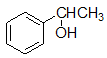 D:
D: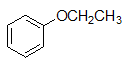
A:397 kPa B:793 kPa C:793 Pa D: 397 Pa
A:1,4-戊二烯 B:1,3-戊二烯 C:1,2-戊二烯 D:2,3-戊二烯
A:顺—1—氯—4—溴环己烷 B:反—1—溴—4—氯环己烷 C:顺—1—溴—4—氯环己烷 D:反—1—氯—4—溴环己烷
A:
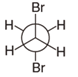
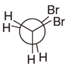 C:
C: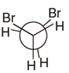 D:
D: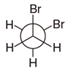
A:Ka·Kb > Kw B:Ka·Kb < Kw C:Ka·Kb= Kw D:Ka = Kb
A:
101.325KPa
B:0.6106KPa
C:其余选项都不是
D:100KPa
A:溴水 B:AgNO3溶液 C: HBr D: KMnO4酸性溶液
A:[NaHCO3]/[Na2CO3] B:[NaHCO3] C: [H2CO3]/[Na2CO3] D:[H2CO3]
A:18个电子 B:8个电子 C:10个电子 D:8~18个电子
A:物质的质量 B:物质的量 C:物质的量浓度 D:质量浓度
A:相等 B:后者大 C:无法确定 D:前者大
A:③④②① B:①④②③ C:①②④③ D:①③④②
A:异戊醇 B:甲醇 C:丙三醇 D:乙二醇
A:分子内无手性碳原子 B:分子内无对称面 C:分子内含有对称面 D:分子内含两个手性碳原子
A:官能团异构 B:互变异构 C:位置异构 D:碳架异构
A:抗酸成分 B:共轭酸 C:不确定 D:抗碱成分
A:
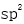 杂化轨道
B: 孤电子杂化轨道
C:sp杂化轨道
D:
杂化轨道
B: 孤电子杂化轨道
C:sp杂化轨道
D: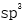 杂化轨道
杂化轨道
A:320-460
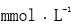 B:280-320
B:280-320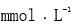 C:大于320
C:大于320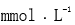 D:小于280
D:小于280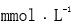
A:CH3OH B:CH3CN C:CH3Cl D:NH3
A:同离子效应的作用总是大于盐效应 B:同离子效应的作用总是小于盐效应 C:二者同时存在 D:二者不能同时存在
A: n(NaCl) B: n(硫酸) C: n(HCl) D: n(NaOH)
A:CCl4 B:NH3 C:H2 D:HCl
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!