第四章 多组分系统热力学:抓住多组分体系中偏摩尔量和化学势的概念;认识理想液态混合物及其通性;掌握拉乌尔定律和亨利定律;学会溶液中各组分化学势的表示方法,明晰稀溶液依数性及其应用。4.1偏摩尔量:偏摩尔量的引出解决了什么问题? 我们在使用它时,应该注意什么?各偏摩尔量在变化的时候相互有联系吗?[单选题]溶液中任一组分的偏摩尔体积( )。选项:[必然和纯组分的摩尔体积相等, 可能是正值,也可能是负制, 总是正值, 不可能是负值]
4.2化学势:化学势定义的与四个基本方程之间有何关联?偏摩尔吉布斯函数的化学势如何应用?各种气体的化学势的表达式从哪里来?
4.3溶液系统的化学势:理想液态混合物和理想稀溶液中的各组分的化学势的表达式有什么区别和联系?四个依数性概念的关键何在?
[判断题]溶液化学势等于溶剂化学势与溶质化学势之和。选项:[对, 错]
[单选题]
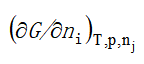 ( )。选项:[只能称为化学势, 既可称为化学势也可称为偏摩尔量, 是某物质的摩尔吉布斯函数, 只能称为偏摩尔量]
( )。选项:[只能称为化学势, 既可称为化学势也可称为偏摩尔量, 是某物质的摩尔吉布斯函数, 只能称为偏摩尔量][多选题]挥发性溶质溶于水后,则下列说法正确的是( )。选项:[溶液的蒸气压较纯水的蒸气压大小要视体系与组成而定, 水的凝固点下降, 溶液的蒸气压大于纯水的蒸气压, 水的蒸气压下降,与溶质的浓度无关]
[判断题]活度等于1的状态与标准态的化学势相等。选项:[错, 对]
[多选题]等温等压下,有几种纯液体组成的液态理想混合物时,正确的是( )。选项:[
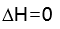 ,
, 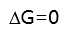 ,
, 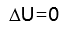
,
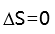 ]
][判断题]溶剂的沸点升高常数Kb是随溶剂的本性而异的。选项:[错, 对]
[单选题]同一溶液中的溶质,当选用不同的标准态时,溶质的( )。选项:[活度相同,活度系数、化学势不同, 活度、活度系数、化学势都相同, 活度、活度系数不同,化学势相同, 活度系数相同,活度、化学势不同]
温馨提示支付 ¥1.00 元后可查看付费内容,请先翻页预览!

