提示:内容已经过期谨慎付费,点击上方查看最新答案
高等化工热力学
- 气体真空节流膨胀产生冷效应时的微分节流系数是( )。
- 下述说法哪一个正确? 某物质在临界点的性质( )。
- 关于化工热力学研究特点的下列说法中不正确的是( )
- 一流体从状态1分别经历可逆过程R与不可逆过程NR到达状态2,两个过程的环境状态相同,则过程R的理想功比过程NR的理想功要:( )
- 二元气体混合物的摩尔分数
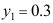 ,在一定的
,在一定的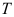 、
、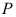 下,
下,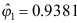 ,
,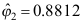 ,则此时混合物的逸度系数为( )。
,则此时混合物的逸度系数为( )。 - 偏摩尔性质是( )。
- 90℃,1atm下苯(1)-甲苯(2)汽液平衡系统可视为完全理想系。此条件下蒸汽压为:
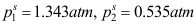 ,则汽液平衡组成
,则汽液平衡组成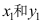 分别是( )。
分别是( )。 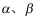 两相达到平衡,系统的热力学性质表述中错误的是:( )
两相达到平衡,系统的热力学性质表述中错误的是:( )- 由于直接混合引起两个物系之间进行热交换,那么包括这两个物系的绝热体系的熵变为( )。
- 关于化工热力学用途的下列说法中不正确的是( )
- 气体经过稳流绝热膨胀,对外做功,如忽略宏观动能,位能变化,无摩擦损失,则此过程气体焓值( )。
- 传热速率的单位,不正确的是( )。
- 真实气体在______的条件下,其行为与理想气体相近:( )。
- 关于制冷原理,以下说法不正确的是( )。
- 纯流体在一定温度下,如压力低于该温度下的饱和蒸汽压,则此物质的状态为( )。
- 泡点的轨迹称为_____,露点的轨迹称为_____,饱和汽、液相线与三相线所包围的区域称为_____。( )
- 以下四个偏导数中只有( )有偏摩尔性质
- 作为朗肯循环改进的回热循环是从汽轮机(即蒸汽透平机)中抽出部分蒸汽去( )。
- 戊醇和水形成的二元三相气液液平衡状态,其自由度F=( )。
- 乙醇-水在101.3KPa下共沸体系,其自由度为( )。
- 对单原子气体和甲烷,其偏心因子ω近似等于( )。
- 分离过程的有效能损失
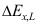 ( )。
( )。 - 关于热力学基本方程dU=TdS-PdV, 下面的说法中准确的是( )。
- 卡诺制冷循环的制冷系数与( )有关。
- 理想的Rankine循环工质是在汽轮机中作( )膨胀。
- 对于蒸汽动力循环要提高热效率,可采取一系列措施,以下说法不正确的是( )。
- 二元非理想溶液在极小浓度的条件下,其溶质组分和溶剂组分分别遵守( )
- 各种状态方程如RK方程、理想气体方程、vdw方程、SRK方程、PR方程,请为它们的计算准确度排序。( )
- 热源温度为1200K,环境温度为300K,高温热源提供热量1000J中的无效能为( )J。
- 对理想溶液的性质,下列说法描述不正确的是:( )
- 下列哪个条件不符合蒸汽压缩制冷循环制冷剂的选择要求( )。
在过程能量系统分析中,按“三环节”结构模型划分,反应器属于哪个子系统?
- 熵产生
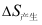 是由于( )而引起。
是由于( )而引起。 - 纯物质的第二virial系数B( )
- 溴化锂-水吸收制冷循环过程的制冷剂是( )。
- 常压下某液体沸腾时,保持不变的热力学性质是( )。
- 下列四个关系式中哪一个不是麦克斯韦关系式?( )
- 节流效应T-P图上转化曲线是表示( )的轨迹。
- 某封闭体系经历一不可逆过程,系统所做的功和排出的热量分别为100kJ和45kJ,问系统的熵变:( )
- 理想溶液中所有组分的活度系数为零。( )
- 纯物质的平衡汽化过程,摩尔体积、焓、热力学能、吉氏函数的变化值均大于零。( )
- 当压力大于临界压力时,纯物质就以液态存在。( )
- 在一定温度和压力下的理想溶液的组分逸度与其摩尔分数成正比。( )
不可逆过程一定是自发的,自发过程一定是不可逆的
无论流体的温度高于或低于环境温度,其有效能均为正
在化工过程中,高温位物流与低温位物流直接混合换热过程中总热量保持不变,但(火用)减少,存在混合(火用)损。
- 体系混合过程的性质变化与该体系相应的超额性质是相同的。( )
在化工过程中,高温位物流与低温位物流直接混合换热过程中总热量保持不变,但火用减少,存在混合火用损。
真实气体的焓不仅与温度有关,而且与压强也有关
A:μj>0 B:μj=0 C:μj <0 D:不确定
AI参考:气体真空节流膨胀产生冷效应时的微分节流系数是【C:μj <0】。微分节流系数μj描述了通过节流元件的流量与压力、温度之间的关系。在真空节流过程中,流量随压力的降低而减小,因此μj为负值,即μj<0。'
A:是该物质本身的特性 B:与外界压力有关 C:与外界物质有关 D:与外界温度有关
答案:是该物质本身特性
A:获取数据的方法为少量实验数据加半经验模型 B:处理方法为以理想态为标准态加上校正 C:研究体系为实际状态 D:解释微观本质及其产生某种现象的内部原因
答案:解释微观本质及其产生某种现象的内部原因
A:相等 B:小 C:大 D:不确定
答案:对
A:0.9192 B:0.9097 C:0.9827 D:0.8979
答案:0.90353AI参考:正确答案是C,逸度系数与温度和压力有关,因此应选C项。具体解析如下:在一定温度和压力下,某物质的逸度等于摩尔分数除以混合物的化学势。本题中给出的图像为摩尔分数随温度和压力的变化,当给定温度为300K、压力为1atm时,A、B项中的物质逸度为1/化学势($C$选项正确),即该物质的逸度系数为0.9827;给定温度为350K、压力为2atm时,摩尔分数发生变化,而该物质的逸度系数为:$frac{0.9756}{化学势(新条件)} = 0.9756/化学势(350K,1atm)$,因此D项错误。因此,本题答案为C选项。注意:由于本题未给出具体的混合物化学势,因此无法求出具体的逸度系数。本题主要考察了逸度和化学势的概念和计算方法。综上,本题的正确答案为C选项。'
A:剩余性质 B:强度性质 C:容量性质 D:超额性质
答案:强度性质
A:0.773, 0.576 B:0.227, 0.424 C:0.576, 0.773 D:0.424, 0.227
AI参考:正确答案是B:0.227, 0.424。题目中给出的是理想系的蒸汽压,由题图可知在90℃和1atm下苯-甲苯汽液平衡系统的蒸汽压为46.5kPa,也就是说此时该系统中蒸汽分压与液体分压之和等于大气压强。再由数据比例计算出对应的液体和蒸汽的分压百分比,液体部分总和为0.9786+0.5698=1.5448(占整个体系的15.45%),液态甲苯占总液体量的0.645=64.5%,剩余部分(约为2-15.45%=85%)即为汽态苯的体积,由图可得,气态苯在1atm下的蒸汽分压为37.7kPa,那么汽态苯的体积百分比为37.7/46.5=80%,液态苯的体积百分比为(1-80%)=20%,再由数据比例计算出对应的液体和蒸汽的分压百分比,液态苯占总液体量的比例为(20%)/(1+20%)=20%,所以液态苯的组成是0.227,汽态苯的组成是0.424。因此答案为B。'
A: B: C: D:
A:不定值 B:零 C:正值 D:负值
AI参考:正确答案是D:负值。在绝热体系中,熵变只与过程有关,与始末状态无关。两个物系之间直接混合引起热交换是一个不可逆过程,所以熵变是负值。因此,本题的正确选项为D:负值。'
A:通过热力学模型,用易测得数据推算难测数据,用少量实验数据推算大量有用数据; B:优化工艺过程 C:可以判断新工艺、新方法的可行性 D:预测反应的速率
A:不确定 B:不变 C:减少 D:增加
A:kJ/h B:kW·h C:kJ/s D:J/h
AI参考:传热速率的单位,不正确的是 B:kW·h。传热速率的正确单位有 kJ/h (千焦耳/时)、J/s (焦耳/秒) 和 W (瓦)。kW·h 是电能的单位,与传热速率无关。因此,B选项是不正确的。'
A:高温低压 B:低温高压 C:低温低压 D:高温高压
A:只有当 ,经节流膨胀后,气体温度才会降低 B:任何气体,经等熵膨胀后,温度都会下降 C:任何气体,经节流膨胀后,温度都会下降 D:在相同初态下,等熵膨胀温度降比节流膨胀温度降大
A:饱和液体 B:饱和蒸汽 C:过热蒸汽 D:过冷液体
A:饱和液相线,饱和汽相线,汽液共存区 B:饱和汽相线,饱和液相线,汽液共存区 C:汽液共存线,饱和汽相线,饱和液相区 D:饱和液相线,汽液共存区,饱和汽相线
AI参考:正确答案是:B:饱和汽相线,饱和液相线,汽液共存区。泡点的轨迹称为饱和汽相线,露点的轨迹称为饱和液相线,两者形成的区域为汽液共存区。所以选择B选项。'
A: B: C: D:
AI参考:正确答案是B。只有B选项具有偏摩尔性质。偏导数是一种函数关系,用于描述函数在某个变量的变化率在特定方向上的表现。在化学工程中,偏摩尔性质是用来描述体系中某些宏观量随一组独立变量变化的性质。对于给定的函数关系,只有B选项是描述宏观量的函数,因此具有偏摩尔性质。其他选项要么是偏微分性质,要么是只与单一变量有关的关系,不具有偏摩尔性质。'
A:冷凝器加热冷凝水 B:锅炉加热锅炉进水 C:回热加热器加热锅炉进水 D:过热器再加热
A:1 B:0 C:2 D:3
A:2 B:1 C:0 D:3
A:3 B:2 C:0 D:1
A:> 0 B:可正可负 C:= 0 D:< 0
AI参考:正确选项是【D:< 0】。根据题目描述,分离过程的有效能损失小于某个数值,即有效能损失为负值,因此选项D是正确答案。'
A:PdV是体积功 B:TdS是过程热 C:TdS是可逆热 D:在可逆过程中,PdV等于体积功,TdS即为过程热
A:制冷剂的循环速率 B:制冷剂的性质 C:压缩机的功率 D:制冷剂的工作温度
A:等压 B:等焓 C:等熵 D:等温
A:对Rankine循环进行改进,采用再热循环。 B:同一Rankine循环动力装置,可提高乏气压力。 C:对Rankine循环进行改进,采用回热循环。 D:同一Rankine循环动力装置,可提高蒸气过热温度和蒸汽压力
A:Henry规则和Henry规则 B:Henry规则和Lewis-Randll规则 C:Lewis-Randll规则和Lewis-Randll规则 D:均不适合
A:SPR > RK > PR > vdw > 理想气体方程 B:PR ≈ SRK > RK > vdw > 理想气体方程 C:RK > PR> SRK > vdw > 理想气体方程 D:PR > vdw > SRK > RK > 理想气体方程
A:250 B:750 C:400 D:300
A: B: C: D:
A:较低的临界温度 B:沸点低 C:汽化潜热大 D:冷凝压力低
A:不属于以上任一环节 B:能量利用环节 C:能量转换环节 D:能量回收环节
A:体系与环境之间的热量交换 B:体系内部的不可逆性 C:体系与外界的物质交换 D:体系与外界功的交换
AI参考:选项 B:体系内部的不可逆性 是正确答案。熵产生是由于体系内部各种物理和化学过程引起的,这些过程包括热量转化、物质转化、微观粒子的扩散等,这些过程都是不可逆过程。这些不可逆过程会导致体系内部能量的分布和转换,从而产生熵。而选项 A、C、D 均不是引起熵产生的主要原因。'
A:是任何两强度性质的函数 B:仅是T的函数 C:是T和V的函数 D:是T和P的函数
A:水 B:溴化锂和水 C:液溴 D:溴化锂
A:摩尔体积 B:摩尔内能 C:摩尔熵 D:摩尔自由焓
A: B: C: D:
A:μj = 0 B:μj > 0 C:μj < 0 D:不确定
A:不确定 B:等于零 C:大于零 D:小于零
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
AI参考:B:错。自发的过程不一定是不可逆的,也有可能存在某种机制使得过程逐渐变得不可逆。因此,不可逆过程不一定是自发的,自发过程也不一定是不可逆的。'
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
AI参考:正确答案是B:错。\r真实气体的焓不仅与温度有关,而且与压力也有关。这是错误的,因为焓是一个状态函数,只与气体的状态有关,而与温度和压力的数值大小无关。只有当温度和压力同时变化时,焓才会随之改变。'
温馨提示支付 ¥1.80 元后可查看付费内容,请先翻页预览!

