浙江大学
- 只要电极反应为可逆反应的电极就能作为参比电极
- 金属/溶液间的相间电位的产生原因与双电层产生的原因相同( )
- 由于离子迁移数与离子的迁移速率成正比,因此,一种离子的迁移速率一定时,其迁移数也一定,凡是能够改变离子迁移速率的因素都能改变离子迁移数
- 电化学反应平衡被打破往阴极方向偏离,则电极电位发生负移
- 马口铁是镀锡铁板,是罐头用的主要容器。在封存食品环境下,锡镀层是阳极性镀层,对基体铁起到保护作用
- 若某一电极体系处于平衡状态,则正、逆向反应速度均为零
- 双电层结构既可以自发形成,也可以认为调控
- 现如今,碱性Zn-Mn电池已基本实现无Hg化,为了抑制电极材料的自放电,在电解液中加入缓蚀剂以达到上述目的
- 当电极系统中无外加电流(即无净电流通过),则该电化学体系处于平衡状态
- 任何电极过程都存在着速度控制步骤
- 电解食盐水时阳极主要发生析氯反应而不是析氧反应,这是因为前者的平衡电极电位小于后者
- 电极表面有稳态电流通过,肯定有净物质的生成或消耗
- 电解池的耗电功率随电解电流增大而增大
- 双电层区内部的溶液本体介质的介电常数是不一样的
- 电极电位偏离平衡电位发生正移,则电化学反应偏离平衡态,发生净的阴极反应
- 溶液/溶液间的相间电位的产生是由于两相交界处的正负离子的迁移数不同( )
- 组成电极材料的晶粒尺寸达到纳米级后,该电极材料的电化学性能总能提高
- 平衡电极电位更高的电极的阴极反应速度也更快
- 两个(或以上)电极反应在同一电极上发生耦合,在开路状态下形成的稳定电位叫“混合电位”,该电位不是平衡电位
- 电解库伦法又分直接库伦法和间接库伦法
- 当电极表面无外加电流(即无净电流通过),则该电极处于平衡状态
- 现代电化学认为,若某一电极反应的速度完全受双电层内电荷的转移步骤控制,则电极电位的变化是通过改变电极的正、逆向反应的活化能达到改变电化学反应速度的
- 溶液中各离子的迁移数的总和为1
- 关于电镀用阳极,以下描述正确的是()
- 电化学反应 O + ne = R 在Ⅰ/Ⅱ相界面处于平衡时,存在 ( )。
- 下列电化学家中曾获得诺贝尔奖的是( )
- 能斯特方程是()
- 某一物种(i,核电荷数n)在两相界面处平衡的基本条件为( )。
- 影响某一固定电极反应净反应速度的因素有( )
- 电解池在工作时()
- 下列哪个不是电子转移步骤的基本动力学参数()
- 用电位法测定溶液的pH值时,电极系统由玻璃电极与饱和甘汞电极组成,其中玻璃电极是作为测量溶液中氢离子活度(浓度)的()
- 关于交换电流密度(i0)的描述不正确的是( )
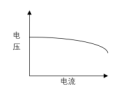
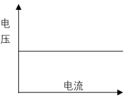
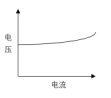
- 以下( )是化学电源在充电时的电压-电流曲线。
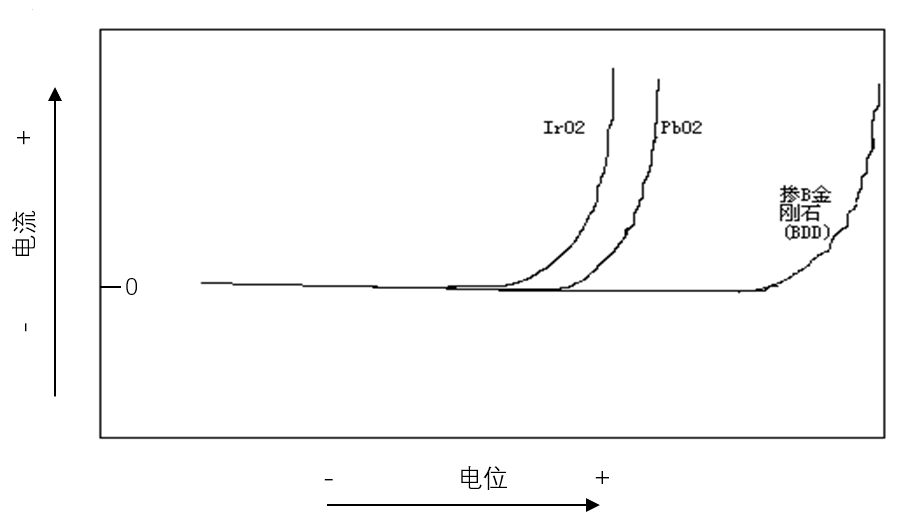
下图为三种电极在H2SO4水溶液中的阳极极化曲线,试问何种电极是析氧的最佳电极?
- https://image.zhihuishu.com/zhs/onlineexam/ueditor/201912/599fdd9bf07a4e5db99ddedf6a06f546.png
- 下列各种溶液中可作盐桥溶液的是()
- 已知Volta电池中负极为Zn金属,正极为Cu金属,电解质溶液为H2SO4。试问若对该电池进行充电,正极发生的主要电化学反应为()
- 理论上说,采用电解的方法可将0.01M Pb2+ + 0.01M Cu2+混合液中的()以析出金属单质的形式分离开来。已知j0(Pb2+/Pb)= -0.126V (SHE)、j0(Cu2+/Cu)=0.345V (SHE)。
- 下列关于理想极化电极的说法错误的是()
- 相的内电位由()组成
- 已知Volta电池中负极为Zn金属,正极为Cu金属,电解质溶液为H2SO4。试问该电池在工作时,正极主要发生的电化学反应为()
- https://image.zhihuishu.com/zhs/onlineexam/ueditor/201912/4bf547bf13aa4bd58d0d76d03b531f85.png
- 粒子在溶液中运动受到以下哪种力的作用()
- 在开路(断路)稳态时,下述不正确的是()
- 以下( )是在某一恒定体积的容器中采用电解库伦法(施加的电位恒定)做定量分析时的电流-时间的关系曲线。
- 当电极反应1(R1 – n1e « O1,j平衡=0.3V(SHE))与电极反应2(R2 – n2e « O2,j平衡=0.5V(SHE))在同一电极表面上发生。若对该电极表面通阳极电流,则()
- 若电极反应Fe – 2 e- ® Fe2+ 在某一阳极电位下的净反应电流密度为i (mA/cm2),则Fe金属的溶解速度为()
- ()是金属防护最常用的手段
- 电化学研究与测量用的参比电极有特殊的要求,下述错误的是()
A:错 B:对
答案:错
A:错 B:对
答案:对
A:对 B:错
答案:B
A:对 B:错
答案:对
A:对 B:错
答案:对
A:对 B:错
答案:错
A:对 B:错
答案:对
A:对 B:错
答案:对
A:对 B:错
答案:错
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:采用不溶性阳极所得的电镀层纯度更大 B:采用不溶性阳极更节省能耗 C:不溶性阳极表面发生的是电催化反应 D:可溶性阳极表面发生金属溶解,其电化学反应的的电流效率往往低于100%
A:
![]()
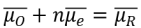
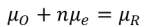
A:Macus B:Van Hoff C:Goodenough D:Nernst
A:动力学方程 B:适用于平衡状态 C:近似适用于准平衡状态 D:热力学方程
A:
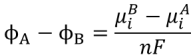
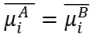
A:电极电位 B:电极与溶液的接触面积 C:电极材料 D:溶液的搅拌状态
A:电子经溶液(电解质)从正极流向负极 B:溶液中阳离子从负极定向流向正极 C:负极发生还原反应,正极发生氧化反应 D:电子从负极经外电路流向正极
A:外电流密度 B:交换电流密度 C:传递系数
A:金属电极 B:电解电极 C:参比电极 D:指示电极
A:i0是电化学反应在平衡状态时的正、逆向反应绝对电流,是可以直接测定的 B:i0越大,电极反应越不容易偏离平衡状态 C:i0反映电化学反应的可逆程度 D:i0与反应物浓度有关
A:
A:IrO2 B:PbO2 C:BDD
A:准可逆 B:完全不可逆 C:完全可逆
A:正负离子的扩散速度几乎相同的稀溶液 B:正负离子的扩散速度接近, 浓度较大的惰性盐溶液 C:正负离子的扩散速度几乎相同的浓溶液 D:可溶性惰性强电解质溶液
A:2H++2e→H2 B:2H2O-4e→4H++O2 C:Cu-2e→Cu2+
A:Pb2+ B:Cu2+ C:其它两个选项都不对
A:理想极化电极不发生电极反应 B:交换电流密度趋近于零 C:电极电位恒定不变 D:不可逆电极
A:
相的表面电位
B:相的外电位
C:相的表面电位、相的外电位两项共同
A:Cu-2e→Cu2+ B:2H++2e→H2 C:Cu2++2e→Cu
A:曲线1 B:都不可能 C:曲线2
A:
其他都是
B:电场力
C:溶液的摩擦力
A:电极上可能仍会发生净的氧化反应或还原反应,此时氧化电流等于还原电流,但方向相反 B:若是单电极反应,则电极处在平衡状态 C:此时形成的稳态电位不一定是平衡电位 D:电极表面不会发生净的氧化反应或还原反应
A:
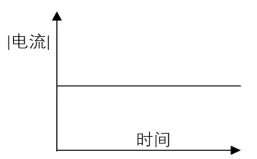
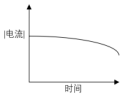
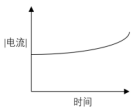
A:两个电极反应将都发生氧化反应 B:若一个发生阳极反应,另一个必发生还原反应 C:此时实际电极电位必高于0.5V(SHE) D:反应1发生氧化反应,但2不一定
A:2´F´i (mmol·cm-2·s-1) B:2i/F (mmol·cm-2·s-1) C:(1/2)i/F (mmol·cm-2·s-1) D:2 F/i (mmol·cm-2·s-1)
A:涂层 B:电化学保护 C:缓蚀剂
A:电极反应具有很高的可逆性 B:交换电流密度(i0)要小 C:不易发生极化 D:参比电极内的溶液尽可能不受测试体系污染
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!

