第四章单元测试
- 对于一个给定条件下的反应,随着反应的进行** ( )
某化学反应的方程式为 2 A→P,则在动力学研究中表明该反应为** ( )
- 反应N2(g)+ 3 H2(g)= 2 NH3(g),ΔHΘ < 0 ,升高温度时,正反应速率 υ 和逆反应速率υ’的变化为** ( )
- 对于催化剂特性的描述,不正确的是*** ( )
- 某反应在一定条件下的平衡转化率为 35%,当加入催化剂后,若其它反应条件不变,则反应的平衡转化率是 ( )
- 某一反应 A → B ,不论其起始浓度如何,完成 70% 反应的时间都相同,则该反应的级数为 ( )
- 某化学反应,消耗
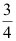 反应物所需时间是消耗
反应物所需时间是消耗 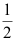 所需时间的 2 倍,则该反应的级数
所需时间的 2 倍,则该反应的级数
为 ( ) - 化学反应 CO(g)+ Cl2(g)= COCl2(g), 实验测得速率方程为
υ= k [Cl2]n [CO] ,当维持温度和CO 的浓度不变时,Cl2(g)的浓度增大到原来的 3 倍,υ增大到原来的 5.2 倍,则反应对Cl2(g)的级数 n为 ( ) - 对于一个确定的化学反应来说,下列说法中正确的是 ( )
- 对基元反应而言,下列叙述中正确的是 ( )
- 某化学反应:2 A + B → C 是一步完成的。A 的起始浓度为2 mol·L-1,B的起始浓度为4 mol·L-1,1 秒钟后,A 的浓度下降到 1 mol·L-1,则该反应速率为 ( )
- 某基元反应的ΔrHmΘ = -150 kJ · mol-1 ,则其正反应活化能** ( )
- 使用合适的催化剂能加快反应的速率,反应结果催化剂本身组成不发生改变,质量也不变。催化剂并不参与反应,仅起促进反应进行的作用。( )
- 反应的活化能越大,在一定温度下,反应速率也越快。( )
- 正 、逆反应的活化能,数值相等,符号相反。( )
A:平衡常数 K 变大 B:正反应速率降低 C:速率常数 k 变小 D:逆反应速率降低
答案:正反应速率降低
A:二级反应 B:双分子反应 C:其余三个选项都无法确定 D:基元反应
A:υ减小,υ’减小 B:υ减小,υ’增大 C:υ增大,υ’增大 D:υ增大,υ’减小
A:催化剂只能缩短反应达到平衡的时间而不能改变平衡状态 B:催化剂在反应前后其化学性质和物理性质皆不变 C:加入催化剂不能实现热力学上不可能进行的反应 D:催化剂不能改变平衡常数
A:大于35% B:小于35% C:无法判断 D:等于35%
A:一级 B:零级 C:二级 D:无法判断
A:二级 B:一级 C:零级 D:三级
A:1 B:1.5 C:3 D:2
A:ΔrHmΘ越负,反应速率越快 B:活化能越小,反应速率越快 C:ΔrGmΘ 越负,反应速率越快 D:活化能越大,反应速率越快
A:反应级数不一定与反应分子数相一致 B:反应级数总是大于反应分子数 C:反应级数总是小于反应分子数 D:反应级数和反应分子数总是一致的
A:0.5 mol·L-1·s-1 B:-0.5 mol·L-1·s-1 C:-1 mol·L-1·s-1 D:2 mol·L-1·s-1
A:必定大于或等于150 kJ · mol-1 B:可以大于或小于150 kJ · mol-1 C:只能小于150 kJ · mol-1 D:必定等于或小于150 kJ · mol-1
A:对 B:错
A:对 B:错
A:对 B:错
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!