第五章单元测试
- 已知某反应的ΔrGmΘ> 0,则该反应的平衡常数KΘ值** ( )
- 下列反应2 SO2(g)+ O2(g)= 2 SO3(g) 达平衡时,保持体积不变,加入惰性气体 He,使总压力增加一倍,则( )
- 某温度时,化学反应 A +
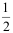 B =
B = 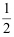 A2B 的平衡常数 K=1×104 ,则在相同温度下,反应 A2B = 2A + B 的平衡常数为 ( )
A2B 的平衡常数 K=1×104 ,则在相同温度下,反应 A2B = 2A + B 的平衡常数为 ( ) - 670 K时 H2(g)+ D2(g)= 2 HD(g)的平衡常数 KΘ= 3.78 ,同温度下反应 HD(g)=
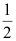 H2(g)+
H2(g)+ 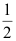 D2(g) 的 K 为 ( )
D2(g) 的 K 为 ( ) - 在 523 K 时,反应 PCl5(g)= PCl3(g)+ Cl2(g) 的 KΘ=1.85 , 则反应的ΔrGmΘ(kJ·mol-1)为 ( )
- 将 BaO2放在一个与U形压力管相连的抽空玻璃容器中,在固定温度下将容器加热,研究反应2 BaO2(s)=2 BaO(s)+ O2(g),在体系达平衡时,下列论述中正确的是 ( )
- 在一定温度下,将 1.00 mol SO3(g)放在 1.00 L密闭容器中,下列反应2 SO3(g)= 2 SO2(g)+ O2(g)达到平衡时,SO2(g)为 0.60 mol ,则反应的平衡常数KΘ 为*** ( )
- 已知 25 ℃时Ag 2O(s)的ΔfGmΘ =-10.82 kJ·mol-1,则欲使Ag2O(s)在 25 ℃时 自发分解,O2(g)的分压为( )
- 已知乙苯脱氢制乙烯的反应如下:
C6H5-C2H5(g)= C6H5-C2H3(g)+ H2(g)若 873 K时其 KΘ=0.178 ,则在该温度及平衡压力为101325 Pa 下,乙苯的转化率为*** ( ) - 已知反应3 H2 (g)+ N2(g)= 2 NH3(g)ΔrHmΘ=-92.4 kJ·mol-1,若 298 K时 KΘ= 6.75×105 ,则673 K 时的 KΘ 值为 ( )
- 在反应 A + B = C + D 中,开始时只有A 和 B ,经过长时间反应,最终结果是* ( )
- 反应 PCl5(g)= PCl3(g)+ Cl2(g) ,平衡时总压力为 p kPa,分解率α=50%,则此时反应的平衡常数 KΘ 为( )
- 液态水在100℃.101.3 kPa条件下气化为水蒸气;冰在0℃.101.3 kPa条件下转化为液态水,这些过程均可认为是可逆过程,因此△G = 0 。( )
- 等温方程式 Δ G = Δ GΘ + RT ln Q 仅适用于可逆反应的平衡状态。( )
- 任何一个可逆的化学反应,当达到平衡时各反应物和生成物的浓度等于常数。( )
A:KΘ< 0 B:KΘ> 0 C:KΘ> 1 D:KΘ< 1
答案:KΘ< 1
A:条件不足,无法判断 B:平衡向右移动 C:平衡不发生移动 D:平衡向左移动
A:1×104 B:1×10-8 C:1×10-4 D:1×100
A:0.133 B:0.265 C:1.94 D:0.514
A:2670 B:-2.67 C:2.67 D:-2670
A:氧的压力与 BaO2 的质量成正比 B:如果向体系内导入氧,则氧与BaO反应,最终O2(g)的压力将增加 C:氧的压力等于 Kp D:氧的压力与生成的 BaO 质量成正比
A:0.54 B:0.36 C:0.68 D:0.45
A:> 16.33 Pa B:> 1.29 kPa C:< 1.29 kPa D:< 16.33 Pa
A:30.2% B:18.9% C:38.9% D:151%
A:8.21×104 B:6.40×10-4 C:7.14×10-2 D:4.26×102
A:A.B.C.D浓度都一样 B:C 和 D 浓度大于 A 和 B C:A 和 B 浓度大于 C 和 D D:A.B.C.D浓度不再变化
A:
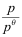 B:
B: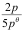 C:
C: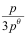 D:
D: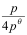
A:错 B:对
A:错 B:对
A:错 B:对
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!