广西师范大学
第一章单元测试
希托夫法测迁移数:用Ag电极电解AgNO3溶液,测出在阳极部AgNO3的浓度增加了x mol,而串联在电路上的Ag库仑计上有y mol Ag析出。则Ag+的迁移数为:( )。
298K时,有相同浓度的NaOH(1)和NaCl(2)水溶液,两溶液中的Na+的迁移数t1与t2之间的关系为:( )。
对于同一电解质的水溶液,当其浓度逐渐增加时,何种性质将随之增加:( )。
某一强电解质Mν+ Xν-,其平均活度a±与活度aB之间的关系是:( )。
下列电解质溶液中,离子平均活度系数最大的是:( )。
在饱和AgCl溶液中加入NaNO3,AgCl的饱和浓度如何变化:( )。
质量摩尔浓度为m的Na3PO4溶液,平均活度系数为γ±,则电解质的活度为: ( )。
浓度为0.1 mol kg–1的MgCl2水溶液,其离子强度为:( )。
Al2(SO4)3的化学势μ与Al3+和SO42–的化学势μ+、μ-的关系为:( )。
下列电解质水溶液中(浓度单位mol kg–1),摩尔电导率最大的是:( )。
298K时,Λm(LiI),Λm(H+),Λm(LiCl)的值分别为1.17×10–2、3.50×10–2和1.15×10–2 S m2 mol–1。LiCl中的t+为0.34,假设电解质完全电离,则HI中的t+ 为:( )。
浓度为1.0 mol dm–3的强电解质溶液,它的摩尔电导率数值近似于:( )。
在10 cm3的1 mol dm–3 KOH溶液中加入10 cm3水,其摩尔电导率将:( )。
欲要比较各种电解质的导电能力的大小,更为合理应为:( )。
CaCl2的摩尔电导率与其离子的摩尔电导率的关系是:( )。
LiCl的无限稀释摩尔电导率115.03×10–4 (S m2 mol–1),在298K时,测得LiCl稀溶液中Li+的迁移数为0.3364,则Cl-的摩尔电导率Λm(Cl-)为:( )。
298K、当HCl溶液的浓度从0.01 mol kg–1增加到0.02 mol kg–1时,其电导率κ和摩尔电导率Λm将: ( )。
浓度均为m的不同价型电解质,设1-3价型电解质的离子强度为I1,2-2价型电解质的离子强度为I2,则I1和I2的关系为:( )。
在一定温度和浓度的水溶液中,带相同电荷数的Li+、Na+、K+、Rb+ 、… 它们的离子半径依次增大,但其离子摩尔电导率恰也依次增大,这是由于:( )。
水溶液中氢和氢氧根离子的电淌度特别大,究其原因,下述分析哪个对:( )。
溶液是电中性的,正、负离子所带总电量相等,所以正、负离子的迁移数也相等。( )
离子迁移数与离子速率成正比,某正离子的运动速率一定时,其迁移数也一定。( )
- 离子的摩尔电导率与其价态有关系。( )
- 电解质溶液中各离子迁移数之和为1。( )
电解池通过1 F电量时,可以使1 mol物质电解。( )
因离子在电场作用下可以定向移动,所以测定电解质溶液的电导率时要用直流电桥。( )
无限稀电解质溶液的摩尔电导率可以看成是正、负离子无限稀摩尔电导率之和,这一规律只适用于强电解质。( )
电解质的无限稀摩尔电导率
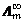 可以由Λm作图外推到c1/2 = 0得到。( )
可以由Λm作图外推到c1/2 = 0得到。( )若a(CaF2) = 0.5,则a(Ca2+) = 0.5,a(F-) = 1。( )
对于BaCl2溶液,以下等式成立:
(A) a = γm ; (B) a = a+·a - ; (C) γ± = γ+·γ - 2 ;
(D) m = m+·m- ; (E) m±3 = m+·m-2 ; (F) m± = 4m3 。
( )
A:
(x―y)/x
B:y/x
C:x/y
D:(y―x)/y
答案:
(y―x)/y
A:
无法比较
B:t1>t2
C:t1<t2
D:t1=t2
答案:
t1<t2
A:
电解质的离子平均活度系数
B:离子淌度
C:摩尔电导率
D:在稀溶液范围内的电导率
答案:
在稀溶液范围内的电导率
A:
a±=(aB)1/ν
B:a±=aBν
C:a±=(aB)2
D:a±=aB
答案:
a±=(aB)1/ν
A:
0.01 mol kg–1 NaCl
B:0.01 mol kg–1 CuSO4
C:0.01 mol kg–1 CaCl2
D:0.01 mol kg–1 LaCl3
答案:
0.01 mol kg–1 NaCl
A:
无法判定
B:变小
C:不变
D:变大
答案:
变大
A:
aB=4(m/mө)4(γ±)4
B:aB=4(m/mө)(γ±)4
C:aB=27(m/mө)(γ±)4
D:aB=27(m/mө)4(γ±)4
答案:
aB=27(m/mө)4(γ±)4
A:
0.15 mol kg–1
B:0.3 mol kg–1
C:0.1 mol kg–1
D:0.2 mol kg–1
答案:
0.3 mol kg–1
A:
μ=2μ++3μ-
B:μ=μ+ μ-
C:μ=μ++μ-
D:μ=3μ++2μ-
答案:
μ=2μ++3μ-
A:
HAc:0.001
B:KOH:0.001
C:KCl:0.001
D:HCl:0.001
答案:
HCl:0.001
A:
0.18
B:0.82
C:0.34
D:0.66
答案:
0.82
A:
与电导率相等
B:是电导率的10 3倍
C:是电导率的10 2倍
D:是电导率的10–3倍
答案:
是电导率的10–3倍
A:
不能确定
B:增加
C:不变
D:减少
答案:
增加
A:
电解质的电导率值
B:电解质的电导值
C:电解质的极限摩尔电导率值
D:电解质的摩尔电导率值
答案:
电解质的摩尔电导率值
A:
Λm∞(CaCl2)=2[Λ∞m(Ca2+)+Λ∞m(Cl-)]
B:Λm∞(CaCl2)=Λ∞m(Ca2+)+Λ∞m(Cl-)
C:Λm∞(CaCl2)=1/2[Λ∞m(Ca2+)]+Λ∞m(Cl-)
D:Λm∞(CaCl2)=Λ∞m(Ca2+)+2Λ∞m(Cl-)
答案:
Λm∞(CaCl2)=Λ∞m(Ca2+)+2Λ∞m(Cl-)
A:
76.33×10–4 S m2 mol–1
B:113.03×10–4 S m2 mol–1
C:76.33×102 S m2 mol–1
D:38.70×10–4 S m2 mol–1
答案:
76.33×10–4 S m2 mol–1
A:
κ增加,Λm 减小
B:κ减小,Λm 增大
C:κ减小,Λm 减小
D:κ增加,Λm增加
答案:
κ增加,Λm 减小
A:
I1=1.5I2
B:I1<I2
C:I1=I2
D:无法比较
答案:
I1=1.5I2
A:
离子的迁移数依次减小
B:离子的水化作用依次减弱
C:离子淌度依次减小
D:电场强度的作用依次减弱
答案:
离子的水化作用依次减弱
A:
离子荷质比大
B:发生质子传导
C:发生电子传导
D:离子水化半径小
答案:
发生质子传导
A:对 B:错
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:对
A:错 B:对
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:错
A:错 B:对
答案:错
A:错 B:对
答案:错
A:错 B:对
答案:错

