- 原电池是将电能转化成化学能的装置。( )
- 当氢原子与F、O、N原子以单键键合时,往往可以形成氢键。( )
- 极性分子中的化学键都是极性键。( )
- 在缓冲溶液中加入适量水稀释时,缓冲溶液的pH值完全不变 。( )
- 叶绿素与血红素都是配合物,而且是具有环状结构的螯合物。( )
- 微观粒子的运动和宏观物体一样都有固定的轨迹。( )
- 配位键形成的条件是:一个原子的价电子层有空轨道,另一个原子价电子层有孤对电子。( )
- 一般来说,溶液中离子浓度越大,离子强度越大,活度系数越小。( )
- KI溶液在空气中久置,可以使淀粉试纸变蓝。( )
- 某盐溶于水后,溶液的pH=7,则说明该盐不水解。( )
- 合理使用催化剂可以提高生成物的产量和产率。( )
- 质量相等的阻冻剂甲醛、乙醇、甘油效果相同。( )
- 催化剂只能改变反应速率,不能改变标准平衡常数。( )
- 氢原子中,E4s
- 基态原子有几个成单电子就能形成几个共价单键。( )
- 极性共价键可以认为是非极性键与离子键之间的一种过渡状态。( )
- 基态原子的电子层结构中,最外层电子数不超过8,次外层电子数不超过18,是由于”能级交错“造成的。( )
- Ag+只能形成外轨型配合物。( )
- 所有的同核原子形成的分子都是非极性分子,如P4,O2,N2,O3等。( )
- 根据分子轨道理论,下列双原子分子中,表现为顺磁性的是( )。
- 下列对于氢卤酸描述对的是( )。
- 关于Zn元素位于周期表中的位置,下列说法对的是( )。
- 下列不属于配合物的是( )。
- 将Ag+/Ag电对和Cu2+/Cu电对组成原电池,下列描述对的是( )。
- 对于铬酸盐和重铬酸盐,下列描述对的是( )。
- 对于过氧化氢,下列描述对的是( )。
- 关于[Cu(NH3)4]2+溶液,下列说法正确的是( )。
- 下列元素周期表的金属,描述对的是( )。
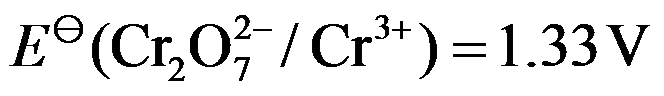
- 关于二元弱酸H2CO3,下列描述对的是( )。
- 298K,下列盐溶液中,pH内容已经隐藏,点击付费后查看
- 下列化学键或分子间力具有方向性和饱和性的是( )。
- 下列各组分子中,两分子之间仅存在诱导力和色散力的是( )。
- 在0.010 mol•L-1的H2S溶液中加入少量Na2S时,将会使H2S的( )。
- 下列配体中属于两可配体的是( )。
- S8中硫的氧化值为( )。
- 标况下,下列哪种中间价态的物质可自发进行歧化反应。( )
- 下列具有顺磁性的分子或离子是( )。
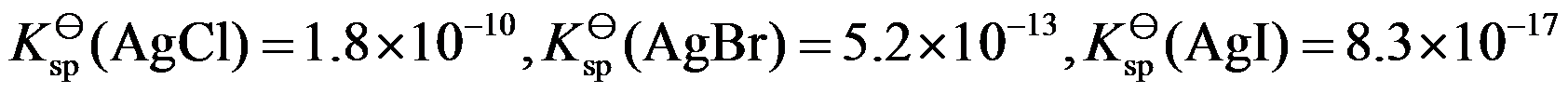
- 某A2B型难溶强电解质,在一定温度下,其溶度积常数为3.2×10-8,则其溶解度为( )mol•L-1。
- 主量子数等于4的电子层中包含的亚层数为( )。
- O2分轨道排布式是( )。
- [CrCl2(en)2]Cl配合物中,Cr3+的配位数为( )。
- 下列水溶液的渗透压最大的是( )。
- 下列物质中,可以用来鉴别Fe3+的是( )。
- 在Fe3+离子溶液中滴加KSCN溶液,生成[Fe(NCS)n]3-n配离子(n=1~6),则中心原子的配位数等于( )。
- 下列电子的各组量子数,可能存在的是( )。
- 当可逆反应达化学平衡时,下列叙述不对的是( )。
- 下列离子或分子中采取等性杂化的是( )。
- 下列哪个元素具有最多的氧化值。( )
- 在CaSO4饱和溶液中,加入少量下列试剂可以使CaSO4的溶解度减小。( )
- 某一氧化还原反应A+B2+=B+A2+,该反应的标准电动势为0.296 V,其标准平衡常数为( )。
- 量子数n,l和m不能决定( )。
- 已知[Co(NH3)6]3+的µ=0,Co3+采取的杂化方式为( )。
- 描述电子出现的最大概率区域距离原子核的平均距离的量子数是( )。
- 过一硫酸H2SO5中硫的氧化值为( )。
- 298K时,PbI2的溶度积常数为7.1×10-9,若将等体积的0.0010 mol·L-1的Pb(NO3)2溶液和0.0010 mol·L-1KI溶液混合,则( )。
- 下列影响盐类水解因素中,描述错误的是( )。
- 根据酸碱质子理论,H2O分子的共轭酸是( )。
- 下列四类硫酸盐,在酸性介质中,氧化性最强的是( )。
- 4d电子的电子云径向分布图中的峰的个数等于( )。
- 在浓度均为0.01 mol•L-1的Cl- 和I- 混合溶液中,不断逐滴加入稀硝酸银溶液,对于生成沉淀的说法正确是( )。
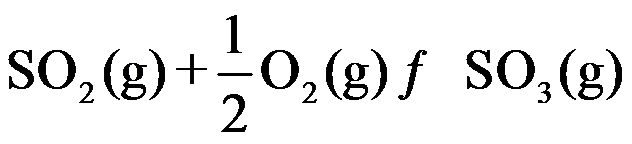
- 高锰酸根离子在碱性介质中和亚硫酸根离子反应生成锰酸根离子,该反应配平后,OH-的系数为( )。
- 下列外轨型配合物不可能采取的杂化方式为( )。
- 下列基态原子的价电子构型中,对的是( )。
- 已知,298K时AgCl和Ag2CO3的溶度积分别为1.8×10-10和8.1×10-12,在等浓度的氯离子和碳酸根离子的混合溶液中,逐滴加入硝酸银,则( )。
- MnO2中Mn的氧化值等于4,关于MnO2的说法正确的是( )。
- 下列分子中化学键键级等于零的是( )。
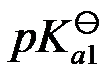
- 下列分子中采取不等性杂化的有( )。
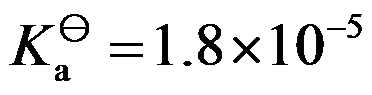
- 下列离子的盐溶液中,加入氢氧化钠,能产生氧化物沉淀的是( )。
- HgCl2和Hg2Cl2均是易电离的盐。( )
- 向二氯化汞溶液中,加浓氨水后生成( )。
- 关于Cu(Ⅰ)和Cu(Ⅱ)的性质,下列描述错误的是( )。
- 下列银配合物中,稳定性最强的是( )。
- 对于CuS的性质,下列描述错误的是( )。
- Cu2+与I-反应生成CuI2。( )
- 具有d10构型的银离子易形成配位数为2的直线形配离子。( )
- 中药用于安神镇静的朱砂是下列哪种化合物( )。
- 下列能用于检验醛类化合物的试剂有( )。
- 将硫化氢气体通入三氯化铁溶液中,可以得到Fe2S3。( )
- 下列不能形成氨配合物的离子是( )。
- 酸性介质中,Cr2O2- 7和H2O2反应的产物是( )。
- 常温下,MnO- 4和I-在强碱性溶液中发生氧化还原反应,产物最可能是( )。
- 高锰酸钾必须保存在棕色瓶中。( )
- 碱性介质中,CrO- 2能被H2O2氧化为Cr2O2- 7。( )
- 下列属于两性氢氧化物的有( )。
- 下列能将Mn2+氧化为MnO- 4的物质是( )。
- 下列用于实验室制备少量氯气的反应是( )。
- 检测微量Fe3+的特征试剂是( )。
- 常温下,Br2在碱中歧化为Br-和BrO-。( )
- 硝酸盐加热分解可以得到金属单质的是( )。
- 下列各酸中,酸性最强的是( )。
- 多数情况下,碳酸的热稳定性小于酸式盐,酸式盐的热稳定性小于相应正盐。( )
- P区元素的含氧酸中,既具有氧化性又具有还原性的是( )。
- 俗名是密陀僧的矿物药是( )。
- 卤化氢中,熔点最低的是( )。
- 硫代硫酸钠被I2氧化为硫酸钠,该反应是分析化学中碘量法的基础。( )
- 下列金属硫化物不能在水溶液中制备的是( )。
- 关于H2O2的性质,描述正确的是( )。
- 二氯二氨合铂有顺式与反式两种异构体,顺式称为顺铂,它的溶解度较大而且具有较强的抗肿瘤活性。( )
- [Ca(edta)]2-的中心原子的配位数等于( )。
- 配合物[Fe(CO)5]中心原子氧化值等于( )。
- 根据配合物价键理论,中心原子的配位数是由( )决定的。
- 碱金属与碱土金属都不能生成简单配合物,只能生成螯合物。( )
- 根据配合物价键理论,中心原子与配位体是通过( )键结合。
- 酸度太大或碱度太大都不利于某些配合物的稳定性。( )
- 所有配合物都是由外界和内界组成。( )
- 配合物的种类包括( )。
- 在Fe3+溶液中加入适量氟离子,下列说法错误的是( )。
- 若键轴为x轴,pz-pz轨道重叠形成π键。( )
- 下列分子中,不采取sp3杂化的有( )。
- 下列化合物中,属于离子型化合物的是( )。
- 下列分子中,偶极矩不为零的是( )。
- 非极性键组成的分子一定是非极性分子,极性键组成的分子一定是极性分子。 ( )
- 按照分子轨道理论,下列分子或离子中,键级最大的是( )
- 下列分子中,空间构型为是V形的是( )。
- Ar与H2O分子之间存在的分子间作用力有( )。
- 离子键和共价键一样既具有饱和性,又具有方向性。 ( )
- 电子云的角度分布图与原子轨道的角度分布图相比较,电子云的角度分布图“瘦”一些,而且没有正负号。( )
- 多电子体系中,下列四组量子数取值代表的电子能量最高的是( )。
- 4s电子云的壳层概率径向分布图中有( )个峰。
- 决定原子轨道形状的量子数是( )。
- 下列概念中,不是玻尔原子模型提出的是( )。
- 核外电子运动具有哪些特征( )?
- 能级分裂与能级交错现象可以用( )解释。
- Cu原子的基态电子层结构是( )。
- 元素周期表中所有原子基态的电子层结构都可以用核外电子填充的三个规则解释。( )
- 电子云小黑点图中黑点的疏密表示电子在该处出现的概率密度的大小。( )
- 下列关于原电池装置中盐桥的说法,错误的是( )。
- 标准电极电势值只与电极本性有关,与外界因素无关。( )
- 在酸性介质中,当溶液中H+浓度增加时,氧化能力增强的氧化剂是( )。
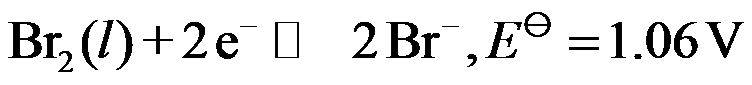
- 下列电对中标准电极电势值最小的是( )。
- 任一金属离子和金属单质组成的电对M2+/M,对于其电极电势E,下列说法错误的是( )。
- 标准状态下,下列两个反应均能正向进行:Cu + 2Fe3+ = 2Fe2+ + Cu2+ Fe2+ + Cl2 = Fe3+ + 2Cl- 由此可判断标准状态下,上述各物质中,最强的氧化剂是( )。
- 由反应Fe(s)+2Ag+(aq) = Fe2+(aq)+2Ag(s)组成的原电池,若将Ag+浓度增大到原来浓度的10倍,则电池电动势的变化为( )。
- 氧化剂电对的标准电极电势大于还原剂电对的标准电极电势,表明该氧化还原反应能够正向自发进行。( )
- 将0.1 mol/L AgNO3溶液分别加入到等体积含有0.1 mol/L氯离子和0.1 mol/L碘离子的溶液中,可能产生的现象是( )。
- 已知某AB型难溶强电解质的溶度积常数是1.0×10-10,其在纯水中的溶解度等于( )。
- 实验室中可以通过控制不同的pH值范围,使不同的氢氧化物、硫化物沉淀进行分离。( )
- 沉淀只能从溶解度大的向溶解度小的转化。( )
- 下列硫化物沉淀可以溶解于盐酸的是( )。已知HgS、CuS、MnS的溶度积分别是1.6×10-56、6.3×10-36、2.5×10-13。
- 溶液中某离子沉淀完全,并不是说该离子的浓度等于0,只是小于1.0×10-5 mol/L。( )
- 已知AgCl和Ag2CrO4的溶度积分别是1.8×10-10和1.1×10-12,则下列说法正确的是( )。
- 根据溶度积规则,沉淀溶解的必要条件是离子积大于溶度积。( )
- 同离子效应使难溶强电解质的溶解度减小。( )
- 下列有关分步沉淀叙述正确的是( )。
- 根据酸碱质子论,酸碱的强弱只与其本性有关。( )
- 相同浓度的氨水和氢氧化钠溶液的pH值相同。( )
- 在弱电解质溶液中,发生同离子效应时,弱电解质的电离度减小,因此不存在盐效应。( )
- 缓冲容量是用来衡量缓冲溶液缓冲能力大小的尺度,对于给定的缓冲对,和缓冲溶液的总浓度及二组分的比值有关。( )
- 下列0.1 mol/L溶液,显酸性的是( )。
- 在HAc-NaAc组成的缓冲溶液中,若c(HAc)
- 下列物质中,既是质子酸,又是质子碱的是( )。
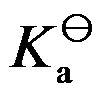
- 将0.1 mol/L下列溶液加水稀释1倍后,pH变化最小的是( )。
- 298K时,某一元弱碱溶液的浓度等于0.1 mol/L时,其电离平衡常数等于10-5,其溶液的pH等于( )。
- 达到化学平衡时,各反应物和生成物的浓度不再随时间而变化。( )
- 浓度的改变可以改变标准平衡常数的数值,从而影响化学平衡。( )
- 对于可逆反应 aA(g) + bB(l)→ cC(g)+ dD(s),增大气体总压,平衡正向移动,下列说法正确的是( )。
- 所有化学反应都可以达到化学平衡。( )
- 催化剂通过影响反应速率来影响化学平衡。( )
- 对于放热反应来说,升高温度会使其标准平衡常数变小。( )
- 标准平衡常数大于1,说明反应一定向着正反应方向进行。( )
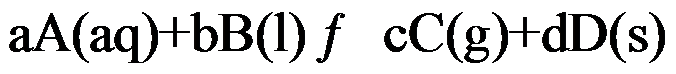
- 对于可逆反应 aA(g) + bB(l)→ cC(g)+ dD(s),升高温度,平衡正向移动,下列说法正确的是( )。
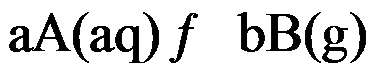
- 下列浓度表示方法中,与温度无关的是( )。
- 医学上, 下列哪些溶液是等渗溶液?( )。
- 为了防止水在仪器内结冰,可以在水中加入甘油或乙二醇。( )
- 质量摩尔浓度用下列哪个符号表示( )。
- 98℃下水沸腾时的压力是( )。
- 只要两个溶液之间存在浓度差就可以产生渗透压。
- 下面几种溶液的浓度都是0.1mol/L,①NaCl溶液,②蔗糖溶液,③CaCl2溶液。按照溶液的渗透压由高到低排列,顺序正确的是( )。
- 难挥发、非电解质、稀溶液的沸点升高的本质是( )。
- 溶液是由溶质和溶剂共同组成。( )
- 溶液只有液体形式。( )
- 正常大气压下水的沸点是多少度
答案:错
答案:对
答案:错
答案:错
答案:对
答案:错
答案:对
答案:对
答案:对
答案:错
答案:错
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!

