第一章 化学反应的热效应、方向和限度:化学反应千变万化,错综复杂,但实质上都是原子或原子团之间的重新组合,对化学反应规律的了解有助于我们主动地控制反应使其按照指定的方向进行。在一定条件下反应能否正向进行?能进行到什么程度?能提供多少热,做多少功?这些问题可在《化学反应的热效应、方向和限度》中找到答案。1.1第一节 热力学第一定律:介绍系统与环境、状态函数与状态方程、过程与途径、热与功、热力学能等热力学基本概念,阐述热力学第一定律的数学表达式,通过体积功的计算,引入可逆过程这一重要热力学概念。[单选题]不做非体积功时,刚性绝热箱内发生一化学反应,则该反应系统为
1.2第二节 化学反应的热效应:介绍反应热的概念,阐述利用Hess定律和各种热力学参数计算反应热的方法。
1.3第三节 热力学第二定律:从自发过程的特征入手,引入热力学第二定律和吉布斯能判据,介绍化学反应方向的判断方法。
1.4第四节 化学反应的限度和平衡常数:介绍标准平衡常数的表达方法,使用注意事项,以及温度对平衡常数的影响。
1.1第一节 热力学第一定律:介绍系统与环境、状态函数与状态方程、过程与途径、热与功、热力学能等热力学基本概念,阐述热力学第一定律的数学表达式,通过体积功的计算,引入可逆过程这一重要热力学概念。
1.2第二节 化学反应的热效应:介绍反应热的概念,阐述利用Hess定律和各种热力学参数计算反应热的方法。
1.3第三节 热力学第二定律:从自发过程的特征入手,引入热力学第二定律和吉布斯能判据,介绍化学反应方向的判断方法。
1.4第四节 化学反应的限度和平衡常数:介绍标准平衡常数的表达方法,使用注意事项,以及温度对平衡常数的影响。
选项:[绝热体系, 敞开体系 , 孤立体系, 封闭体系 ]
[单选题]下列参数中,属于广度性质状态函数的是
[单选题]
函数数值只与参与反应的物质数量有关。而与化学反应方程式写法无关的是
选项:[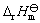 ,
, 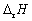 , K , ξ]
, K , ξ] [单选题]
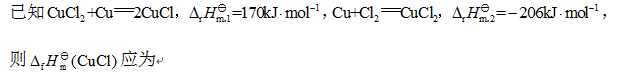
[单选题]
恒压过程中
[单选题]
化学反应的恒压热效应与恒容热效应之间关系是
[单选题]
CO2(g)的标准摩尔生成焓等于
[单选题]
N2 + 3H2 = 2NH3的反应进度 ξ = 1mol,表示系统中
[单选题]
在恒温恒压下,某一化学反应正向自发进行,一定是其
[单选题]

[单选题]

[单选题]

[单选题]
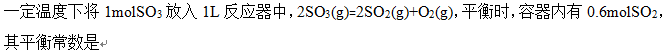
[单选题]

[单选题]
 选项:[ 吸热反应 , 既不吸热,也不放热 , 放热反应 , 无法确定 ]
选项:[ 吸热反应 , 既不吸热,也不放热 , 放热反应 , 无法确定 ] [单选题]由于ΔH=Qp,ΔU=Qv,故Qp,Qv是状态函数。
选项:[对, 错]
[单选题]稳定单质的标准摩尔熵等于零。
选项:[对, 错]
[单选题]系统与环境存在热交换时,系统的温度必定变化。
选项:[对, 错]
[单选题]当ξ=1时,表示该反应已经进行完全。
选项:[对, 错]
[单选题]
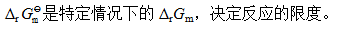
[单选题]

[单选题]
在恒温恒压下,某一化学反应正向自发进行,一定是其
[单选题]
N2 + 3H2 = 2NH3的反应进度 ξ = 1mol,表示系统中
[单选题]
CO2(g)的标准摩尔生成焓等于
[单选题]

[单选题]

[单选题]

[单选题]
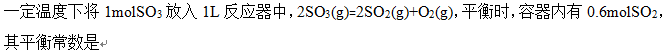
[单选题]稳定单质的标准摩尔熵等于零。
选项:[错, 对]
[单选题]系统与环境存在热交换时,系统的温度必定变化。
选项:[对, 错]
[单选题]
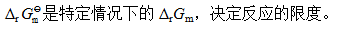
[单选题]当ξ=1时,表示该反应已经进行完全。
选项:[错, 对]
[单选题]
 选项:[ 无法确定 , 既不吸热,也不放热 , 放热反应 , 吸热反应 ]
选项:[ 无法确定 , 既不吸热,也不放热 , 放热反应 , 吸热反应 ] [单选题]由于ΔH=Qp,ΔU=Qv,故Qp,Qv是状态函数。
选项:[错, 对]
[单选题]不做非体积功时,刚性绝热箱内发生一化学反应,则该反应系统为
选项:[孤立体系, 绝热体系, 敞开体系 , 封闭体系 ]
[单选题]
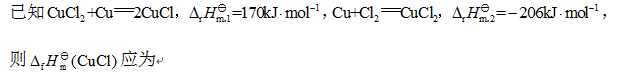
[单选题]下列参数中,属于广度性质状态函数的是
[单选题]
函数数值只与参与反应的物质数量有关。而与化学反应方程式写法无关的是
选项:[K , ξ,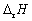 ,
, 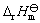 ]
] [单选题]
恒压过程中
[单选题]
化学反应的恒压热效应与恒容热效应之间关系是
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!

