第八章 原子结构与元素周期性:自然界存在着无数种物质,尽管性质千变万化,但它们都是由一百一十多种元素的原子按照一定的数目和方式结合而成的。性质取决于结构,原子结构的知识是了解物质性质的基础。本章运用量子力学的观点介绍原子核外电子的运动状态及其规律,揭示原子结构和性质之间的关系,为学习分子结构及性质提供基础。8.1第一节 微观粒子的运动特征:介绍微观粒子的波粒二象性及测不准原理,说明微观粒子的运动状态描述方法。[单选题]
8.2第二节 微观粒子运动的描述:介绍波函数和原子轨道,量子数的取值和组合,简介原子轨道的角度分布图。
8.3第三节 多电子原子的原子结构:介绍原子中电子填充的三大原则,阐述多电子原子组态的写法。
8.4第四节 元素周期表与元素性质的周期性:介绍原子的电子组态与元素周期表的划分方法,简介元素性质的周期性。
8.1第一节 微观粒子的运动特征:介绍微观粒子的波粒二象性及测不准原理,说明微观粒子的运动状态描述方法。
8.2第二节 微观粒子运动的描述:介绍波函数和原子轨道,量子数的取值和组合,简介原子轨道的角度分布图。
8.3第三节 多电子原子的原子结构:介绍原子中电子填充的三大原则,阐述多电子原子组态的写法。
8.4第四节 元素周期表与元素性质的周期性:介绍原子的电子组态与元素周期表的划分方法,简介元素性质的周期性。
29号元素Cu的基态电子组态为
[单选题]
基态Na原子(z = 11)最外层有一个电子,描述这个电子运动状态的四个量子数组合(n.l,m,s)是
[单选题]
下列元素的电负性大小顺序为
, C<Si<N<O<F
, Si<C<O<N<F
, C<N<O<F<S
]
[单选题]
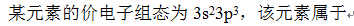
[单选题]
多电子原子中,能量最高的原子轨道是
, n = 2,l = 0
, n = 4,l = 0
, n = 3,l = 2
]
[单选题]
下图中表示基态Fe原子的3d和4s轨道中8个电子排布正确的是

,

,
 ,
, 
]
[单选题]电子云图中黑点越密集,表示在那里运动的电子越多。选项:[对, 错]
[单选题]将氢原子的1s电子激发至3s轨道或者3p轨道所需要的能量相等。选项:[对, 错]
[单选题]s电子在一个球面上运动,而p电子在一个双球面上运动。选项:[错, 对]
[单选题]只有当四个量子数组合合理时,才能确定电子的一种空间运动状态。选项:[对, 错]
[单选题]形状和伸展方向完全相同的原子轨道称为简并轨道。选项:[对, 错]
[单选题]中性基态原子的最后一个电子排在d轨道或s轨道上的,属于ds区。选项:[对, 错]
[单选题]
原子的电子排布式中出现3d4,意思是3个d轨道中有4个电子。
[单选题]
第三电子层最多可容纳的电子数为
[单选题]
原子轨道或波函数ψ可用来描述
[单选题]
当n = 4时,l最大取值应当是
[单选题]
决定氧原子轨道能量的量子数为
[单选题]
决定氢原子轨道能量的量子数为
[单选题]
决定核外电子运动状态的量子数组合是
选项:[n,m , n,l , n,l,m,s, n,l,m]
[单选题]
下列描述原子核外某电子运动状态的量子数组合(n、l、m、s),其中错误的是
[单选题]
原子轨道或波函数ψ可用来描述
[单选题]
第三电子层最多可容纳的电子数为
[单选题]
决定核外电子运动状态的量子数组合是
选项:[n,m , n,l,m,s, n,l , n,l,m]
[单选题]
决定氢原子轨道能量的量子数为
[单选题]
决定氧原子轨道能量的量子数为
[单选题]
当n = 4时,l最大取值应当是
[单选题]
下列描述原子核外某电子运动状态的量子数组合(n、l、m、s),其中错误的是
[单选题]
基态Na原子(z = 11)最外层有一个电子,描述这个电子运动状态的四个量子数组合(n.l,m,s)是
[单选题]
29号元素Cu的基态电子组态为
[单选题]
下图中表示基态Fe原子的3d和4s轨道中8个电子排布正确的是

,
 ,
, 
,

]
[单选题]
多电子原子中,能量最高的原子轨道是
, n = 3,l = 2
, n = 2,l = 0
, n = 4,l = 0
]
[单选题]
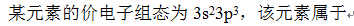
[单选题]
下列元素的电负性大小顺序为
, C<Si<N<O<F
, Si<C<N<O<F
, C<N<O<F<S
]
[单选题]形状和伸展方向完全相同的原子轨道称为简并轨道。选项:[对, 错]
[单选题]只有当四个量子数组合合理时,才能确定电子的一种空间运动状态。选项:[对, 错]
[单选题]s电子在一个球面上运动,而p电子在一个双球面上运动。选项:[对, 错]
[单选题]将氢原子的1s电子激发至3s轨道或者3p轨道所需要的能量相等。选项:[对, 错]
[单选题]电子云图中黑点越密集,表示在那里运动的电子越多。选项:[错, 对]
[单选题]
原子的电子排布式中出现3d4,意思是3个d轨道中有4个电子。
[单选题]中性基态原子的最后一个电子排在d轨道或s轨道上的,属于ds区。选项:[错, 对]

