青岛科技大学
- 原子轨道等性杂化前后其数目不变,只是能量变得完全相同,因而杂化以后形成的分子对称性更好,能量更低
- 碘易升华的原因是分子间作用力大,蒸气压高
- P4O10是最强的干燥剂之一,它可以夺取H2SO4中的H2O
- 同一体系,不同状态可能有相同的热力学能值
- 在共轭酸碱体系中,酸、碱的浓度越大,则其缓冲能力越强
- MnO4-在酸性溶液中歧化的主要产物是MnO42-和Mn3-
- 金刚石比石墨稳定,所以金刚石的标准生成焓等于零
- 电子就象云雾一样在原子核周围运动,故称为电子云
- 同一电子层的3个p轨道的能量形状大小都相同,不同的是在空间的取向
- 金属指示剂的作用原理是其酸式色和碱式色显著不同
- 林帮曲线是以pH为横坐标,lgKθMY为纵坐标的曲线,从该曲线上可以查出准确滴定单一金属离子时允许的pHmin
- 弱电解质的离解度随弱电解质浓度降低而增大
- 速率方程式中浓度的指数与化学计量系数一致,则反应一定为基元反应
- 离子型化合物中不可能含有共价键
- 在定温定容下,反应NH4Cl (s) NH3 (g) + HCl (g)达平衡,加入惰性气体平衡不移动
- NH4+离子中中心N原子采取的是不等性sp3杂化
- 配离子的电荷数等于中心离子的电荷数
- Ca2+,Mg2+离子共存时,可以通过控制溶液pH对Ca2+,Mg2+进行分别滴定。
- 平衡常数是衡量反应进行程度的特征常数,其大小只与温度有关,与计量数无关
- 只要组成缓冲溶液的两组分的浓度比接近1,缓冲溶液就具有很强的缓冲能力
- 下列热力学函数不等于零的是
- 下列物质能用酸碱滴定法直接准确滴定的是
- 下列物质碱性最强的是
- 对反应 2MnO4- + 3SO32- + H2O = 2MnO2 + 3 SO42- + 2OH-, △rGmθ = - zFE θ 中的z等于
- 下列关于热效应的说法不对的是
- 以为沉淀剂,采用重量法测定Ba2+离子,假如所得沉淀形中包藏了CaSO4,则测定结果会
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201811/bd996da7113b4dc397208f4bb54e7433.png
- AgCl沉淀可以溶解在氨水中,这是由于
- 配制pH = 9.2的缓冲溶液时,应选用的缓冲对是
- 下列物理量中与反应方程式的计量数无关的是
- 已知[Co(NH3)6]3+ 的磁矩μ = 0 B.M,则下列关于该配合物的杂化方式及空间构型叙述正确的是
- 下列叙述中错误的是
- 下列离子中和EDTA形成配合物稳定性最强的金属离子是
- NO2分子的空间构型是
- 某体系在失去15 kJ热给环境后,体系的内能增加了5 kJ,则环境对体系所作的功是
- 下列物质中可以用直接法配制标准溶液的是
- 用EDTA直接滴定有色金属离子M,终点所呈现的颜色是
- 下列电对中,若H+浓度增大,哪个电对的电极电势将不变
- 下列电子排布式中,原子处于激发状态的是
- 在草酸溶液中加入( )物质时,其解离度下降
- 在氨水中加入( )时,NH3·H2O的解离度下降,同时溶液的pH减小。
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201811/3f6796ea52944c4e94e9f80587390d40.png
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201811/4a4f09592c68434c8f75cd3a63dae3bc.png
- 在滴定分析中为了掩蔽Fe3+的干扰,可选用以下的哪种物质
- 下列盐属于正盐的是
- 某反应在298 K、100 kPa,正反应能自发进行,高温时逆反应能自发进行,说明该反应
- 测定(NH4)2SO4中的氮时,不能用NaOH标准溶液直接滴定,这是因为
- SO2分子的价键结构式中存在一种特殊的共价键为
- 一个阳离子使另一个阴离子变形能力增大的特性是
- http://image.zhihuishu.com/zhs/onlineexam/ueditor/201811/a9f959a143e8425f814cef0945bbf401.png
A:对 B:错
答案:A: 对
A:错 B:对
答案:A: 错 正确的说法应该是碘易升华的原因是分子间作用力相对较小,使得其蒸气压相对于其他固体物质在相同条件下较高。
A:对 B:错
答案:B: 错 P4O10(磷酐或磷酸酐)是一种非常强的干燥剂,但它并不会从H2SO4(硫酸)中夺取水,因为H2SO4本身是强酸并且具有很强的吸水性,通常用作干燥剂。P4O10一般用于干燥气体和其他物质,而不是用来从强酸如H2SO4中去除水。
A:对 B:错
答案:对
A:错 B:对
答案:错
A:对 B:错
答案:B: 错 MnO4- 在酸性溶液中歧化的主要产物是 Mn2+ 和 MnO2。
A:错 B:对
答案:A: 错
A:错 B:对
答案:B: 对
A:对 B:错
答案:对
A:错 B:对
A:错 B:对
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:DfGmq298.15(Fe,s ) B:Smq298.15(石墨,s) C:DfHmq298.15(石墨,s) D:DfHmq298.15(Br2,l)
A:苯酚钠(苯酚的
NaF(HF的=6.31×10-4)
A:Sn(OH)2 B:Sn(OH)4 C:Pb(OH)2 D:Pb(OH)4
A:10 B:6 C:3 D:2
A: 恒压反应热等于体系的焓变 B:对于固相或液相反应,公式ΔH = ΔU成立 C: 恒容反应热等于体系内能的变化 D:恒容反应热等于体系的焓变
A:偏低 B:不确定 C:偏高 D: 无影响
A:Fe3+,Fe2+ B:Sn4+,Fe2+ C:Sn4+,Sn2+ D:Fe3+,Sn2+
A: 盐效应 B:酸效应 C:配位效应 D:同离子效应
A:NH3-NH4Cl (Kb = 1.8 ´ 10–5) B: HAc-NaAc (Ka = 1.8 ´ 10–5) C: NaHCO3-Na2CO3 (Ka2 = 5.6 ´ 10–11) D:NaH2PO4-Na2HPO4 (Ka2 = 6.3 ´ 10–8)
A:
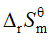 B:
B: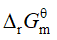 C:
C: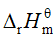 D:
D: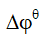
A:d2sp2,四方锥 B:sp3d2,正八面体 C:sp3d2 ,三方棱柱 D:d2sp3,正八面体
A:配合物的内界常比外界更不易解离 B:配合物必定是含有配离子的化合物 C:配位键与共价键没有本质区别 D:配位键由配体提供孤对电子,形成体接受孤对电子而形成
A:Ca2+ B:Ag+ C:Pb2+ D:Al3+
A:V形 B:平面三角形 C:三角锥形 D:直线形
A:20 kJ B:–10 kJ C:10 kJ D:–20 kJ
A:EDTA B:K2Cr2O7 C:Na2S2O3·5H2O D:KMnO4
A:指示剂-M络合物的颜色 B:EDTA-M 络合物的颜色 C:上述A+B的混合色 D:游离指示剂的颜色
A:Cr2O72-/Cr3+ B:Cl2/Cl- C:Fe(OH)3/ Fe(OH)2 D:MnO2/Mn2+
A:1s22s22p63s23p63d34s2 B:1s22s22p33s1 C:1s22s22p6 D:1s22s22p63s23p63d54s1
A:Na2C2O4 B:NH3·H2O C: NaCl D:加水稀释
A:水 B:NaCl C:HCl D:NH4Cl
A:在标准状态下,1 mol N2(g)和3 mol H2(g)完全作用生成2 mol NH3(g),可放出92.2 kJ的热 B:它表明在任何条件下NH3的合成过程是一放热反应 C:1 mol N2(g)和3 mol H2(g)反应可放出92.2 kJ的热量 D:按上述计量关系进行时生成1 mol NH3(g)可放热92.2 kJ
A:能,不能 B:不能,能 C: 能,能 D:不能,不能
A:H3PO4 B:HNO3 C:NH3 D:HCl
A:NaH2PO4 B:NaH2PO3 C:Na2HPO4 D:NaH2PO2
A:ΔH < 0,ΔS > 0 B:ΔH > 0,ΔS > 0 C:ΔH > 0,ΔS < 0 D:ΔH < 0,ΔS < 0
A:(NH4)2SO4中含游离H2SO4 B:(NH4)2SO4不是酸 C:NH4+的Ka太小 D:NH3 的Kb太小
A:σ键 B:
A:电荷大,半径大 B:电荷低,半径小 C:电荷高,半径小 D:电荷高,半径大
A:Ag2C2O4 B:AgCl C:AgBr D:Ag2CrO4
温馨提示支付 ¥5.00 元后可查看付费内容,请先翻页预览!

