第十四章测试1.HNO3的浓度越大,其氧化性越强。( )
A:对 B:错
答案:A
2.铜与浓HNO3反应生成NO2,铜与稀HNO3反应生成NO,所以稀HNO3的氧化性比浓HNO3强。( )
A:错 B:对 3. 固体铵盐受热分解产物因生成铵盐的酸的性质不同而异。( )
A:对 B:错 4. 所有固体铵盐的热分解产物中均有氨气。( )
A:错 B:对 5. 氮的最高氧化值为+5,可以推断NF5能稳定存在。( )
A:错 B:对 6. 硝酸盐易溶于水,所以常用作配位剂。( )
A:错 B:对 7.硼砂的化学式为Na2B2O7。( )
A:错 B:对 8. 硼在自然界主要以含氧化合物的形式存在。( )
A:错 B:对 9. 硼是非金属元素,但它的电负性比氢小。( )
A:错 B:对 10.Na2CO3比NaHCO3的溶解度大,同理,CaCO3比Ca(HCO3)2的溶解度也大。( )
A:对 B:错 11. 在硼的化合物中,硼原子的最高配位数不超过4,这是因为( )。
A:硼与配位原子电负性差小 B:配位原子半径小 C:硼的氧化值最大为3 D:硼原子无价层d轨道 12. 石墨中层与层之间的结合力是( )。
A:自由电子 B:大p键。 C:共价键 D:范德华力 13. 下列碳酸盐中,在加热时最易分解的是( )。
A:碳酸氢铵 B:碳酸钙 C:碳酸钾 D:碳酸铵 14.下列碳酸盐中,热稳定性最强的是( )。
A:碳酸银 B:碳酸钠 C:碳酸铅 D:碳酸铜。 15.下列硝酸盐受热分解,产生相应亚硝酸盐的是( )。
A:硝酸锂 B:硝酸铜 C:硝酸铅 D:硝酸钾 16. 硅酸盐的热稳定性主要取决于( )。
A:硅酸盐是离子化合物 B:硅-氧间能形成链状结构 C:硅-氧键的强度大 D:硅-硅键的强度大。 17.NaH2PO4的水溶液呈( )。
A:中性。 B:弱碱性 C:弱酸性 D:强碱性 18.下列分子或离子,与N2不是等电子体的是( )。
A:CO B:NO C:NO+。 D:CN- 19.下列离子或分子中
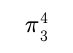 含键的是( )。
含键的是( )。A:硝酸 B:二氧化氮 C:硝酸根 D:亚硝酸 20.下列硝酸盐分解时,产物中不含有NO2的是( )。
A:硝酸镁 B:硝酸铍 C:硝酸锂 D:硝酸钠
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!
