第一章单元测试
与环境之间只有物质交换没有能量交换的系统,称为( )。
在系统的压力p、密度ρ、摩尔热容Cm和热力学能U等性质中,属于广度性质是( )。
在确定一定量某理想气体系统的状态时,只需给定系统的( )。
属于状态函数的是( )。
物质的量相同的理想气体从同一始态出发,分别经过恒温可逆膨胀到p1、V1和绝热可逆膨胀到p2、V2,两过程的体积功分别为W1和W2。若V1 =V2,正确的是( )。
物质的量相同的理想气体从同一始态出发,分别经过恒温可逆压缩到T1、V1和绝热可逆压缩到T2、V2,两过程的体积功分别为W1和W2。若V1 =V2,正确的是( )。
物质的量相同的理想气体从同一始态出发,分别经过恒温可逆、绝热可逆和绝热不可逆过程膨胀到相同的体积,三个过程的终态压力分别为p1、p2和p3,则正确的是( )。
关于焓的说法正确的是( )。
隔离系统中发生任意变化后,正确的是( )。
1mol 双原子理想气体从300 K、100kPa的始态,恒容变化到压力为200kPa的终态。过程
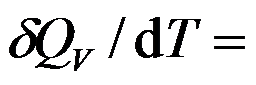 ( )J·mol-1·K-1。
( )J·mol-1·K-1。1mol双原子理想气体的
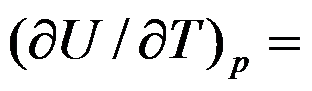 ( )。
( )。1mol双原子理想气体在恒容下温度升高1K,过程的ΔH =( )J。
关系式
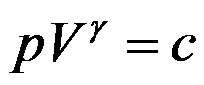 (c为常数)适用于( )。
(c为常数)适用于( )。一定量的理想气体从同一始态出发,分别经恒温可逆和绝热可逆两个过程压缩到相同压力的终态,两个终态的体积和焓分别为(V1、H1)和(V2、H2),则( )。
理想气体经节流膨胀过程后,则( )。
100℃、101.325kPa的液体水在恒温恒压下蒸发为100℃、101.325kPa的水蒸气,正确的是( )。
在一定温度和压力范围内,液体的摩尔蒸发焓随温度的变化率
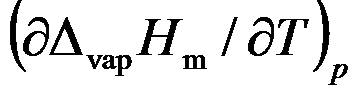 ( )。
( )。根据标准摩尔燃烧焓的定义,不正确的是( )。
已知A(g)、B(g)和C(l)的
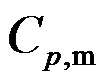 分别为10、20和40
分别为10、20和40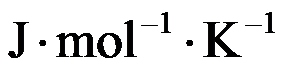 ,若反应2A(g)+B(g)→C(l)在500K时的
,若反应2A(g)+B(g)→C(l)在500K时的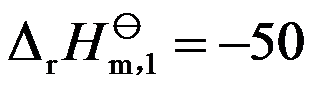
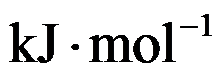 ,则反应在1000K时的
,则反应在1000K时的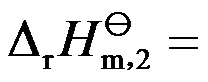 ( )
( )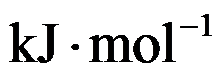 。
。卡诺(Carnot)循环(工作介质为理想气体)由恒温可逆膨胀、绝热可逆膨胀、恒温可逆压缩和绝热可逆压缩四个过程组成,各过程的体积功依次为
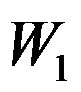 、
、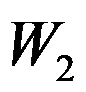 、
、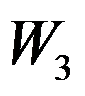 和
和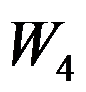 ,关系正确的是( )。
,关系正确的是( )。以水蒸气为工作介质,工作在240℃和30℃两热源之间热机的最大效率
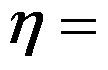 ( )%。
( )%。在温度为800K的高温热源和温度为300K的低温热源之间工作的卡诺(Carnot)热机,热机放给低温热源的热150kJ,则热机从高温热源吸热
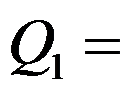 ( )kJ。
( )kJ。实际气体CO2经节流膨胀后,温度下降,则( )。
下列叙述中错误的是( )。
根据熵的统计意义,熵值增大的过程是( )。
实际气体经过绝热可逆压缩,过程的熵变( )。
1molAg(s)在等容下由273.15K加热到303.15K,已知在该温度区间内Ag(s)的CV,m=24.48J·K-1·mol-1,过程的熵变为( )。
计算熵变的公式
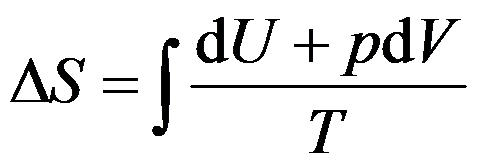 适用于( )。
适用于( )。300K时,2mol理想气体等温膨胀到体积加倍,过程的ΔS(J·K-1)( )。
公式ΔS=ΔH/T适用于( )。
属于恒熵过程的是( )。
热力学第三定律可以表述为( )。
恒温时,封闭系统中亥姆霍兹函数的降低值等于( )。
300K时,某一等温过程的
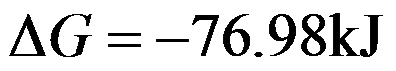 ,
,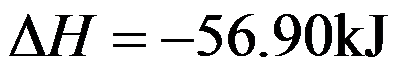 ,则
,则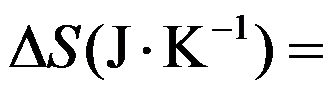 ( )。
( )。100℃、101.325kPa的液体水真空条件下蒸发成为100℃、101.325kPa下的水蒸气,正确的是( )。
在298K时,反应H2(g)+Cl2(g)=2HCl(g)的
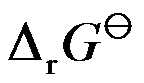 和
和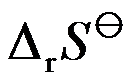 分别为
分别为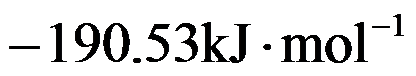 和
和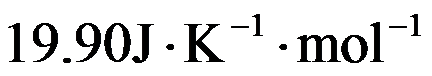 ,则HCl(g)的标准摩尔生成焓为( )。
,则HCl(g)的标准摩尔生成焓为( )。根据热力学基本方程式,
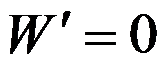 的封闭系统中
的封闭系统中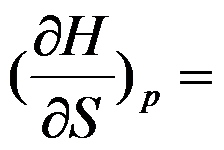 ( )。
( )。根据热力学基本方程式,
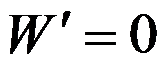 的封闭系统中
的封闭系统中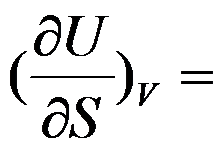 ( )。
( )。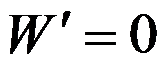 的封闭系统中,属于强度性质的偏微分是( )。
的封闭系统中,属于强度性质的偏微分是( )。恒外压变化过程,系统的终态压力一定等于外压。( )
对于封闭系统,若始态和终态确定后,热力学能有定值。( )
U 是状态函数,因为△U = QV,故QV是特定条件下的状态函数。( )
在没有发生化学反应且没有相变时,均相封闭系统升高单位热力学温度所吸收的热,称为热容。( )
因为
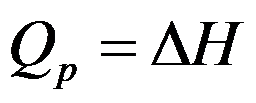 ,故公式
,故公式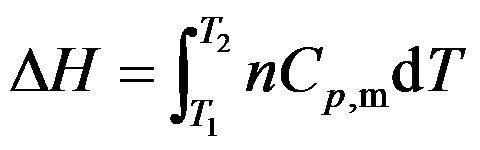 只适用于理想气体的恒压过程焓变的计算。( )
只适用于理想气体的恒压过程焓变的计算。( )因为
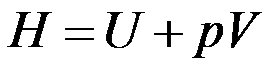 ,所以公式
,所以公式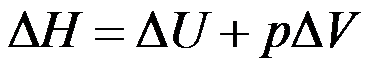 适用于一切变化过程。( )
适用于一切变化过程。( )若反应C(石墨)+1/2O2(g)→CO(g)和2C(石墨)+O2(g)→2CO(g)生成CO(g)物质的量相同,则它们的反应进度也相同。( )
实际气体的标准态是指任意温度、标准压力
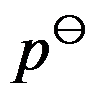 下表现出理想气体性质的纯气体状态。( )
下表现出理想气体性质的纯气体状态。( )热功转换的关系是,热可以无条件地全部转化为功,而功却不能无条件地全部转化为热。( )
从单一热源吸热后全部用来对外作功的热机,称为第一类永动机。( )
绝热循环过程一定是个可逆循环过程。( )
自发过程的熵变△S > 0。( )
理想气体等温可逆膨胀过程熵值不变。( )
封闭系统中理想气体的恒温变化过程,一定存在∆G = ∆A。( )
由物质的标准摩尔生成吉布斯(Gibbs)函数的定义可知,298K时
 。( )
。( )根据热力学基本方程式可知,
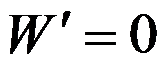 的封闭系统中偏微分
的封闭系统中偏微分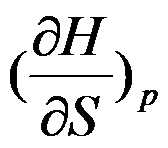 属于强度性质。( )
属于强度性质。( )根据热力学基本方程式可知,
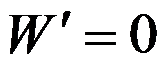 的封闭系统中偏微分
的封闭系统中偏微分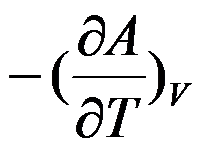 属于强度性质。( )
属于强度性质。( )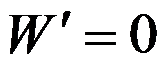 、体积一定的封闭系统中,热力学能随熵的增加而增加。( )
、体积一定的封闭系统中,热力学能随熵的增加而增加。( )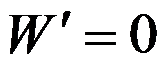 、压力恒定的封闭系统中,焓随熵的增加而增加。( )
、压力恒定的封闭系统中,焓随熵的增加而增加。( )
A:封闭系统 B:敞开系统 C:都不对 D:隔离系统
答案:都不对
A:p B:Cm C:ρ D:U
答案:U
A:V B:T,p C:p D:T,U
答案:T,p
A:H 和 W B:U 和 Q C:T 和 V D:Q 和 W
答案:T 和 V
A:p1<p2,W1>W2 B:p1<p2,W1<W2 C:p1>p2,W1<W2 D:p1>p2,W1>W2
答案:p1>p2,W1<W2
A:T1<T2,W1>W2 B:T1>T2,W1>W2 C:T1<T2,W1<W2 D:T1>T2,W1<W2
答案:T1<T2,W1<W2
A:p1<p3<p2 B:p1<p2<p3 C:p1>p3>p2 D:p1>p2>p3
答案:p1>p3>p2
A:封闭系统的焓等于U与pV之和 B:封闭系统的焓等于恒压热 C:封闭系统的绝对焓可知 D:封闭系统的焓变等于恒压热
答案:封闭系统的焓等于U与pV之和
A:ΔU=0,ΔH=0 B:ΔU=0,ΔH<0 C:ΔU=0,ΔH不确定 D:ΔU=0,ΔH>0
答案:ΔU=0,ΔH不确定
A:
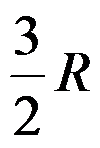 B:
B: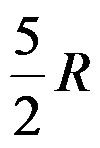 C:
C: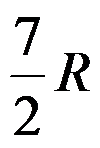 D:
D: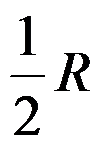
答案:
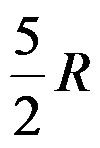
A:
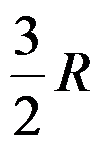 B:
B: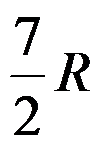 C:
C: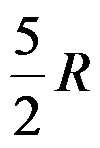 D:
D: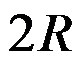
答案:
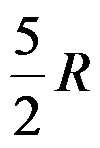
A:
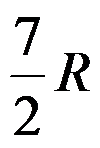 B:
B: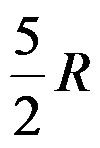 C:
C: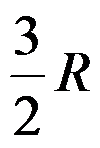 D:
D: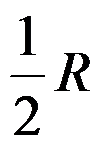
答案:
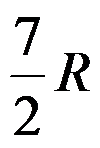
A:任何气体的可逆绝热过程 B:理想气体的可逆绝热过程 C:任何气体的绝热过程 D:理想气体的绝热过程
答案:理想气体的可逆绝热过程
A:V1>V2,H1<H2 B:V1<V2,H1<H2 C:V1>V2,H1>H2 D:V1=V2,H1=H2
答案:V1<V2,H1<H2
A:
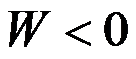 ,
,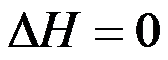 B:
B: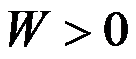 ,
,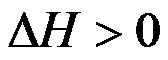 C:
C: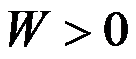 ,
,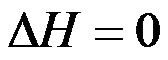 D:
D: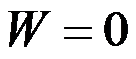 ,
,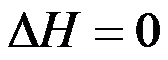
答案:
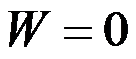 ,
,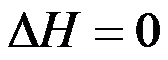
A:
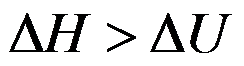
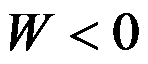 B:
B: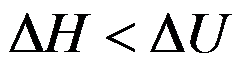
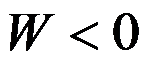 C:
C: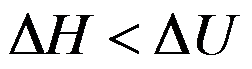
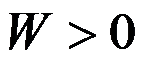 D:
D: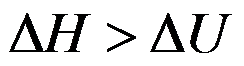
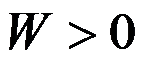
答案:
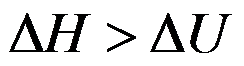
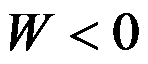
A:不确定 B:=0 C:>0 D:<0
答案:<0
A:
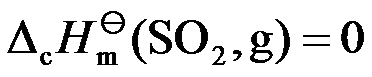 B:
B: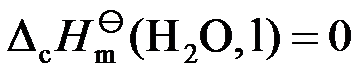 C:
C: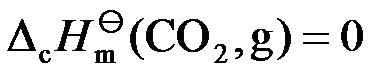 D:
D: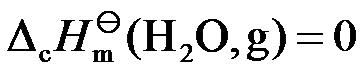
答案:
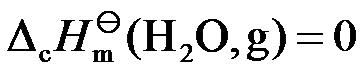
A:-30 B:-70 C:-55 D:-50
答案:-50
A:
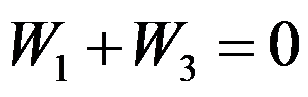 B:
B: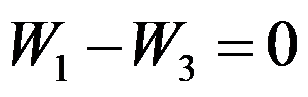 C:
C: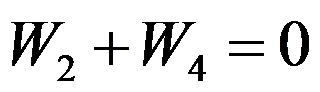 D:
D: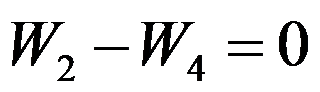
答案:
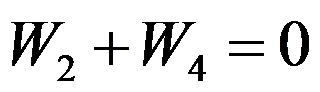
A:69.3 B:87.5 C:12.5 D:40.9
答案:40.9
A:-400 B:-240 C:400 D:240
答案:400
A:ΔS(体)>0,ΔS(环)=0 B:ΔS(体)<0,ΔS(环)>0 C:ΔS(体)<0,ΔS(环)=0 D:ΔS(体)>0,ΔS(环)<0
答案:ΔS(体)>0,ΔS(环)=0
A:熵是状态函数 B:熵增过程都是自发的 C:熵是用来衡量系统混乱程度的 D:“既要马儿跑,又要马儿不吃草”是不可能的
答案:熵增过程都是自发的
A:石灰石分解生成石灰 B:乙烯聚合成聚乙烯 C:水蒸气冷却成水 D:理想气体绝热可逆膨胀
答案:石灰石分解生成石灰
A:=0 B:不确定 C:<0 D:>0
答案:=0
A:25.51J·K-1 B:5.622J·K-1 C:56.22J·K-1 D:2.551J·K-1
答案:2.551J·K-1
A:无非体积功的封闭系统的简单状态变化 B:封闭系统的任意变化过程 C:理想气体的简单状态变化 D:理想气体的任意变化过程
答案:无非体积功的封闭系统的简单状态变化
A:5.76 B:11.52 C:-5.76 D:-11.52
答案:11.52
A:恒压过程 B:恒温过程 C:可逆相变过程 D:绝热过程
答案:可逆相变过程
A:理想气体的恒温可逆过程 B:某液体在正常沸点下的相变过程 C:理想气体的恒温不可逆过程 D:理想气体的绝热可逆膨胀过程
答案:理想气体的绝热可逆膨胀过程
A:0℃时纯物质晶体的熵值为零 B:0K时纯物质完美晶体的熵值为零 C:0K时纯物质晶体的熵值为零 D:0℃时纯物质完美晶体的熵值为零
答案:0K时纯物质完美晶体的熵值为零
A:可逆条件下系统对外所做体积功和非体积功的总值 B:系统对外所做体积功和非体积功的总值 C:系统对外所做非体积功的值 D:系统对外所做体积功的值
答案:可逆条件下系统对外所做体积功和非体积功的总值
A:-18.40 B:66.93 C:-66.93 D:703
答案:66.93
A:
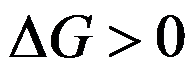 ,不可能
B:
,不可能
B: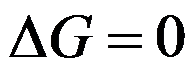 ,不可逆
C:
,不可逆
C: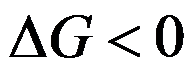 ,不可逆
D:
,不可逆
D: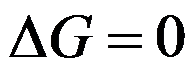 ,可逆
,可逆答案:
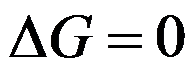 ,不可逆
,不可逆A:
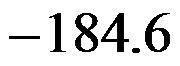
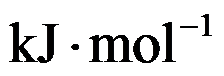 B:
B: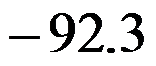
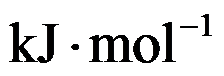 C:
C: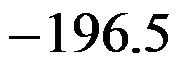
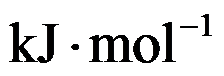 D:
D: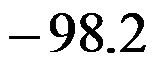
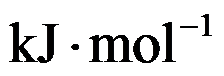
答案:
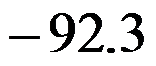
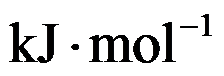
A:
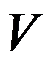 B:
B: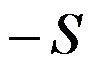 C:
C: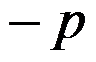 D:
D: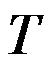
答案:
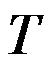
A:
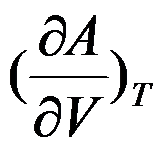 B:
B: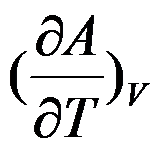 C:
C: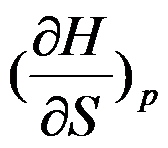 D:
D: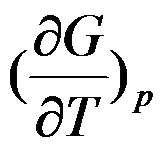
答案:
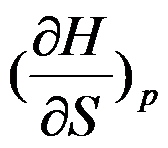
A:
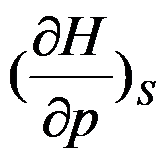 B:
B: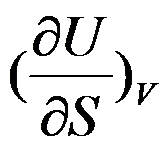 C:
C: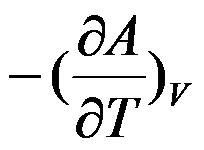 D:
D: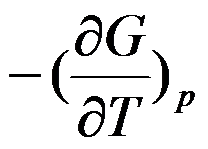
答案:
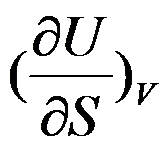
A:错 B:对
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:对
A:对 B:错
答案:错
A:错 B:对
答案:错
A:错 B:对
答案:对
A:对 B:错
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:错
A:错 B:对
答案:对
A:错 B:对
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:对


