第四章单元测试
NH4HS(s)和任意量的NH3(g)及H2S(g)达平衡时,平衡系统的相数P、组分数C和自由度数F分别为( )。
在101325Pa的压力下,I2在液态水与CCl4中的溶解已达到平衡(无固体I2存在),此体系的自由度为( )。
在0℃、不存在固体I2的情况下,一定量的碘溶于H2O-CCl4系统中的自由度F为( )。
单组分系统两相平衡时,下列关系式或说法正确的是( )。
方程
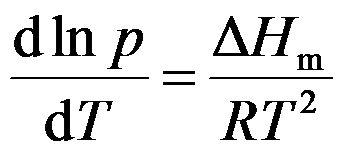 适用于( )过程。
适用于( )过程。某晶体的两种晶形,在转换温度附近的蒸气压随温度变化的关系为:
lgp1=﹣5082/T+11.364
lgp1=-5555/T+12.564
则两晶形的转换温度为( )。
关于三相点,下面说法中正确的是( )。
某一固体在25 ℃和101325 Pa压力下升华,这意味着( )。
在温度为T时,A(l)与B(l)的饱和蒸气压分别为30.0kPa和35.0kPa,A与B完全互溶,当xA=0.5时,pA=10.0kPa,pB=15.0kPa,则此两组分双液系常压下的T~x相图为( )。
在一定压力下,若在A、B二组分系统的温度-组成图(即T-xB)中出现最高恒沸点,则其蒸气总压对拉乌尔定律必产生( )。
已知A和B二组分可形成具有最低恒沸点(xB=0.7)的完全互溶双液系。若把xB=0.4的溶液进行精馏时,在塔顶得到的是( )。
对恒沸混合物的描述,下列各种叙述中不正确的是( )。
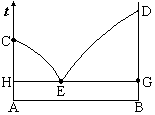
如图,对于形成简单低共熔混合物的两组分系统相图,当系统的组成为x,冷却到tºC时,固-液两相的重量之比是( )。

液体A与液体B不相混溶。在一定温度T0下,当有B存在并且达到平衡时,液体A的蒸气压应为( )。
如图,对于形成简单低共熔混合物的二组分系统相图,当系统点分别处于C、E、G点时,对应的平衡共存的相数为( )。
A及B两组分组成的凝聚系统能生成三种稳定的化合物,则于常压下在液相开始冷却的过程中,最多有( )种固相同时析出。
Na2CO3可形成三种水合盐:Na2CO3·H2O、Na2CO3·7H2O、NaCO3·10H2O,在常压下,将Na2CO3投入冰-水混合物中达三相平衡时,若一相是冰,一相是Na2CO3水溶液,则另一相是( )。
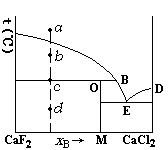
在CaF2-CaCl2的凝聚系统相图中,系统点为a,当降低系统温度时,不正确的是( )。
A和B两组分凝聚系统相图如图所示,在下列叙述中错误的是( )。
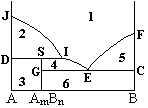
如图A与B是两组分恒压下固相部分互溶凝聚体系相图,图中有( )个单相。
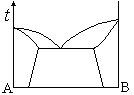
虽然相是均匀的,但并非一定要连续。( )
液体按其互溶程度可以是一相、也可以是两相或三相共存。( )
相图上系统点与相点都是分开的。( )
相图可表示出达到相平衡所需的时间长短。( )
依据相律,纯液体在一定温度下,蒸气压应该是定值。( )
在推导相律时,C个组分必须在每一相中都存在。( )
在使用克劳修斯-克拉佩龙方程时,物质的量只能取1mol。( )
三相点通常是在很靠近正常沸点的某一温度。( )
单组分单相系统是双变量系统,即系统的温度T和压力p可以同时改变,在p-T图中应是一个面。( )
水的三相点的温度是273.15 K,压力是610.62 Pa。( )
多组分液体的沸点是指在一定外压下,溶剂的蒸气压与外压相等时的温度。( )
在一定外压下,多组分体系的沸点随组分及浓度而变化。( )
对于对拉乌尔定律产生最大正偏差的二组分气液平衡系统,可以用蒸馏或者精馏的方法将两个组分分离成纯组分。( )
恒沸混合物与化合物一样,具有确定的组成。( )
在部分互溶双液系相图中,两条溶解度曲线把相图区域围出了一个帽形区。帽形区以外,溶液为单一液相;帽形区以内,溶液分为两相。( )
部分互溶双液系,一定温度下若出现气液两相平衡,则两相的组成与系统的总组成无关,且两相的量之比为常数。( )
部分互溶双液系,一定温度下若出现气液两相平衡,则两相的组成不定。( )
有一种不溶于水的有机化合物,在高温时易分解,欲将其提纯,可采用水蒸气蒸馏法。( )
在有化合物生成的固-液系统中,形成化合物的形式有多种,可以形成水和盐、复盐、复合氧化物、复合有机化合物以及两种金属形成的金属化合物等。( )
对于具有同种晶型,分子、原子或离子大小相近的两种物质,一种物质晶体中的粒子可以被另一种物质的相应粒子以任意比例取代,易形成固相完全互溶固-液系统。( )
A:
P=3,C=2,F=2
B:P=2,C=2,F=2
C:P=2,C=1,F=1
D:P=2,C=3,F=3
答案:
P=2,C=2,F=2
A:4 B:2 C:3 D:1
A:1 B:3 C:0 D:2
A:化学势是零 B:自由度是零 C:
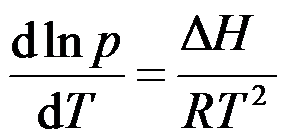 D:
D: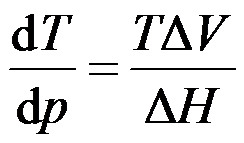
A:
NH4Cl(s)=NH3(g)+HCl(g)
B:H2O(s)=H2O(g)
C:H2O(s)=H2O(l)
D:NH4Cl(s)溶于水形成溶液
A:494.2K B:375.2K C:392.2K D:394.2K
A:三相点的温度可随压力改变 B:三相点是纯物质的三个相平衡共存时的温度和压力所决定的相点 C:三相点就是三条两相平衡线的交点 D:纯物质和多组分系统均有三相点
A:三相点压力大于101325Pa B:三相点温度小于25℃ C:三相点压力小于101325Pa D:固体比液体密度大
A:
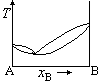 B:
B: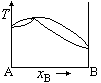 C:
C: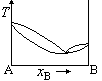 D:
D: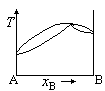
A:纯A B:不一定 C:纯B D:高共沸混合物
A:最低恒沸混合物 B:纯A(l) C:纯B(l) D:不确定
A:其沸点随外压的改变而改变 B:与化合物一样,具有确定的组成 C:不具有确定的组成 D:平衡时,气相和液相的组成相同
A:
m(s)∶m(l) = ac∶ab
B:m(s)∶m(l) = bc∶ac
C:m(s)∶m(l) = ac∶bc
D:m(s)∶m(l) = bc∶ab
A:与体系中A的摩尔分数成比例 B:等于T0下纯A的蒸气压 C:
与T0下纯B的蒸气压之和等于体系的总压
D:大于T0下纯A的蒸气压A:C点1,E点3,G点3 B:C点1,E点1,G点1 C:C点2,E点3,G点1 D:C点2,E点3,G点3
A:5 B:4 C:2 D:3
A:
Na2CO3·7H2O
B:Na2CO3·10H2O
C:Na2CO3
D:Na2CO3·H2O
A:
a点P = 1,F* = 2
B:c点P = 2,F * = 1
C:b点P = 2,F * = 1
D:d点P = 2,F * = 1
A:
J、F、E、I和S诸点F = 0
B:GC直线、DI直线上的点,F = 0
C:1为液相,P = 1,F = 2
D:要分离出纯AmBn,系统点必须在6区内
A:4 B:1 C:2 D:3
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:对 B:错


