第五章单元测试
在0.01mol·dm-3的CaCl2溶液中,Ca2+离子的迁移数为0.426,该溶液中Cl-的迁移数为( )。
在289K无限稀释的水溶液中离子摩尔电导率最大的是( )。
式
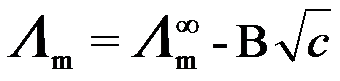 适用于( )。
适用于( )。在10 cm3 浓度为1mol·dm-3的KOH溶液中加入10 cm3水,其摩尔电导率将( )。
( )公式表示了离子独立移动定律。
电导测定应用广泛,但下列问题中( )是不能用电导测定来解决的。
电解质的活度a与正、负离子的活度a+、a-的关系为( )。
浓度为b的CaCl2溶液,下列关系式中正确的是( )。
0.3 mol·kg-1 Na2HPO4水溶液的离子强度是( )。
有4个浓度都是0.01mol·kg-1的电解质溶液,其中平均活度系数最大的是( )。
醌氢醌电极属于( )。
实验测定电池电动势时,采用了补偿法,这是为了( )。
采用对消法(或称补偿法)测定电池电动势时,需要选用一个标准电池。这种标准电池所具备的最基本条件是( )。
在298K时,已知Cu2++2e—=Cu,E1y = 0.337 V;Cu++e—=Cu,E2y= 0.521V,则反应Cu2++e—=Cu+的E3y 为( )。
在298K时,已知1/2Hg22++e—=Hg,E1y = 0.798 V;Hg2++2e—=Hg,E2y= 0.854V,则Hg2++e—=1/2Hg22+的E3y 为( )。
已知下列物质水溶液在一定浓度下其正离子迁移数 (tB)。选用( )作盐桥可使双液电池液体接界电势最小。
实验室里为测定由电极Ag|AgNO3(aq)及Ag, AgCl|KCl(aq)组成的电池的电动势,( )项是不能采用的。
当电池的电动势E=0时,表示( )。
标准氢电极的电极电势Ey (H2|H+)=0是指( )。
有两个电池,电动势分别为E1和E2:
H2(py)│KOH(0.1 mol·kg-1)│O2(py) ,E1
H2(py)│H2SO4(0.0l mol·kg-1)│O2(py) ,E2
比较其电动势大小( )。
298K时,在下列电池 Pt│H2(py)│H+(a=1)‖CuSO4(0.01 mol·kg-1)┃Cu(s) 右边溶液中加入0.1mol·kg-1Na2SO4溶液时(不考虑稀释效应),则电池的电动势将( )。
下列电池不属于浓差电池的是( )。
已知298K时,Hg2Cl2 +2e—= 2Hg + 2Cl—,E1y = 0.2676V;AgCl +e—=Ag + Cl—,E2y= 0.2224V,则当电池反应为Hg2Cl2 + 2Ag = 2AgCl +2Hg时,其电池的标准电动势为( )。
298K时反应Zn+Fe2+=Zn2+ +Fe的Ey为0.323V,则其平衡常数为( )。
298K时Ag2SO4+2e—=2Ag +SO42-的E1y为0.627V,而Ag+ + e—=Ag的E2y为0.799V,则Ag2SO4的活度积为( )。
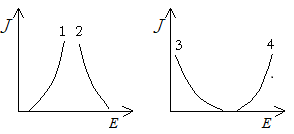
下列示意图描述了原电池和电解池中电极的极化规律,其中表示原电池阳极的是( )。
通电于含有相同浓度的Fe2+,Ca2+,Zn2+,Cu2+的电解质溶液,已知Ey (Fe2+|Fe) =-0.440V,Ey (Ca2+|Ca)= -2.866 V;Ey (Zn2+|Zn)=-0.7628V,Ey (Cu2+|Cu)=0.337 V,当不考虑超电势时,在电极上金属析出的次序是( )。
电解混合电解液时,有一种电解质可以首先析出,它的分解电压等于下列选项中( )的差值。(式中 E平、E阴和E阳分别代表电极的可逆电极电势和阴、阳极的实际析出电势)
Na+、H +的还原电势分别为 -2.17V和-0.83V,但用Hg作阴极电解NaCl溶液时,阴极产物是Na-Hg齐,这个现象的解释是( )。
Fe2+ + 2e ® Fe,E1,∆rGmӨ(1)
Fe3+ + e ® Fe2+,E2,∆rGmӨ(2)
(1) + (2),得:
(3) Fe3+ + 3e ® Fe,E3,∆rGmӨ(3)
则∆rGmӨ(3)=∆rGmӨ(1)+∆rGmӨ(2),E3=E1 + E2。( )
对于电极Pt |Cl2(p)|Cl- 其还原电极电势为:
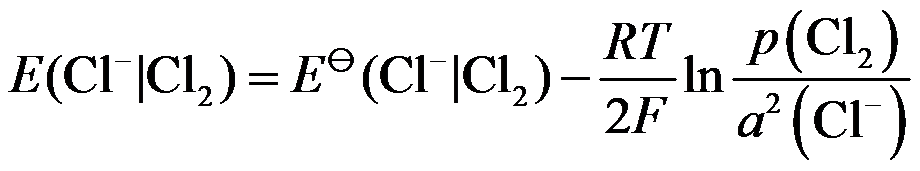 。( )
。( )电极产生极化的原因在于电极过程是很复杂的物理化学过程,各元过程的速率不一致,从而产生所谓的极化现象。( )
A:
0.574
B:0.426
C:0.218
D:0.852
答案:
0.574
A:
OH-
B:NO3-
C:SO42-SO42-
D:I-
A:弱电解质 B:强电解质的稀溶液 C:强电解质 D:无限稀溶液
A:不能确定 B:减小 C:增加 D:不变
A:
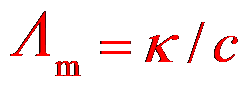 B:
B: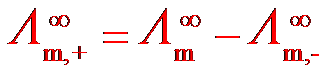 C:
C: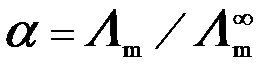 +
D:
+
D: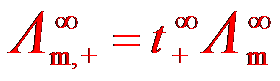
A:测电解质溶液的浓度 B:求离子的平均活度系数 C:求弱电解质的解离度 D:求难溶盐的溶解度
A:
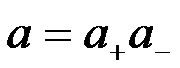 B:
B: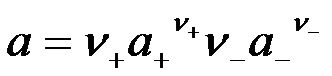 C:
C: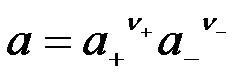
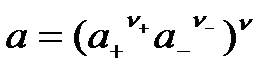
A:
a ± = 4γ± b/by
B:a = 4γ±3 b/by
C:a± = 41/3 γ± (b / by)
D:a =γ±3(b/by)3
A:
1.2 mol·kg-1
B:0.3 mol·kg-1
C:1.8 mol·kg-1
D:0.9 mol·kg-1
A:
CaCl2
B:AlCl3
C:Na2SO4
D:KCl
A:第一类电极 B:第三类电极 C:离子选择电极 D:第二类电极
A:维持回路电流接近于零 B:维持回路电流保持恒定 C:维持回路电压接近于零 D:维持回路电压保持恒定
A:高度可逆,电动势温度系数小,稳定 B:电极反应的交换电流密度很大,可逆性大 C:电动势精确已知,与测量温度无关 D:电池可逆,电势具有热力学意义
A:0.153 V B:0.184V C:-0.184 V D:-0.153V
A:0.056V B:0.910 V C:-0.056V D:-0.910 V
A:
KNO3 (t(K+)= 0.5103)
B:BaCl2 (t(Ba2+) = 0.4253)
C:NaCl (t(Na+) = 0.3854)
A:直流检流计 B:标准电池 C:电位计 D:饱和的KCl盐桥
A:电池反应的平衡常数Ka=1 B:正极与负极的电极电势相等 C:电池反应中,反应物的活度与产物活度相等 D:电池中各物质都处于标准态
A:在任何温度时 B:273K时 C:298K时 D:在临界温度时
A:不能确定 B:
E1= E2
C:E1> E2
D:E1< E2
A:无法判断 B:下降 C:上升 D:基本不变
A:
Na(Hg)(A)| NaCl(m1)|AgCl(s)|Ag(s)—Ag(s)|AgCl(s)| NaCl(m2)|Na(Hg)(A)
B:Na(Hg)(A)|NaCl(m1)|| NaCl(m2)|Na(Hg)(A)
C:Ag(s)|AgCl(s)|NaCl(aq)|Na(Hg)(A)|NaCl(CH3CN溶液)|Na(s)
D:Tl(Hg)(a1)|Tl+(aq)|Tl(Hg)(a2)
A:-0.1772V B:0.0276V C:-0.0886V D:0.0452V
A:
2.35×102
B:8.32×1010
C:2.89×105
D:5.53×104
A:
1.2×10-3
B:1.51×10-6
C:3.8×10-17
D:2.98×10-3
A:曲线3 B:曲线1 C:曲线4 D:曲线2
A:Ca → Fe → Zn → Cu B:Ca → Cu → Zn → Fe C:Cu → Fe → Zn → Ca D:Ca → Zn → Fe → Cu
A:
E阳 + E阴
B:E阳(最小) - E阴(最大)
C:E阳(最大) - E阴(最小)
D:E平,阳- E平,阴
A:还原电势预示Na更易析出 B:其余选项都不正确 C:氢在汞电极上的超电势可能超过1.5V D:Na和Hg形成液体合金
A:对 B:错
A:错 B:对
A:错 B:对


