第三章单元测试
在恒温恒压下,一个化学反应的
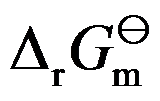 是指参加反应的各物质在下列哪种情况下反应吉布斯函数变( )。
是指参加反应的各物质在下列哪种情况下反应吉布斯函数变( )。已知温度 T 时反应
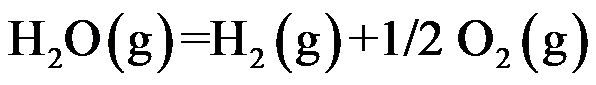 的标准平衡常数
的标准平衡常数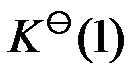 及反应
及反应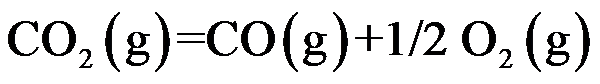 的标准平衡常数
的标准平衡常数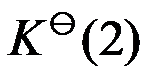 ,则同温度下反应
,则同温度下反应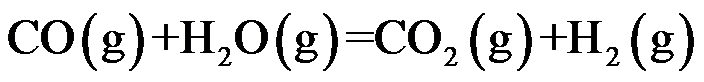 的标准平衡常数
的标准平衡常数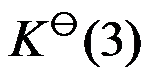 应为( )。
应为( )。对于反应
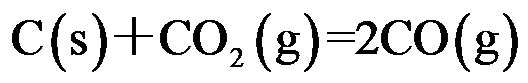 ,下列各式正确的是( )。
,下列各式正确的是( )。假设各反应中的气体都是理想气体,则
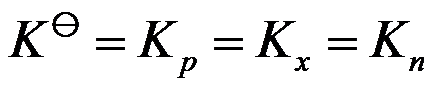 的反应是( )。
的反应是( )。900℃时反应:
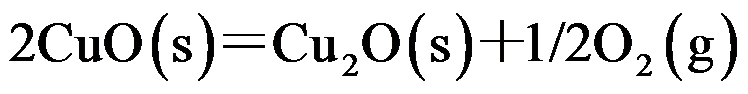 的
的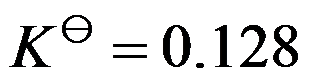 ,则其平衡分解压力为( )。
,则其平衡分解压力为( )。在标准状态下,
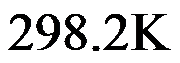 时,氧化汞的分解反应:
时,氧化汞的分解反应: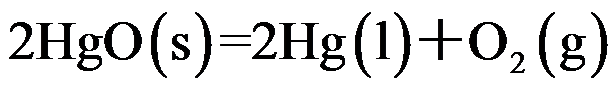 的分解压力为
的分解压力为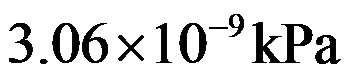 ,
,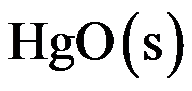 的标准摩尔生成吉布斯函数是( )
的标准摩尔生成吉布斯函数是( )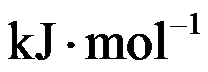 。
。反应
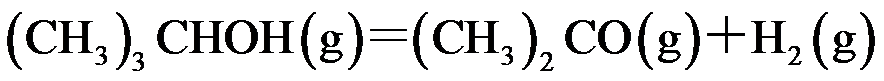 ,在457.4 K 时
,在457.4 K 时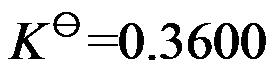 ,
,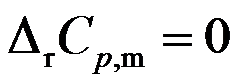 ,在500 K时
,在500 K时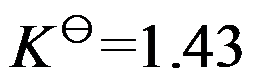 ,则
,则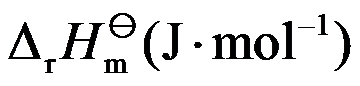 为( )。
为( )。巳知反应
 ;
;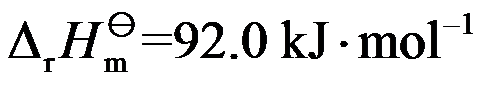 ;
;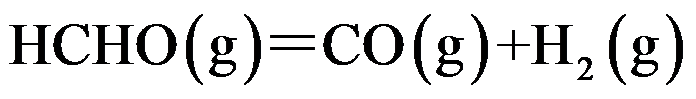 ;
;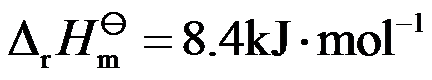 。若要提高平衡混合物中HCHO的含量, 应采取( )。
。若要提高平衡混合物中HCHO的含量, 应采取( )。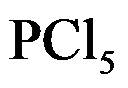 的分解反应是
的分解反应是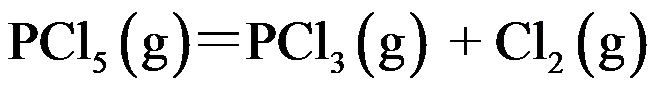 ,在 473 K 达到平衡时,
,在 473 K 达到平衡时,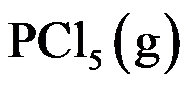 有 48.5% 分解,在 573 K 达到平衡时,有 97% 分解,则此反应为( )。
有 48.5% 分解,在 573 K 达到平衡时,有 97% 分解,则此反应为( )。平衡常数
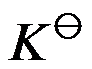 与温度 T 的关系为
与温度 T 的关系为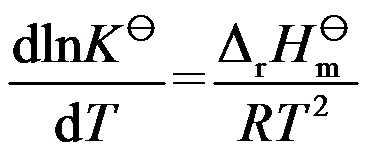 ,当温度升高时,
,当温度升高时,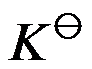 应该( )。
应该( )。对于反应
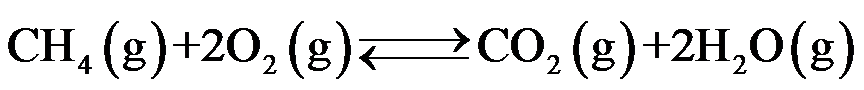 ,在恒温下,增加反应系统的平衡压力,使其体积变小,这时,y(CO2)( )。
,在恒温下,增加反应系统的平衡压力,使其体积变小,这时,y(CO2)( )。在
 反应中,若增加压强或降低温度,B的转化率均增大,则反应体系应是( )。
反应中,若增加压强或降低温度,B的转化率均增大,则反应体系应是( )。等温等压下加入惰性气体,对正反应有利的是( )。
对于反应
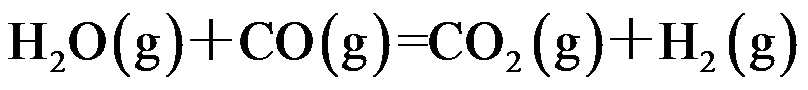 ,下列哪些因素变化,不影响其转化率( )。
,下列哪些因素变化,不影响其转化率( )。由反应
①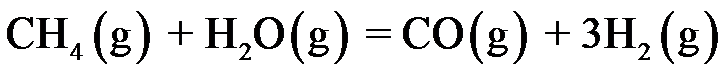 ②
②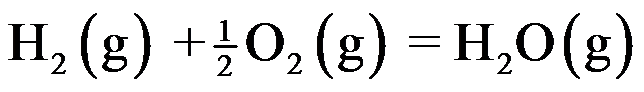 ③
③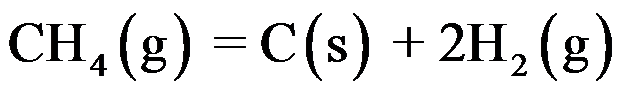
④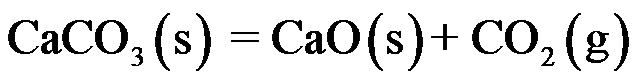 构成的几组反应中都可以建立同时平衡的是( )。
构成的几组反应中都可以建立同时平衡的是( )。因为
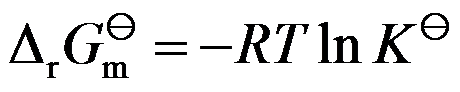 ,所以
,所以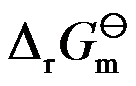 是平衡状态时的吉布斯函数变化。( )
是平衡状态时的吉布斯函数变化。( )对于理想气体混合物的反应,该反应的标准平衡常数仅仅是温度的函数。( )
已知 298 K 时,
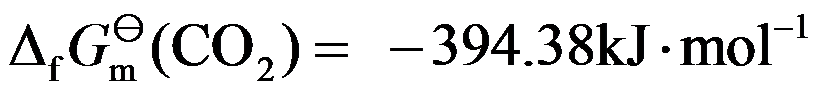 ,
,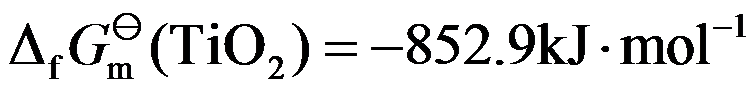 ,则在 298 K 的标准态下,可以直接用碳来还原TiO2。( )
,则在 298 K 的标准态下,可以直接用碳来还原TiO2。( )在等温等压条件下,
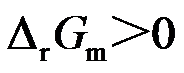 的反应一定不能进行。( )
的反应一定不能进行。( )等温、等压且无非体积功的条件下,一切吸热且熵减少的过程,都不能自发进行。( )
温度T 时,若
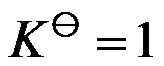 ,说明这个反应在此温度,压力为 100kPa 的条件下已达到平衡。( )
,说明这个反应在此温度,压力为 100kPa 的条件下已达到平衡。( )在有纯凝聚相参加的理想气体反应中,
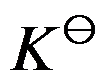 的表示式不包含液体(或固体)的分压。( )
的表示式不包含液体(或固体)的分压。( )若已知
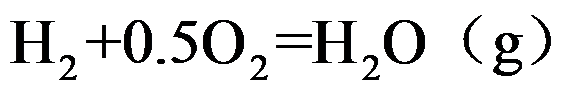 的平衡组成,则能求得
的平衡组成,则能求得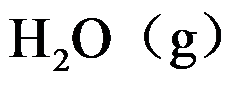 的标准摩尔生成吉布斯函数。( )
的标准摩尔生成吉布斯函数。( )因
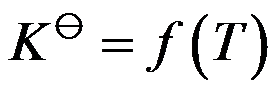 ,所以对理想气体的化学反应,当温度一定时,其平衡组成也一定。( )
,所以对理想气体的化学反应,当温度一定时,其平衡组成也一定。( )根据反应体系的平衡组成的测定可以计算该反应的热力学的变化值。( )
温度升高平衡常数增大的反应一定是吸热反应。( )
对于理想气体反应
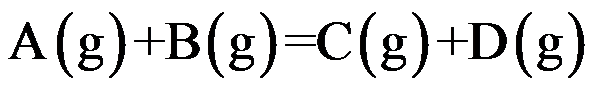 ,其标准平衡常数与温度关系为
,其标准平衡常数与温度关系为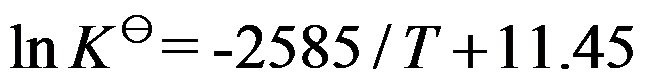 ,则
,则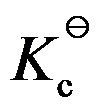 与温度的关系为
与温度的关系为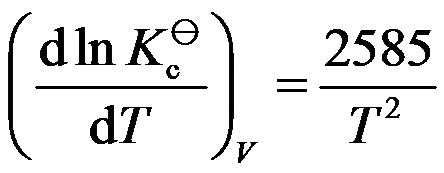 。( )
。( )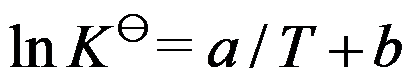 ,升高温度,平衡向右移动,则
,升高温度,平衡向右移动,则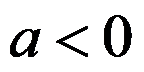 ,
,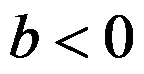 。( )
。( )对摩尔数增加的反应和摩尔数减小的反应,温度对反应平衡的影响不同。( )
压力增大,平衡正向移动的理想气体反应一定是摩尔数减小的反应。( )
对于摩尔数增加的理想气体反应,充入惰性气体,平衡一定正向移动。( )
同时平衡体系中有几个反应,就可以列出几个独立的平衡常数表示式来计算平衡组成。( )
改变压力,同时平衡体系中的一个反应的组成发生改变,另一个反应的组成可能不变。( )
A:化学平衡时 B:浓度不变时 C:可逆反应中 D:标准态时
答案:标准态时
A:
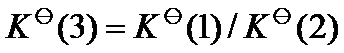 B:
B: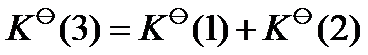 C:
C: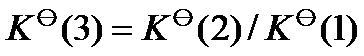 D:
D: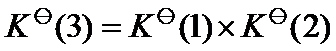
A:
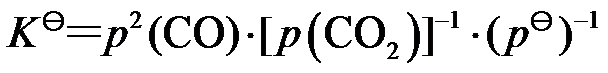 B:
B: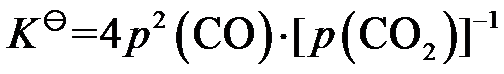 C:
C: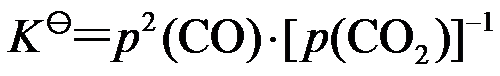 D:
D: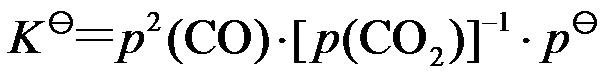
A:
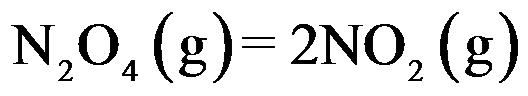 B:
B: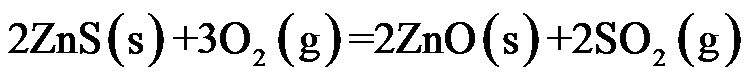 C:
C: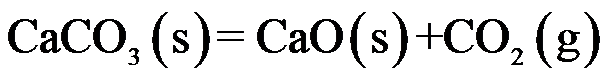 D:
D: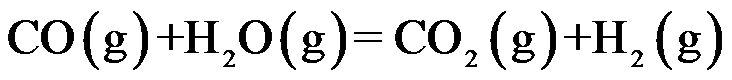
A:1638.14Pa B:12969.6 Pa C:791348.25 Pa D:835.9 Pa
A:30.0 B:-60.0 C:-30.0 D:60.0
A:0.615 B:6.15 C:6.150×103 D:6.150×104
A:升高温度 B:增加压力 C:减小压力 D:降低温度
A:吸热反应 B:即不放热也不吸热 C:这两个温度下的平衡常数相等 D:放热反应
A:不变 B:增大 C:不能判断 D:减小
A:不变 B:变大 C:变小 D:无法确定
A:A是气体,C是固体,正反应放热 B:A是固体,C是气体,正反应吸热 C:A是气体,C是气体,正反应放热 D:A是气体,C是气体,正反应吸热
A:
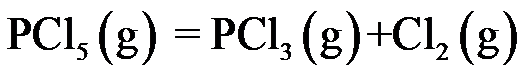 B:
B: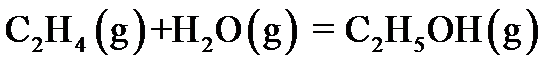 C:
C: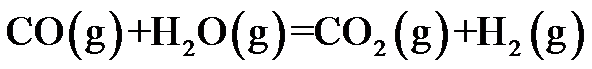 D:
D: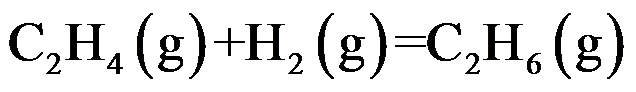
A:通入 H2 气 B:降低温度同时增加压力 C:通入惰性气体 D:升高温度
A:②、③、④ B:①、②、③ C:①、②、④ D:①、③、④
A:错 B:对
A:对 B:错
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对


