第二章
+2
0
+2.5
答案:+2
若其他物质均处于标准态,溶液pH由0变到5时,电极电位改变最大的是
Cr2O72-/Cr3+
O2/H2O2
BrO3-/Br-
答案:Cr2O72-/Cr3+
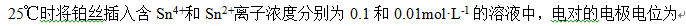
答案:
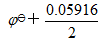
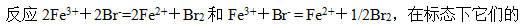
答案:
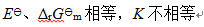
若电池电动势为负值,表示此电池反应的方向是
不确定
正向
不能进行
答案:逆向

答案:

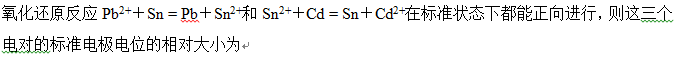
答案:
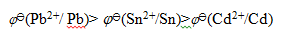
根据KCl溶液浓度,常用甘汞电极分为饱和甘汞电极、摩尔甘汞和0.1mol·L-1甘汞电极。其电极反应为Hg2Cl2(s)+2e=2Hg(l)+2Cl-(aq),设饱和甘汞电极、摩尔甘汞电极和0.1mol·L-1甘汞电极的电极电势分别为φ1、φ2、φ3,则室温下,三者的相对大小为
答案:φ1<φ2<φ3
CH4中C与4个H形成四个共价键,因此C的氧化数是4。
答案:错
组成原电池的两个电对的电极电位相等时,电池反应处于平衡状态。
答案:对
电极电位只取决于电极本身的性质,而与其他因素无关。
答案:错
原电池的电动势越大,电池反应的速率越快。
答案:错
电极电位与电池的电动势与反应进度有关。
答案:错
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!

