第一章单元测试
- 热和功是状态函数。( )
- 体系和环境的划分是相对的。( )
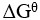 =0,意味着体系处于平衡态。( )
=0,意味着体系处于平衡态。( )- 一个反应的ΔG值越负,其自发进行的倾向越大,反应速率越快。( )
- 在298K时,Mg的熵为零。( )
- 熵增反应是自发反应。( )
- 热力学第一定律是公理。( )
- ΔG < 0,反应自发进行。( )
U和ΔU都是状态函数。( )
- 任何过程的熵就是该过程的热温商。( )
- 实际气体和理想气体更接近的条件是( )。
- NH4NO3能溶于水,是一吸热过程,下列答案正确的是( )。
- 封闭体系是指该体系与环境之间( )。
- 有一个盛满热水的烧杯,当研究烧杯中的热水时,则此体系为( )。
- 对任一过程( )。
下列反应中ΔS<0的反应为( )。
- 公式 Qp = ΔH 的适用条件是( )。
- 下列反应中,吉布斯函数变符合标准生成吉布斯函数定义的反应是( )。
已知
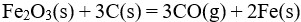 反应的
反应的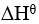 为正,
为正,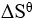 为正(假定
为正(假定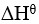 和
和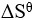 不随温度而变),下列说法正确的是( )。
不随温度而变),下列说法正确的是( )。在1173K,101.3kPa时,某反应的
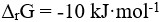 ,这表明( )。
,这表明( )。
A:对 B:错
答案:错
A:对 B:错
答案:对
A:错 B:对
答案:错
A:错 B:对
答案:错
A:错 B:对
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:对
A:对 B:错
答案:错
A:对 B:错
答案:错
A:对 B:错
答案:错
A:高温低压 B:低温低压 C:高温高压 D:低温低压
答案:高温低压
A:ΔG<0, ΔH>0, ΔS<0 B:ΔG<0, ΔH>0, ΔS>0 C:ΔG>0, ΔH>0, ΔS>0 D:ΔG<0, ΔH<0, ΔS>0
答案:ΔG<0, ΔH>0, ΔS>0
A:没有物质和能量交换 B:没有物质交换,只有能量交换 C:有物质和能量交换 D:只有物质交换,没有能量交换
答案:没有物质交换,只有能量交换
A:敞开体系 B:绝热体系 C:孤立体系 D:封闭体系
答案:敞开体系
A:体系所做的功与途径无关 B:体系所吸收的热量与途径无关 C:体系的内能变化与途径无关 D:体系的焓与途径无关
答案:体系的内能变化与途径无关
A:
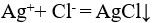
答案:
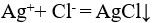
A:恒容过程 B:恒压过程 C:恒压须做体积功的过程 D:恒压不做非体积功的过程
答案:恒压不做非体积功的过程
A:Na(s) + 1/2 Cl2(g) = NaCl(s) B:1/2 H2(g) + 1/2 I2(g) = HI(g) C:S(单斜) + O2(g) = SO2(g) D:2C(石墨) + O2(g) = 2CO(g)
答案:Na(s) + 1/2 Cl2(g) = NaCl(s)
A:任何温度下均为自发过程 B:低温下自发过程,高温下非自发过程 C:任何温度下均为非自发过程 D:高温下自发过程,低温下非自发过程
答案:高温下自发过程,低温下非自发过程
A:该反应在1173K和101.3kPa条件下,反应是自发的 B:该反应是自发反应 C:该反应是放热反应 D:该反应在任何条件下均不自发
答案:该反应在1173K和101.3kPa条件下,反应是自发的
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!


