第三章单元测试
酸性水溶液中不含
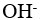 ,碱性水溶液中不含
,碱性水溶液中不含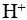 。( )
。( )将
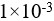
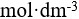 的HCl溶液稀释1000倍,则溶液的pH=8。( )
的HCl溶液稀释1000倍,则溶液的pH=8。( )- 在一定温度下,改变溶液的pH,水的离子积不变。( )
同浓度、等体积的HCl和HAc溶液,由于HAc解离出的H+浓度小,用NaOH滴定至化学计量点,HAc所需的NaOH量就少。( )
- 难溶电解质的溶解度大小可以根据难溶电解质的溶度积大小直接比较,即:溶度积较大的,溶解度较大;溶度积较小的,溶解度较小。( )
- 弱电解质的解离度随着溶液的稀释逐渐增大,解离出的离子浓度也会逐渐增大,解离常数也增大。( )
1
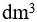 1.0
1.0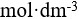 的NaOH溶液与0.1
的NaOH溶液与0.1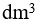 2.0
2.0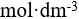 的
的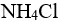 溶液混合即可作为缓冲溶液。( )
溶液混合即可作为缓冲溶液。( )在HAc-
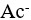 共轭酸碱对中,HAc为弱酸,
共轭酸碱对中,HAc为弱酸,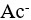 为强碱。( )
为强碱。( )一定温度下,AgCl水溶液中,
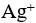 与
与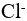 浓度的乘积是一个常数。( )
浓度的乘积是一个常数。( )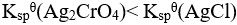 ,因此
,因此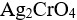 不会转化为AgCl。( ))
不会转化为AgCl。( ))- HAc溶液中加入少量的NaAc晶体,不发生变化的是( )。
配制pH=9.0的缓冲溶液,选择最佳缓冲对为( )。
已知某温度下,
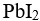 和
和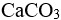 的
的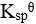 近似相等,则两者的溶解度( )。
近似相等,则两者的溶解度( )。根据酸碱质子理论,下列分子或离子为两性物质的是( )。
AgCl在下列哪种溶液中的溶解度最小( )。
- 下列哪种条件下,缓冲溶液的缓冲容量较大( )。
- 下列措施可以抑制FeCl3水解的是( )。
某溶液含有等浓度的
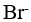 、
、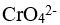 ,向此溶液中逐滴加入
,向此溶液中逐滴加入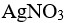 溶液时,已知:
溶液时,已知: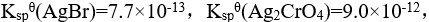 分步沉淀的顺序为( )。
分步沉淀的顺序为( )。- HgS可以溶于王水(浓HCl和浓HNO₃按体积比3:1混合)利用的是( )。
已知:
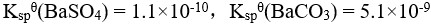 ,判断反应
,判断反应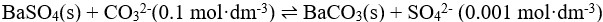 进行的方向( )。
进行的方向( )。设0.10
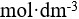 氢氰酸溶液的解离度为0.010%,则该温度下HCN的解离常数( )。
氢氰酸溶液的解离度为0.010%,则该温度下HCN的解离常数( )。向1
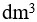 的0.10
的0.10 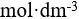 氨水溶液中加入
氨水溶液中加入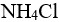 固体,M(
固体,M(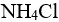 )=53.49,忽略体积变化,使溶液的pH=9.0,需要加入多少克( )。
)=53.49,忽略体积变化,使溶液的pH=9.0,需要加入多少克( )。在10
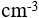 的0.0015
的0.0015 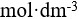 的
的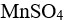 溶液中,加入5
溶液中,加入5 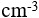 0.15
0.15 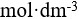 的氨水和0.495克硫酸铵晶体,不考虑体积效应,已知:
的氨水和0.495克硫酸铵晶体,不考虑体积效应,已知: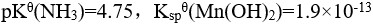 ,判断此时有无
,判断此时有无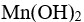 沉淀生成( )。
沉淀生成( )。若溶液中含有1.0
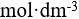 的
的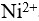 和0.1
和0.1 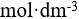 的
的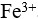 ,加NaOH使
,加NaOH使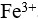 沉淀完全,而
沉淀完全,而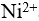 不沉淀,已知:
不沉淀,已知: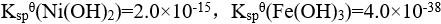 ,则溶液的pH值应控制在( )。
,则溶液的pH值应控制在( )。
A:错 B:对
答案:错
A:错 B:对
A:错 B:对
A:对 B:错
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:错 B:对
A:HAc的解离常数 B:HAc的浓度 C:HAc的解离度 D:溶液pH值
A:




A:近似相等 B:无法确定 C:
s(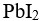 )<s(
)<s(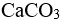 )
)
s(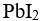 )>s(
)>s(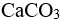 )
)
A:H2O B:
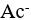
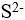
A:
0.001 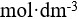 NaCl
NaCl
0.001 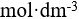
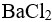
0.001 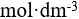
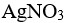
A:pH值大 B:弱酸(或弱碱)的 pK值大 C:缓冲组分的浓度比接近1 D:缓冲组分的浓度比值大
A:加碱 B:加水稀释 C:加酸 D:加热
A:
AgBr,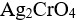
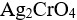 ,AgBr
,AgBr
A:酸溶解法 B:氧化还原溶解法和配位溶解法 C:氧化还原溶解法 D:配位溶解法
A:达到平衡 B:向右 C:向左 D:处于标准态
A:
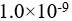
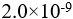
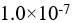
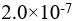
A:9.5 B:0.18 C:3.2 D:5.9
A:无法确定 B:无 C:有
A:6.7>pH>3.2 B:10.8>pH>7.3 C:pH>3.2 D:pH<10.8
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!


