提示:内容已经过期谨慎付费,点击上方查看最新答案
物理化学(上海海洋大学)
- 关系式
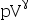 =常数,只适用于( )。
=常数,只适用于( )。 - 若使CO2在水中的溶解度为最大,应选择的条件是( )
- 在等温等压,不做其他功的情况下,下列哪一个过程是不可逆过程( )
- 某气体在恒压升温和恒容升温过程中(不做非体积功)所吸收的热量相同,假设两过程均不做非体积功,比较恒压过程体系升高的温度
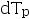 与恒容过程体系升高的温度
与恒容过程体系升高的温度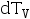 的大小。( )
的大小。( ) - 对封闭系统来说,当过程的始态和终态确定后,下列各项中没有确定的值是:( )
- 下列物质中,标准摩尔熵最大的是( )
- 以下哪个现象不违背热力学第二定律( )
- 等温等压下,在A和B组成的均相体系中,若A的偏摩尔体积随浓度的改变而增加,则B的偏摩尔体积将( )。
- 已知298.15K及101325Pa压力下,1克液态苯蒸发需要吸热439.36J,当1mol液态苯完全蒸发时其内能的变化是( )
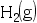 和
和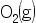 在绝热钢瓶中反应生成
在绝热钢瓶中反应生成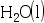 的过程( )
的过程( )- 对化学反应进度ξ,下列表述正确的是 ( )
- 对于理想气体参与的化学反应,其ΔH和ΔU的相对大小是( )
- 理想气体自相同始态出发分别经过绝热可逆和绝热不可逆膨胀过程达到相同的终态体积,则下列选项中正确的是
- 人在室内休息时,大约每天要吃0.2
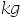 的酐酪(摄取的能量约为4000
的酐酪(摄取的能量约为4000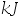 )。假定这些能量全部不储存在体内,为了维持体温不变,这些能量全部变为热使汗水蒸发。已知水的汽化热为44
)。假定这些能量全部不储存在体内,为了维持体温不变,这些能量全部变为热使汗水蒸发。已知水的汽化热为44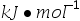 ,则每天需喝水 ( )
,则每天需喝水 ( ) - 恒压下,1mol的单原子理想气体从25℃可逆降温至0℃,此过程的熵变是( )
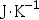
- 1mol理想气体经一定温可逆膨胀过程,则( )
- 某液体在恒温恒压下蒸发为蒸气,过程中的
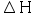 ( )
( ) - 1 mol理想气体,经途径A由某一初始压力
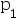 恒温可逆膨胀到压力
恒温可逆膨胀到压力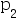 ,体积
,体积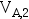 ; 经途径B,绝热可逆膨胀到压力
; 经途径B,绝热可逆膨胀到压力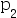 ,体积
,体积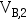 。则有:( )
。则有:( ) - 熵增加的过程一定是自发过程。( )
- 不可逆过程的熵是不会减少的。( )
- 系统达到平衡的时候,熵值最大,吉布斯自由能最小。( )
- 体系与环境之间没有热量交换则体系的温度必然恒定;若体系的温度恒定则体系与环境之间必然无热量交换。( )
- 可逆过程中,体系对环境做功最大,而环境对体系做功最小。( )
- 如果体系放热,则其内能一定减少。( )
- 某绝热体系在接受了环境所做的功之后,其温度一定升高。( )
- 隔离体系中发生的任何变化其△U=0,因此△H也为0。( )
- 在一绝热体系中,水向真空蒸发为水蒸气(以水和水蒸气为体系)。该过程中,W>0,ΔU>0。( )
- 不可逆过程的熵变是不可求的。( )
- 液态水在100℃、101.325kPa下蒸发为水蒸气,△G=0,△H>0,△U>0。( )
- 可逆的化学反应就是可逆过程。( )
- 在373.15 K,101.325 kPa下,1 mol
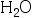 (l)蒸发为水蒸气。(假设为理想气体),因为此过程中系统的温度不变,所以ΔU=0。( )
(l)蒸发为水蒸气。(假设为理想气体),因为此过程中系统的温度不变,所以ΔU=0。( ) - 因为
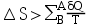 ,所以体系由初态
,所以体系由初态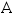 经历不同的不可逆过程到达终态
经历不同的不可逆过程到达终态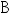 ,其熵的改变值各不相同。( )
,其熵的改变值各不相同。( ) - 一理想气体系统,由体积V1变为V2(V1>V2),温度不变,分别经历一步,两步,三步和无限多步四条途径,相应的功为W1,W2,W3和W,W1>W2>W3>W。( )
- 热在任何情况下都不能完全转变为功。( )
- 根据熵增加原理,宇宙会自发朝熵增加的方向变化,因此会最终湮灭。( )
- 当体系的状态一定时,所有的状态函数都有一定的数值。( )
- 某物质在某溶剂中的溶解度( )
- 在一定温度下,水在其饱和蒸汽压下汽化,下列各函数增量中哪一项为零( )
- 如果只考虑温度的影响,纯物质系统最多可以共存几个相( )
- 克拉佩龙方程表示( )
- 某系统存在任意量 C(s)、
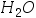 (g)、CO(g)、C
(g)、CO(g)、C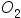 (g),
(g),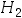 (g)五种物质,相互建立了下述三个平衡:
(g)五种物质,相互建立了下述三个平衡: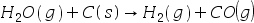 ,
, 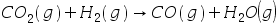 ,
, 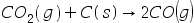 。则该系统的独立组分数C为:( )。
。则该系统的独立组分数C为:( )。 - 在相图上,当物系点处于哪一点时,只存在一个相( )
- CuSO4 (s)与H2O能生成如下固体水合物:CuSO4·H2O(s)、 CuSO4·3H2O (s)、CuSO4·4H2O(s)、CuSO4·5H2O (s)。在一定压力下,能与水溶液、冰共存的固体水合物最多有( )种。
- 对于恒沸混合物体系,经精馏塔能分离可以得到( )
- 体系中的物种数
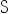 和组分数
和组分数 都是固定的。( )
都是固定的。( ) - 水的相图中,液-固两相平衡线不能任意延长,终止于临界点为
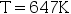 ,
,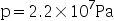 ,这时液-固界面消失。( )
,这时液-固界面消失。( ) - 某两相在同一温度下但压力不等,这两相可以达到平衡。( )
- 将双组分进行连续的部分气化和部分冷凝,使混合液得以分离就是精馏的原理。( )
- 二元体系相图中,物系点移动方向是垂直上下,而相点则水平移动。( )
- 二元液系中若A组分对拉乌尔定律产生正偏差,那么在T-x图上必有最高恒沸点。( )
- 水的相图中,体系为三相平衡共存时,P=3,f=0,该点为水的三相点,也是水的冰点。( )
- 一单相体系,如果有三种物质混合组成,它们不发生化学反应,则描述该系统状态的独立变量数应为3。 ( )
- 根据定义,所有体系的广度性质都有可加和性质。( )
- 加入任何溶质都能使溶液的沸点升高。( )
- 所谓稀溶液的渗透压就是为阻止溶剂从稀溶液一端透过半透膜向浓溶液一边迁移在浓溶液上加的额外压力。( )
- 在一个多组分溶液中,只有溶质才有偏摩尔量。( )
- 如同理想气体一样,理想液态混合物中分子间没有相互作用力。( )
- 两组分混合成溶液时,没有热效应产生,此时形成的溶液为理想液态混合物。( )
- 化学势的判据就是吉布斯自由能判据。( )
- 化学势与偏摩尔量是同一公式的不同表达方式。 ( )
- 下述化学势的公式中,不正确的是( )
- 以下变量中不会影响偏摩尔量数值的是:( )
- 在298.15K时,A和B两种气体在同一溶剂中的亨利常数分别为
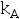 =2
=2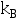 ,当A和B压力相同时,在该溶液中A和B的浓度关系为( )
,当A和B压力相同时,在该溶液中A和B的浓度关系为( ) - 二组分理想溶液的总蒸汽压是( )
- 将非挥发性溶质溶于溶剂中形成稀溶液时,将引起( )
- 某物质溶于互不相溶的两液相α和β中,该物质在α相以A的形式存在,在β相以A2形式存在,则定温定压下,两相平衡时( )
- 下列各式中哪个是化学势:( )
- 已知水的两种状态A(369K,101.3kPa,g) 、B(369K,101.3kPa,l),则
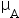 与
与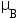 的关系为( )
的关系为( ) - 弯曲液面产生的附加压力的方向总是指向曲面的曲率中心。( )
- 定温下表面张力不随浓度变化时,浓度增大,吸附量不变。( )
- 同一个体系,表面吉布斯自由能单位为
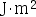 ,表面张力单位为
,表面张力单位为 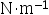 ,两者数值不同。 ( )
,两者数值不同。 ( ) - 液滴越大,液体受到的附加压力越大;液体的表面张力越大,附加压力越大。( )
- 体系表面积增大过程中得到的表面功等于吉布斯自由能的增加量。( )
- 自然界中不存在天然的纳米体系,因为纳米体系的能量非常高,过于活泼。( )
- 表面张力和表面吉布斯能虽然物理意义和单位不同,但它们是等价的,具有相同的量纲和数值。( )
- 表面能和表面张力都是标量。( )
- 一根毛细管插入水中,液面上升高度为h,当在水中加入少量NaCl,这时毛细管中液面的高度为( )
- 微小晶体与同一种的大块晶体比较,下列说法中不正确的是 ( )
- 在一抽真空的室温玻璃罩中存放两个半径不等的圆形汞滴,系统内大小汞滴未达平衡时,汞蒸汽的压力p与大汞滴的饱和蒸气压
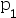 和小汞滴的饱和蒸气压
和小汞滴的饱和蒸气压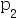 的关系是( )
的关系是( ) - 胶束的出现标志着表面活性剂的:( )
- 同外压恒温下,微小液滴的蒸气压比平面液体的蒸气压:( )
- 液体的内压力和表面张力的联系与区別在于( )
- 附加压力产生的原因是( )。
- 常见亚稳态现象都与表面性质有关,下面说法正确的是:( )
- 若将某一种电解质溶液稀释,那么它的摩尔电导率也会下降。( )
- 原电池的正极为阴极,负极为阳极。( )
- 离子独立运动定律只适用于无限稀薄的强电解质溶液。( )
- 若正离子迁移速率比负离子迁移速率大,会使得溶液中阴极一边浓度增大,阳极一边浓度减小。( )
- 法拉第定律:在电极发生电极反应的物质的量与通过电极的电量成反比。( )
- 恒温恒压下
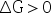 ,反应一定不能进行。( )
,反应一定不能进行。( ) - 电解池中,正离子向阴极迁移,负离子向阳极迁移。( )
- 可逆电池的两个必要条件是1)电池反应必须是可逆的 2)通入的电流无限小。( )
- 在25℃无限稀薄的水溶液中,离子摩尔电导率最大的是( )。
- 电池
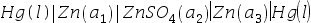 的电动势:( )。
的电动势:( )。 - 对应电池
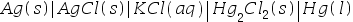 的化学反应是: ( )
的化学反应是: ( ) - 在浓度相同时,含有1mol
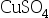 溶液的电导率是含有1mol(
溶液的电导率是含有1mol(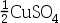 )溶液的( )
)溶液的( ) - 已知某电导池的电导池系数为125.4 m-1,当其中盛有CaCl2溶液时,测得电阻为1050Ω,则该溶液的电导率κ=( )S* m-1。
- 在电极分类中,属于金属电极为: ( )
- 298K时,当溶液的浓度从0.01
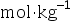 增加到0.1
增加到0.1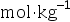 时,其电导率
时,其电导率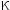 和摩尔电导率
和摩尔电导率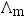 。( )
。( ) - 无限稀薄的KCl溶液中,
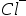 离子的迁移数为0.505,该溶液中
离子的迁移数为0.505,该溶液中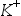 离子的迁移数为:( )。
离子的迁移数为:( )。
A:理想气体任意过程 B:理想气体绝热过程 C:理想气体绝热可逆过程 D:任何气体绝热可逆过程
答案:理想气体的绝热可逆过程
A:高温高压 B:低温低压 C:高温低压 D:低温高压
答案:低温高压
A: B: C:与无关 D:
AI参考:正确答案是D:不可逆过程是指系统经历一种宏观过程,微观上系统不能自发地由一个平衡态通过绝热的方式恢复到初态,而在给定的条件下,这个过程是不可逆的。在等温等压,不做其他功的情况下,只有化学反应中的化学能转化为热能的过程是不可逆过程。因此,本题的正确选项是D:不可逆过程是指系统经历一种宏观过程,微观上系统不能自发地由一个平衡态通过绝热的方式恢复到初态。'
A:≥ B:< C:= D:>
答案:C恒压过程有体积功存在.
A:Q+W B:Q C:Q(W=0) D:W(Q=0)
答案:W
A: B: C: D:
答案:硫酸镁
A:没有漏气、没有摩擦的理想热机,其效率可能是100% B:桶中浑浊的泥水在静置一段时间后,泥沙下沉,上面的水变清,泥、水自动分离 C:一杯热茶在打开盖后,茶会自动变得更热 D:热量自发地从低温物体传到高温物体
AI参考:B选项“桶中浑浊的泥水在静置一段时间后,泥沙下沉,上面的水变清,泥、水自动分离”不违背热力学第二定律。热力学第二定律指出,在一个封闭系统中,能量转化和传递的方向是确定的,即不可能从单一热源取热使之完全转换为有用的功而不产生其他影响。在这个过程中,能量不能完全被利用,所以理想热机的效率不可能达到100%。而B选项描述的是自然现象,泥沙和水在静置一段时间后会自动分离,没有违反热力学第二定律。其他选项都违背了热力学第二定律。A选项:没有漏气、没有摩擦的理想热机,其效率不可能达到100%,因为存在能量转化和传递的过程。C选项:一杯热茶在打开盖后,茶会自动变得更热,是因为茶与周围环境发生热交换,导致茶的温度降低,这种过程需要消耗其他形式的能量。D选项:热量自发地从低温物体传到高温物体,但需要外界提供能量,如加热等,违反了热力学第二定律。因此,本题选B。'
A:减小 B:增加 C:不变 D:不一定
A: B: C: D:
AI参考:液态苯的汽化是一个熵增加、绝热增温的可逆过程,因此液态苯蒸发成气态苯时,其内能增加。已知298.15K及101325Pa压力下,1克液态苯蒸发需要吸热439.36J,当1mol液态苯完全蒸发时其质量为$m = 18g$,即需要吸热$Q = 439.36 \times 18 = 8208.48J$,因此其内能的变化是B选项。'
A: B: C: D:
AI参考:正确选项是C:该问题描述的是一种化学反应过程,其中两个物质在绝热钢瓶中反应生成第三个物质。由于没有提供具体的化学反应方程式和反应条件,我们无法确定具体的反应过程和反应产物。因此,无法确定选项A、B、D是否正确。而C选项表示的是绝热钢瓶中发生了一种化学反应,生成了另一个物质,这符合问题的描述,因此是正确的。'
A:对指定的反应,ξ值与物质的选择有关 B:ξ值是体系的状态函数,其值不小于零 C:对指定的反应,随反应的进行ξ值不变 D:ξ值与反应式的写法无关
A:ΔH=ΔU B:不确定 C:ΔH>ΔU D:ΔH<ΔU
A: B: C: D:
A:3.0 B:0.5 C:1.6 D:1.0
A:-1.00 B:-2.00 C:-5.00 D:-1.82
A:△G=△F B:无法确定 C:△G>△F D:△G<△F
AI参考:正确选项为C:△G>△F。理想气体经一定温可逆膨胀过程,需要经历两个步骤:第一步是气体从某一初始状态膨胀至等温状态,第二步是将膨胀过程中获得的内能转移给外界做功。因此,这个过程中既有内能的变化,又有对外做功的情况,而这个过程中需要用到自由能的概念,即△G=△H-T△S。由于可逆过程熵变较大,因此△S>0,而可逆膨胀过程需要消耗一定的功,即△H>0,因此△G>0。而膨胀过程中对外做功的大小取决于气体体积的变化量,与是否可逆无关,因此无法确定△F的大小。综上所述,选项C为正确答案。'
A: B:无法确定 C: D:
A:条件不足,无法判断 B:< C:= D:>
AI参考:正确答案是【C:=】。途径A是恒温可逆膨胀,途径B是绝热可逆膨胀,两者都是等温过程且过程前后气体物质的量不变,因此两途径的前后气体压强相等。所以答案是C:=。'
A:对 B:错
A:错 B:对
A:对 B:错
A:错 B:对
AI参考:答案:A: 错。这是一个关于热力学的问题。根据热力学第一定律,体系与环境之间的热量交换并不影响体系的温度,因此体系与环境之间没有热量交换并不意味着体系的温度必然恒定。同样,体系的温度恒定也不意味着体系与环境之间必然无热量交换,因为其他形式的能量(如内能、势能等)的变化也可能导致体系的温度发生变化。因此,这个判断题是错误的。'
A:对 B:错
A:对 B:错
A:对 B:错
A:对 B:错
AI参考:答案是B:错。根据热力学第一定律,隔离体系中发生的任何变化其ΔU=Q+W,ΔH=ΔU+Δ(pV)。因此,ΔH不一定为0,需要具体分析过程来确定其值。因此,本题判断错误。'
A:对 B:错
A:错 B:对
A:对 B:错
AI参考:B:错。液态水在100℃、101.325kPa下蒸发为水蒸气是一个自发过程,△G=0,△H<0,△U>0。因此,该题表述错误。'
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
AI参考:答案:A。理想气体状态方程:pV = nRT,其中p为气体压强,V为气体体积,n为气体的物质的量,R为气体常数,T为绝对温度。根据题目描述,理想气体系统由体积V1变为V2(V1>V2),温度不变,说明气体的压强和体积同时发生变化。对于一步过程,气体做功的公式为:W = pΔV。由于V1>V2,所以ΔV = V2 - V1 > 0,即气体体积增大,做负功。由于气体压强不变,所以做功的大小只取决于体积的变化量,即W = -ΔV = -(V2 - V1)< 0。对于两步过程,由于题目中没有给出具体的两步过程,无法判断做功的大小。对于三步过程和无限多步过程,由于题目中没有给出具体的三步和无限多步过程,无法判断做功的大小。综上所述,一步过程做功的大小取决于体积的变化量,而两步、三步和无限多步过程无法确定做功的大小。因此,选项A是正确的。'
A:对 B:错
AI参考:答案是B:错。热在一般情况下可以完全转变为功,但需要一定的条件和设备。在现实中,热和功之间的转换需要通过一定的设备和工艺流程来实现,而且需要考虑各种因素的影响,如温度、压力、物质的性质等等。因此,不能简单地说热在任何情况下都不能完全转变为功。'
A:对 B:错
AI参考:答案是B:错。根据熵增加原理,宇宙会自发朝熵增加的方向变化,但并不会最终湮灭。宇宙会不断地演化和扩张,而不是最终湮灭。因此,这个判断题是错误的。'
A:错 B:对
A:同是温度和压力的函数 B:仅是压力的函数 C:仅是温度的函数 D:除了温度压力以外,还是其他因素的函数
AI参考:正确选项是【C:仅是温度的函数】。溶解度是一个物质在特定溶剂中达到饱和状态时所需的温度。这个条件限制了溶解度只与温度有关,而与其他压力、其他因素无关。温度升高时,物质的溶解度通常会提高。因此,正确答案为C:仅是温度的函数。'
A: B: C: D:
A:P=2 B:P=1 C:P=3 D:P=4
A:任意状态下压力随温度的变化率 B:以上说法都不对 C:它适用于任何物质的两相平衡 D:两相平衡时的平衡压力随温度而变化的变化率
AI参考:正确答案是D:两相平衡时的平衡压力随温度而变化的变化率。克拉佩龙方程是用于描述两相平衡时平衡压力随温度变化的变化率的方程,选项D正确。而选项A、B、C都与克拉佩龙方程的含义不符。因此,正确答案是D。'
A:3 B:2 C:4 D:1
A:恒沸点 B:熔点 C:临界点 D:最低共沸点
A:2 B:4 C:1 D:3
A:一个恒沸混合物和一个纯组分 B:一个纯组分 C:两个恒沸混合物 D:两个纯组分
AI参考:正确答案是【B:一个纯组分】。恒沸混合物体系经精馏塔分离可以得到一个纯组分。这是因为恒沸混合物是两个或两个以上沸点相近的物质所形成的混合物,物质间以一定的摩尔分数的沸点出现的特性。故无法进行再精馏操作。若要对含有恒沸物的混合物进行分离,需对原料气体或液体加热到稍低于某一恒沸点的温度,原料液体气化并从汽液混合物中提取一部分作为馏出液,与此同时馏出液同时又会因原料液体的挥发而浓缩,这样分离得到的馏出液往往仍含有恒沸组分,故可继续上述操作。在精馏塔中可得到纯组分。因此,本题答案为B。'
A:对 B:错
AI参考:答案是B:错。体系中的物种数和组分数都是可以变化的,而不是固定的。在化学化工等学科中,体系中的物种数和组分数是用来描述反应系统和相态的重要参数。随着化学反应和相态变化,体系中的物种数和组分数也会随之改变。因此,这个问题的判断是错误的。'
A:错 B:对
AI参考:正确答案是B:对。水的相图中,液-固两相平衡线不能任意延长,终止于临界点为两个不同的点,这时液-固界面消失。这是相图中的基本原理之一。因此,这个说法是正确的。'
A:对 B:错
AI参考:答案是B:错。两相在同一温度下但压力不等,这两相不可能达到平衡,因为压力不同会影响物质的密度、分子结构等物理化学性质,从而影响物质的化学反应速率和平衡移动。因此,这两相不会达到化学平衡状态。'
A:对 B:错
A:错 B:对
A:错 B:对
A:错 B:对
AI参考:水的相图中,体系为三相平衡共存时,P=3,f=0,该点为水的三相点,同时也是水的沸点。因此,选项B“对”是正确的答案。'
A:错 B:对
A:对 B:错
AI参考:B:错。并非所有体系的广度性质都有可加和性质,某些性质不能直接相加。因此,这个说法是不正确的。"
A:错 B:对
A:对 B:错
AI参考:正确答案是A:对。 稀溶液的渗透压就是指稀溶液的沸点升高值在相同压力下降低的水蒸气压与浓溶液浓度的乘积,用来阻止溶剂从稀溶液向浓溶液一边扩散而产生渗透作用,是维持渗透平衡的压力差。因此本题说法正确。"
A:对 B:错
A:对 B:错
A:对 B:错
AI参考:答案是B:错。 理想液态混合物是指组分间不发生任何化学或物理变化,并且没有任何热效应的混合物。而两组分混合成溶液时,如果其中一部分会发生化学变化或存在化学势差,或者存在热效应,则不会形成理想液态混合物。因此,该判断题是错误的。"
A:错 B:对
AI参考:选项A:错误。 化学势判据和吉布斯自由能判据都是用来判断系统在某一状态下,系统达到平衡时,系统向着哪一个方向进行反应的依据。化学势判据主要是根据化学反应中物质转移的方向和速率来判定的,而吉布斯自由能判据则考虑了系统的体积变化、温度、压力等因素的影响。因此,化学势判据和吉布斯自由能判据在某些情况下可以相互补充,但不能完全等同。"
A:对 B:错
AI参考:A. 对。化学势与偏摩尔量是同一公式的不同表达方式,两者是等价的。"
A: B: C: D:
A:质量 B:浓度 C:压强 D:温度
AI参考:正确选项是【A:质量】 偏摩尔量是表示物系内物质个体数量或质量差异的量,与物质的量、质量、体积等有关。在四个选项中,只有质量不会影响偏摩尔量的数值,浓度、压强和温度都会影响偏摩尔量的数值。浓度会影响物质的个体的数量或质量,压强会影响物系内气体分子个体的动能,温度会影响物系内分子热运动能量。因此,正确答案是A:质量。"
A: B: C:不能确定 D:
A:与溶液的组成无关 B:介于二纯组分蒸汽压之间 C:小于纯组分的蒸汽压 D:大于纯组分的蒸汽压
AI参考:正确答案是C:小于纯组分的蒸汽压。 理想溶液的蒸汽压小于纯组分的蒸汽压,因为理想溶液中各组分之间的相互作用仅存在于液体分子之间和气体分子之间,而气体分子之间没有相互作用力。因此,二组分理想溶液的总蒸汽压是小于纯组分的蒸汽压。"
A:蒸汽压升高 B:沸点升高 C:都不对 D:熔点升高
A: B: C: D:
A: .w65223610491s .brush0 { fill: rgb(255,255,255); } .w65223610491s .pen0 { stroke: rgb(0,0,0); stroke-width: 1; stroke-linejoin: round; } .w65223610491s .font0 { font-style: italic; font-size: 204px; font-family: "Times New Roman", serif; } .w65223610491s .font1 { font-style: italic; font-size: 262px; font-family: "Times New Roman", serif; } .w65223610491s .font2 { font-style: italic; font-size: 406px; font-family: "Times New Roman", serif; } .w65223610491s .font3 { font-size: 262px; font-family: "Times New Roman", serif; } .w65223610491s .font4 { font-size: 406px; font-family: "Times New Roman", serif; } .w65223610491s .font5 { font-size: 373px; font-family: Symbol, serif; } .w65223610491s .font6 { font-weight: bold; font-size: 76px; font-family: System, sans-serif; } z n p T B n F , , ) / ( ¶ ¶ B: .w65223610515s .brush0 { fill: rgb(255,255,255); } .w65223610515s .pen0 { stroke: rgb(0,0,0); stroke-width: 1; stroke-linejoin: round; } .w65223610515s .font0 { font-style: italic; font-size: 204px; font-family: "Times New Roman", serif; } .w65223610515s .font1 { font-style: italic; font-size: 262px; font-family: "Times New Roman", serif; } .w65223610515s .font2 { font-style: italic; font-size: 406px; font-family: "Times New Roman", serif; } .w65223610515s .font3 { font-size: 262px; font-family: "Times New Roman", serif; } .w65223610515s .font4 { font-size: 406px; font-family: "Times New Roman", serif; } .w65223610515s .font5 { font-size: 373px; font-family: Symbol, serif; } .w65223610515s .font6 { font-weight: bold; font-size: 76px; font-family: System, sans-serif; } z n p T B n U , , ) / ( ¶ ¶ C: .w65223610467s .brush0 { fill: rgb(255,255,255); } .w65223610467s .pen0 { stroke: rgb(0,0,0); stroke-width: 1; stroke-linejoin: round; } .w65223610467s .font0 { font-style: italic; font-size: 204px; font-family: "Times New Roman", serif; } .w65223610467s .font1 { font-style: italic; font-size: 262px; font-family: "Times New Roman", serif; } .w65223610467s .font2 { font-style: italic; font-size: 406px; font-family: "Times New Roman", serif; } .w65223610467s .font3 { font-size: 262px; font-family: "Times New Roman", serif; } .w65223610467s .font4 { font-size: 406px; font-family: "Times New Roman", serif; } .w65223610467s .font5 { font-size: 373px; font-family: Symbol, serif; } .w65223610467s .font6 { font-weight: bold; font-size: 76px; font-family: System, sans-serif; } z n p T B n G , , ) / ( ¶ ¶ D:
AI参考:正确选项是B,这是因为选项B中“n”符号表示的是化学势。化学势是描述化学系统中物质在化学势场中的相对位置的物理量,用于描述物质在系统中的状态和位置,它通常由物质的本性和体系性质决定。因此,化学势是一个非常重要的概念,在化学、化工、材料科学等领域都有广泛的应用。其他选项中给出的符号并不是化学势的表示方式。"
A:无法比较 B: C: D:
A:对 B:错
A:对 B:错
AI参考:答案:B:错。 表面张力是液体表面相邻两部分间单位面积上的相互牵引力。定温下表面张力不随浓度变化时,说明该液体为理想液体。理想液体在表面层没有附着物时,表面层的分子比较稀疏,分子间距大于内部分子间距,分子间相互吸引而产生表面张力。当吸附量达到饱和时,吸附速率等于脱附速率,溶液浓度增大,吸附量仍不变。但在吸附量未达到饱和之前,浓度增大,吸附量会增加。因此本题说法是错误的。"
A:对 B:错
AI参考:答案:B。题目中的说法是错误的。同一体系下的表面吉布斯自由能与表面张力应该是相同单位和数值的。它们都是表面物理化学性质,单位可能不同,但是数值上应该是相同的。所以答案是B,即错误选项。"
A:错 B:对
AI参考:答案是B:对。 液滴越大,液体受到的附加压力越大,这句话是正确的。因为液滴越大,液体的表面层就越厚,受到的附加压力就越大。 而液体的表面张力越大,则液体的表面层越容易收缩,因此附加压力越大,这句话也是正确的。因为表面张力会使得液体表面层产生一种向内收缩的趋势,从而使得附加压力增大。"
A:错 B:对
A:对 B:错
AI参考:答案是B:错。纳米体系可以存在于自然界中,而且它们通常表现出特殊的物理和化学性质,如高比表面积、高反应活性等。因此,自然界的物质中确实存在纳米体系。同时,由于纳米体系中的粒子尺寸非常小,其能量相对较高,但这并不意味着纳米体系过于活泼。因此,这个说法是错误的。"
A:错 B:对
AI参考:答案是B:对。表面张力和表面吉布斯能虽然物理意义和单位不同,但它们是等价的,具有相同的量纲和数值。表面张力和表面吉布斯能都是描述表面性质的概念,它们的单位不同,但它们在描述表面吸附、润湿等性质时具有相似的物理意义。因此,它们是等价的,具有相同的量纲和数值。"
A:对 B:错
AI参考:表面能和表面张力都是标量。是正确的。表面能和表面张力都是只有大小而没有方向的物理量,因此是标量。"
A:无法确定 B:等于h C:大于h D:小于h
A:微小晶体的溶解度小 B:微小晶体的饱和蒸汽压大 C:微小晶体的熔点低 D:微小晶体的表面张力未变
A: B: C: D:
A:分子远未排满溶液表面 B:分子间作用超过它与溶剂的作用; C:表面活性剂降低表面张力的能力下降; D:溶解已达到饱和;
A:不定 B:小 C:一样 D:大
A:作用点相同面方向不同 B:点相同而产生的原因不同 C:产生的原因相同而作用点不同 D:产生的原因相同而作用的方向不同
A:由于在表面上存在表面张力 B:由于表面张力的存在,在弯曲表面两边压力不同 C:难于确定 D:由于存在表面
A:过饱和蒸气是由于小液滴的蒸气压小于大液滴的蒸气压所致; B:饱和溶液陈化、晶粒长大,因为小晶粒溶解度比大晶粒大; C:过热液体形成原因是新相种子——小气泡的附加压力太小; D:人工降雨时在大气中撒入化学物质主要的目的是促进凝结中心形成
A:对 B:错
AI参考:正确答案是B:错。 摩尔电导率是电解质溶液中自由移动的离子浓度和溶液电导的倒数,与溶液的浓度有关,与溶液的稀释程度无关。因此,将某一种电解质溶液稀释,它的摩尔电导率不会下降。"
A:对 B:错
AI参考:原电池的正极得电子发生还原反应,为阴极;负极失电子发生氧化反应,为阳极。所以这个说法是错误的。 因此,答案是B:错。"
A:对 B:错
A:错 B:对
AI参考:判断题:若正离子迁移速率比负离子迁移速率大,会使得溶液中阴极一边浓度增大,阳极一边浓度减小。(对)"
A:对 B:错
A:错 B:对
AI参考:B.对。 根据题目中的图像,该反应是一个可逆反应,在恒温恒压下,正逆反应的速率相等,反应达到平衡状态。因此,该反应在一定条件下可以自发进行。题目中的说法是错误的。"
A:对 B:错
AI参考:正确答案是B:错。 电解池中,正离子向阳极迁移,负离子向阴极迁移。"
A:错 B:对
AI参考:答案是B:对。可逆电池的两个必要条件是:电池反应必须是可逆的,以及电池两极所发生的反应与所充的电解质溶液必须相互不反应(或极微反应),这样在切断外电路后,通路中就无电流,从而也就避免了由于电流通过电池而造成的电能转化为热能。选项中提到“通入的电流无限小”是正确的。因此,这个说法是正确的,即答案为B。"
A: B: C: D:
A:仅与有关,与无关 B:与均无关 C:仅与有关,与无关 D:仅与有关,与无关
AI参考:正确选项:C 分析图中电池内部的电荷流动和能量转化,可以看出电池的电动势只与电池本身的性质有关,即电池内部的化学反应和结构有关,而与电池两端的电压(即外电路的电流)无关。因此,选项C“仅与有关,与无关”是正确的。选项A、B、D都与图中信息不符。"
A: B: C: D:
AI参考:正确选项是C:锂离子电池的化学反应。 该图片中的电池化学反应是锂离子电池的充电和放电过程,电池正极使用锂化合物(如LiCoO2)作为活性物质,负极使用锂金属或锂合金作为活性物质,通过锂离子在正负极之间的迁移来充电和放电。锂离子电池的化学反应类型属于氧化还原反应。因此,选项C“锂离子电池的化学反应”是正确答案。选项A、B、D都与图片中的化学反应不符。"
A: B:2 C:4 D:
AI参考:正确答案是B,由于两者浓度的电导率之比为浓度乘积的比值,在浓度相同时,电导率相同。 浓度相等,物质的量也相等,由于电荷数的浓度与摩尔电导率乘积的乘积相同,即 K/(μ)=1,故摩尔电导率相同。因此,含有1mol
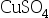 溶液的电导率是含有1mol(
溶液的电导率是含有1mol(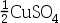 )溶液的电导率是两倍关系,所以答案为B。"
)溶液的电导率是两倍关系,所以答案为B。"A:11.19 B:0.119 C:1.119 D:0.019
A: B: C: D:
A:减小,减小 B:增加,增加 C:增加,减小 D:减小,增加
AI参考:根据图示数据,当溶液浓度从0.01增加到0.1时,电导率和摩尔电导率的变化情况是电导率减小,摩尔电导率增加。这是因为溶液的浓度增加,意味着溶液中溶质的数量增加,而电导率是衡量溶液中离子导电能力的一个指标,因此当溶质数量增加时,电导率会减小。而摩尔电导率是单位体积内溶液的离子总数与单位体积内单位电量的电导率的乘积,当溶液中离子数量增加时,摩尔电导率也会增加。因此,正确答案是A:减小,减小。"
A:0.505 B:64.3 C:67.5 D:0.495
温馨提示支付 ¥3.00 元后可查看付费内容,请先翻页预览!

