第一章 化学动力学:本章讨论化学反应速率,中心是反应速率方程,它在宏观层次上反映了反应速率随反应物和产物的浓度以及温度变化的普遍规律,其中包含作为反应特性的参数,它们在应用时必须同时输入。具体内容包括:.化学反应的速率;反应速率方程;反应速率方程的积分形式;对峙反应;连串反应;平行反应;温度对反应速率的影响;动力学实验方法;动力学实验数据的处理;反应机理与速率方程;各类反应的动力学简介。1.1前言:第一章化学动力学概述[单选题]反应
1.2化学反应的速率及速率方程:化学反应的速率
1.3反应速率方程的积分形式:这节主要介绍动力学方程
1.4复杂反应:这节主要介绍复杂反应
1.5温度对反应速率的影响:温度对反应速率的影响
1.6动力学实验方法:这节主要介绍动力学实验方法
1.7反应机理:反应机理
1.8各类反应的动力学:各类反应的动力学
选项:[
 ,
,  ,
,  ]
] [单选题]
[单选题]反应 2N2O5─→ 4NO2+ O2 在328 K时,O2(g)的生成速率为0.75×10-4mol·dm-3·s-1。则该反应的反应速率以及N2O5的消耗速率分别为( )mol·dm-3·s-1。选项:[
[单选题]
[单选题]
 选项:[NL-3T-1, L3N-1T-1, T-1]
选项:[NL-3T-1, L3N-1T-1, T-1][单选题]
[单选题]
[单选题]
 选项:[恒容, 恒压, 恒温]
选项:[恒容, 恒压, 恒温][单选题]实验测得反应:2A+B ─→2C + D 的速率方程为
[单选题]对于反应 2NO2= 2NO + O2,当选用不同的反应物和产物来表示反应速率时,其相互关系为( )。选项:[-2d[NO2]/dt = 2d[NO]/dt = d[O2]/dt, - d[NO2]/2dt = d[NO]/2dt = d[O2]/dt = V-1 dx/dt, - d[NO2]/2dt = d[NO]/2dt = d[O2]/dt = dx/dt]
[单选题]
[单选题]
[判断题]基元反应不一定符合质量作用定律。选项:[错, 对]
[单选题]
 选项:[0.50;, 0.75;, 0.25]
选项:[0.50;, 0.75;, 0.25][单选题]基元反应2A→B为双分子反应,此反应为( )反应。选项:[零级, 一级;, 二级;]
[判断题]
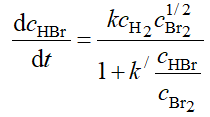 无法定义其反应级数。选项:[对, 错]
无法定义其反应级数。选项:[对, 错][单选题]
 选项:[
选项:[[单选题]
[单选题]
[单选题]零级反应( )基元反应。选项:[肯定是, 肯定不是, 不一定是]

