第二章 原子结构:(1)掌握变量分离方法求解单电子原子Schrödinger方程、量子数及其物理意义。 (2)了解径向分布函数、角度函数、径向波函数。 (3)了解算符与可测物理量和角动量的空间量子化。 (4)掌握多电子原子Schrödinger方程的近似求解和构造原理与Slater行列式。 (5)了解电离能、电子亲和势、电负性、化学硬度等原子结构参数。 (6)掌握多电子原子光谱项、光谱支项的求导。2.1单电子原子的Schrodinger方程及其解:本节主要介绍单电子原子Schrödinger方程的建立、坐标变换与变量分离、原子轨道与能级。[判断题]在多电子原子中,单个电子的动能算符均为
2.2原于轨道和电子云的图形表示:本节主要介绍作图对象与作图方法、轨道和电子云的径向部分和角度部分的对画图、等值面图与界面图、网格图、电子云黑点图、原子轨道的宇称。
2.3量子数与可测物理量:本节主要介绍算符与可测物理量和角动量的空间量子化。
2.4多电子原子的结构:本节主要介绍多电子原子Schrödinger方程的近似求解和构造原理与Slater行列式。
2.5原子结构参数:本节主要介绍电离能、电子亲和势、电负性、化学硬度。
2.6原于光谱项:本节主要介绍组态与状态、L-S矢量耦合模型、原子光谱项和光谱支项的求法、Hund规则、跃迁选律。
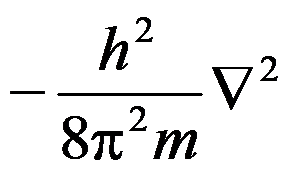 所以每个电子的动能都是相等的。( )选项:[错, 对]
所以每个电子的动能都是相等的。( )选项:[错, 对] [判断题]原子轨道是指原子中的单电子波函数。所以一个原子轨道只能容纳一个电子。( )选项:[错, 对]
[单选题]原子轨道是原子中的单电子波函数, 每个原子轨道只能容纳( )个电子。选项:[1
, 3
, 2
, 4
]
[判断题]求解氢原子的Schrödinger方程能自然得到 n, l, m, ms四个量子数。( )选项:[错, 对]
[单选题]He原子光谱项不可能是( )。选项:[1S, 2P, 3P, 1P]



